Modifizierte Peptide zeigen bessere biologische Eigenschaften für das Tumor-Targeting
Anzeigen
Forscher der Universität und des Universitätsspitals Basel haben neuartige radioaktive Verbindungen entwickelt, die sich zur Diagnose und Therapie von Tumoren und Metastasen eignen.
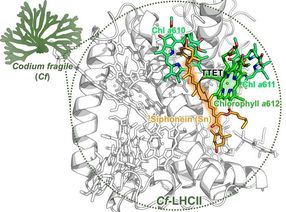
Der Ersatz eines Bausteins im Rückgrat des Peptids schützt es vor dem Abbau durch Proteasen.
Illustration aus: Valverde, I. E., Bauman, A., Kluba, C. A., Vomstein, S., Walter, M. A. and Mindt, T. L. (2013), 1,2,3-Triazoles as Amide Bond Mimics: Triazole Scan Yields Protease-Resistant Peptidomimetics for Tumor Targeting . Angew. Chem. Int. Ed., 52: 8957–8960. Copyright Wiley-VCH Verlag GmbH & Co. KGaA. Reproduced with permission.
Radiopharmazeutika stellen eine moderne Klasse von Arzneimitteln dar, die in der Nuklearmedizin Anwendung als Diagnostika und Therapeutika finden. Für eine hohe Bildqualität bzw. eine effiziente Tumortherapie sind Verbindungen gefragt, die sich schnell und gezielt im Tumorgewebe anreichern. Dafür werden heutzutage unter anderem auch radioaktiv markierte Peptide verwendet, welche spezifisch Rezeptoren von Tumorzellen erkennen.
Allerdings weisen einige vielversprechende Peptide den Nachteil auf, dass sie im Körper oft nur wenige Minuten stabil sind, bevor sie von Enzymen (Proteasen) abgebaut werden. Wenn es gelingt, die Stabilität zu erhöhen, könnte die Anreicherung im Tumorgewebe verbessert werden. Anstrengungen in diese Richtung waren bisher aber nur teilweise erfolgreich. Die Herausforderung liegt darin, die Stabilität der Verbindungen zu verbessern, ohne dadurch erwünschte biologische Eigenschaften zu beeinträchtigen.
Austausch eines Bausteins
Wissenschaftler/innen der Universität und des Universitätsspitals Basel berichten nun von einer innovativen Methode, um dieses Ziel zu erreichen. Sie tauschten systematisch einen Baustein im Rückgrat eines Peptids aus; genauer gesagt ersetzten sie Amidbindungen durch eine Triazoleinheit unter Anwendung der «Klick-Chemie».
In Zell- und Tierexperimenten konnten die Forscher um Prof. Thomas Mindt zeigen, dass die so hergestellten Verbindungen eine bis um das fünffach erhöhte Stabilität aufwiesen und daher langsamer abgebaut wurden. Gleichzeitig bewahrten sie die Fähigkeit, an Tumorzellen zu binden, was zu einer verbesserten Tumoraufnahme führte.
Die an Universität und Universitätsspital Basel entwickelte Methode ermöglicht eine effiziente Synthese von Peptidmimetika mit verbesserten biologischen Eigenschaften. «Wir glauben, dass die Methode im Bereich des Tumor-Targetings mit kleinen Peptiden eine breite Anwendung finden wird, insbesondere im Wirkstofftransport, der molekularen Bildgebung und der Endoradiotherapie», so Forschungsleiter Prof. Thomas Mindt.