Krebsmedikament wirkt gegen Viren
Anzeigen
Forschende des TWINCORE beschreiben einen Mechanismus, der Virusvermehrung hemmt und Zellen vor Schaden schützt. Interessant: Ein bereits zugelassener Wirkstoff könnte sich als nützlich erweisen, um verschiedene Viren zu bekämpfen.

Erstautor Fakhar Waqas (l.) und Projektleiter Frank Peßler im Labor
© TWINCORE/Grabowski
AIDS, die Grippe, COVID-19 – immer wieder überrollen Virusinfektionen ganze Weltregionen und kosten Menschenleben. Bis heute gibt es keine Medikamente mit breiter antiviraler Wirkung. Forschende aus Hannover wollen das ändern: Im Fachjournal PLOS Pathogens beschreiben Prof. Frank Peßler und sein Team am TWINCORE - Zentrum für Experimentelle und Klinische Infektionsforschung, einer gemeinsamen Einrichtung des Helmholtz-Zentrums für Infektionsforschung und der Medizinischen Hochschule Hannover, einen Weg, die Vermehrung unterschiedlichster Viren wirksam zu hemmen. Für die nun veröffentlichte Studie arbeiteten die Forschenden der Arbeitsgruppe Biomarker für Infektionskrankheiten zusammen mit Teams der Universitäten in Gießen und Aarhus sowie des Helmholtz-Instituts für Pharmazeutische Forschung Saarland (HIPS). Gefördert wurde das Projekt im Programm COVID-Protect des Bundesministeriums für Bildung und Forschung (BMBF).
Therapeutische Angriffspunkte bei Menschen
Dass es so kniffelig ist, Viren zu bekämpfen, liegt zum einen an ihrem einfachen Aufbau. Sie bieten nur wenige Angriffspunkte für hemmende Wirkstoffe. Zudem verändern sie sich immer wieder so, dass Wirkstoffe ihr Ziel nicht mehr erkennen. Für ihre Vermehrung nutzen die aus wenigen Komponenten bestehenden Viren körpereigene Strukturen ihres Wirtes, also zum Beispiel des Menschen. Auch weil schwere Auswirkungen einer Virusinfektion häufig einer übermäßigen Reaktion des Abwehrsystems geschuldet sind, richten Forschende ihr Augenmerk zunehmend auf das Zusammenspiel von Virus, der menschlichen Physiologie und dem Abwehrsystem. Ziel ist es, Mechanismen im Körper zu finden, die therapeutisch gehemmt oder verstärkt werden können, um eine Virusinfektion zu bremsen und ihre Auswirkungen zu lindern. Den Forschenden um Frank Peßler ist es nun gelungen, zwei Mechanismen in menschlichen Zellen gleichzeitig so zu beeinflussen, das beides geschieht.
Richtiger Wirkstoff, unerwarteter Mechanismus
Peßler und seine Mitarbeitenden erforschen das körpereigene Molekül Itakonsäure. Bereits vor einiger Zeit entdeckten sie, dass eine pharmakologisch optimierte Variante davon, 4-Octyl-Itaconat, besonders effizient einen Signalweg aktiviert, der verschiedene Schutz- und Abwehrmechanismen menschlicher Zellen steuert. Der Schalter für diesen Signalweg ist ein Protein mit dem Namen NRF2. Immer wieder ergaben ihre Experimente aber auch Hinweise, dass 4-Octyl-Itaconat die Virusvermehrung direkt beeinträchtigt - unabhängig vom NRF2-Signalweg. Um diesen Hinweisen nachzugehen, stellten sie im Labor Zellen ohne NRF2-Protein her. Fehlte der Schutzschalter, vermehrten sich Influenzaviren tatsächlich besser. Zu ihrer Überraschung stellten die Forschenden jedoch fest: Auch ohne NRF2 hemmt 4-Octyl-Itaconat die Vermehrung der Grippeviren, und zwar ebenso stark wie in unveränderten Zellen.
„Als wir die ersten Ergebnisse dieser Versuche sahen, haben wir nicht schlecht gestaunt“, sagt Frank Peßler. „Wir hatten offenbar die ganze Zeit den richtigen Wirkstoff untersucht, sind aber erst jetzt dem entscheidenden Wirkmechanismus auf die Spur gekommen.“
Transportweg blockiert
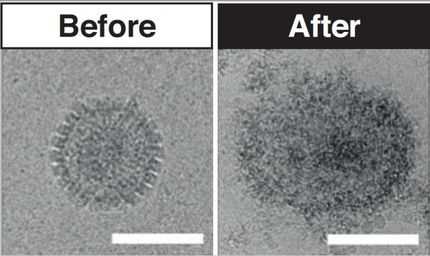
Peßler und seine Mitarbeitenden vermuteten, dass 4-Octyl-Itaconat den Transport von Proteinen und Nukleinsäuren aus dem Zellkern behindere, auf den viele Viren angewiesen sind. Um ihre Vermutung zu überprüfen, verglichen sie den Effekt von 4-Octyl-Itaconat mit dem eines Krebsmedikamentes (Selinexor), das einen Transportkanal aus dem Zellkern blockiert. Sowohl das Krebsmedikament wie auch die Itaconsäure-Variante hemmten die Vermehrung eines Influenzavirus. Sie verhinderten, dass Vorstufen der neu gebildeten Viruspartikel aus dem Kern der Wirtszelle transportiert wurden. Die unfertigen Viren blieben sozusagen im Zellkern stecken. „Wir waren sehr überrascht, wie effizient 4-Octyl-Itaconat die Vermehrung von Influenzaviren durch diesen Mechanismus direkt hemmt“, sagt Peßler. Eine Erklärung für ihre Beobachtung liefern die Autorinnen und Autoren der aktuellen Studie gleich mit: In der Struktur des Transportkanals fanden sie eine Stelle, an die sowohl 4-Octyl-Itaconat als auch das Krebsmedikament binden. Sie ähnelt der Stelle, an der 4-Octyl-Itaconat mit dem Protein interagiert, das den Schalter NRF2 kontrolliert. Mittels biochemischer Methoden konnten die Forschenden nachweisen, dass 4-Octyl-Itaconat tatsächlich an den Kerntransporter in menschlichen Zellen bindet und ihn dadurch blockiert. Auch mit weiteren Substanzen, die bisher nur als NRF2-Aktivatoren bekannt waren, beobachteten Peßler und seine Mitarbeitenden diesen Effekt.
Potential für breite Wirksamkeit
Die nun veröffentlichten Erkenntnisse eröffnen neue Perspektiven für die Entwicklung antiviraler Therapien. Interessanterweise sind nämlich verschiedenste Viren mit ganz unterschiedlichen Lebenszyklen auf den Export von Proteinen oder Nukleinsäuren aus dem Kern angewiesen. Vom Influenzavirus, das die saisonale Grippe verursacht, und SARS-CoV-2 über das Respiratorische Synzytial-Virus (RSV), das vergangenen Winter zahlreiche Kleinkinder ins Krankenhaus brachte, bis hin zur Tollwut, die in vielen asiatischen und afrikanischen (Reise-)Ländern wieder stärker verbreitet ist - sie alle brauchen den Transportkanal, um sich zu vermehren. Bei unterschiedlichen Viren sind dabei verschiedene Schritte der Vermehrung von dem Kanal abhängig. Diesen Weg zu blockieren verspricht daher, vielen verschiedenartigen Viren entgegenzuwirken.
Viren bremsen, Zellen schützen
Auch neu auftretende Viren könnten auf diese Art möglicherweise gebremst werden. „Die nächste Pandemie kommt bestimmt“, sagt Frank Peßler. „Und wäre es nicht schön, eine Tablette zu haben, mit der man den Menschen schnell helfen und die Ausbreitung früh eindämmen kann - sogar bevor man genau weiß, um welches Virus es sich handelt?“
Dass ein Inhibitor des Transportkanals bereits als Medikament zugelassen ist, eröffnet Perspektiven auf eine zügige Anpassung der Therapie an virale Infektionen. Allerdings besitzt dieses Medikament nicht die zellschützenden Eigenschaften der NRF2-Aktivatoren. Peßler plant deshalb, chemische Varianten der Itakonsäure so zu optimieren, dass sie gleichermaßen virushemmend und zellschützend wirken. Dass die Itakonsäure körpereigenen Ursprungs ist, lässt hoffen, dass dabei Wirkstoffkandidaten mit möglichst wenig unerwünschten Nebeneffekten herauskommen.