Molekulare Grundlagen der familiären Herzmuskelschwäche
Nur ein einziger Eiweiß-Baustein ist vertauscht
Anzeigen
Für ihre Arbeit zu den molekularen Grundlagen der vererbten Herzmuskelschwäche wurde Stephanie Reis, Doktorandin der Graduate School of Chemistry and Biochemistry der Ruhr-Universität, mit dem mit 20.000 Euro dotierten Forschungspreis der Dresdner Herz-Kreislauftage e.V. ausgezeichnet. Sie erforscht in ihrer Dissertation die Auswirkungen einer bestimmten Mutation auf die Fähigkeit erwachsener Herzmuskelzellen, sich zusammenzuziehen. Überraschenderweise zeigte sich auch, dass die Herzmuskelzellen durch die Mutation verändert auf das Stresshormon Adrenalin reagieren.
Die familiäre Hypertrophe Kardiomyopathie ist eine der häufigsten vererbbaren Herzkrankheiten. Es handelt sich dabei allerdings nicht um eine immer gleiche Mutation eines Gens, sondern um verschiedene Mutationen, die unterschiedliche Auswirkungen haben können. Charakteristisch ist eine Verdickung der Wand der linken Herzkammer. Während manche Betroffene allerdings wenig oder keine Beschwerden haben, leiden andere unter gefährlichen Herzrhythmusstörungen, Leistungsschwäche, Atemnot und sind vom plötzlichen Herztod bedroht. Der Schwerpunkt der Arbeitsgruppe von Prof. Jaquet liegt in der Aufklärung von molekularen Mechanismen der familiären, Hypertrophen Kardiomyopathie, die bislang noch weitgehend unbekannt sind. Stephanie Reis untersuchte eine spezifische Veränderung in einer Erbanlage (Mutation), welche in einem fehlerhaften Eiweiß, dem Troponin I, resultiert. Nur ein einziger Baustein des Troponins, die Aminosäure Arginin (R), ist infolge der Mutation durch einen anderen Baustein, die Aminosäure Glycin (G), ersetzt. Dieser Austausch (cTnI-R145G) erhöht für betroffene Patienten das Risiko von Rhythmusstörungen und dem plötzlichen Herztod. "Bisherige Untersuchungen konzentrierten sich auf die reine Proteinebene oder das gesamte Organ", erklärt Stephanie Reis. "Über die Wirkung in einer einzelnen Herzmuskelzelle war noch nichts bekannt."
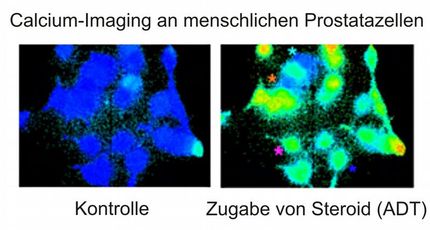
Stephanie Reis analysierte nun die Auswirkungen der Mutation auf die Kontraktion von Herzmuskelzellen und auf die Regulation durch das Stresshormon Adrenalin. Sie zeigte nicht nur, dass diese spezifische Mutation die Kontraktion der Herzzellen, d.h. das Verkürzungsausmaß und die Kinetik des Kontraktionsprozesses, negativ beeinflusst; sie entdeckte auch, für sie selbst überraschend, dass die Adrenalin-vermittelte Regulation der Kontraktion durch das veränderte Troponin beeinflusst wird. Zurzeit nimmt Reis den Kalziumhaushalt der Muskelzellen und die Bindung von Phosphat an das veränderte Troponin unter die Lupe. Von ihren Untersuchungen erhofft sie sich einen Beitrag zum Verständnis, warum einzelne Mutationen bei Patienten mit einer familiären Hypertrophen Kardiomyopathie prognostisch so ungünstig sind.