La resonancia magnética hace visible lo invisible
El agua hiperpolarizada aumenta la intensidad de la señal de las proteínas, el ADN y las membranas
Anuncios
Un pequeño grupo de investigadores, entre los que se encuentra Dennis Kurzbach, de la Facultad de Química de la Universidad de Viena, acaba de publicar en "Nature Protocols" un método avanzado de RMN (Resonancia Magnética Nuclear) para controlar acontecimientos biomoleculares rápidos y complicados, como el plegamiento de proteínas.
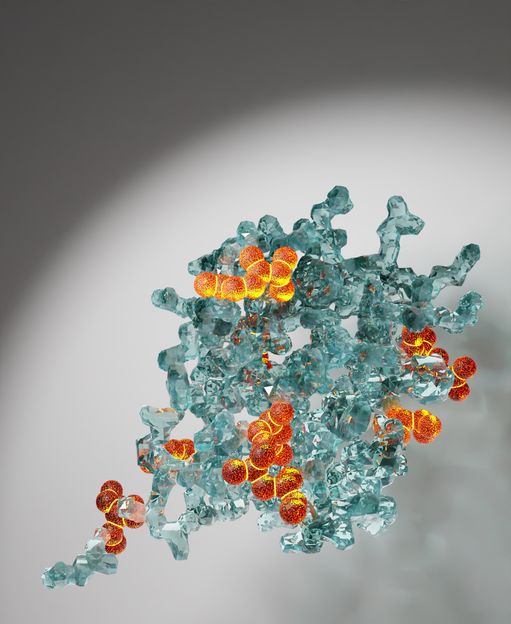
Una visión cristalina de las estructuras de las proteínas: la hiperpolarización hace que los aminoácidos, es decir, los bloques de construcción de las proteínas, se iluminen.
© Mattia Negroni
El plegado de las proteínas, por ejemplo, se consideró durante mucho tiempo uno de los grandes misterios de la investigación moderna. Este proceso crucial, durante el cual las cadenas de aminoácidos adoptan una estructura 3D y una funcionalidad, tiene lugar en milisegundos. Al ser tan rápido, los eventos de plegado de proteínas a menudo no podían ser caracterizados por la espectroscopia de RMN, el método estándar para estudiar las estructuras moleculares. Empleando agua hiperpolarizada, los investigadores han desarrollado ahora un método que mejora drásticamente las señales de las proteínas, los ácidos nucleicos y otras biomoléculas. Esto hace posible el seguimiento de procesos como el plegado de proteínas.
Permitir la RMN en tiempo real
Con la espectroscopia de RMN, los investigadores pueden medir las propiedades magnéticas de los átomos y analizar así la estructura atómica de las moléculas en solución. El método de Dennis Kurzbach y sus colegas Christian Hilty (EE.UU.) y Lucio Frydman (Israel) se basa en la RMN y permite controlar los procesos biológicos en tiempo real. Al utilizar agua hiperpolarizada, los investigadores mejoraron significativamente las señales de RMN de las muestras investigadas y, por tanto, aumentaron la sensibilidad del método.
Con los métodos de hiperpolarización, y más concretamente con la disolución de DNP (D-DNP), es posible un aumento de la señal de más de 10.000 veces. "El agua hiperpolarizada actúa como un potenciador de las señales de RMN de una proteína durante la medición. Los núcleos de hidrógeno del agua hiperpolarizada se intercambian con los de las proteínas, transfiriendo así la fuerza de la señal a estas últimas", afirma Dennis Kurzbach, del Instituto de Química Biológica y subdirector del Centro de RMN de la Facultad de Química.
Con el nuevo método, los investigadores pueden registrar un espectro de RMN cada 100 milisegundos y utilizarlo para rastrear las coordenadas tridimensionales de aminoácidos individuales y cómo cambian con el tiempo. "Esto nos permite controlar procesos que ocurren en milisegundos y distinguir átomos individuales", afirma el químico Dennis Kurzbach, que centra su investigación en el desarrollo de nuevos métodos.
Uso creciente de la RMN para el análisis de proteínas
En su estudio, los autores describen su técnica en detalle, desde la hiperpolarización hasta la transferencia del agua hiperpolarizada al espectrómetro de RMN, pasando por la mezcla del agua hiperpolarizada con la solución de la muestra y la medición de RMN.
Además, presentan seis ejemplos de aplicación del método, incluyendo la observación del plegado de proteínas o incluso las interacciones del ARN (ácidos nucleicos) y las proteínas de unión al ARN como base de las expresiones génicas en la célula. Según los científicos, el nuevo método puede utilizarse para estudios específicos de ARN, ADN y polipéptidos, especialmente cuando el aumento de la señal alcanza el número "mágico" de 1.000 veces.
Un espectrómetro de RMN equipado con un prototipo de hiperpolarización es un requisito previo para la RMN potenciada por agua hiperpolarizada. Sin embargo, este tipo de infraestructura aún no es común. La Facultad de Química de la Universidad de Viena está equipada con un dispositivo DDNP-NMR desde 2020, que ha sido construido por Dennis Kurzbach sobre la base de una subvención de inicio del ERC.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.