RESprotect vergibt Nordamerika-Lizenz für Krebsmedikament an AustCancer
Erster kommerzieller Durchbruch für das Dresdner Unternehmen
Anzeigen
RESprotect GmbH aus Dresden schließt ein Lizenzabkommens mit Australian Cancer Technology ("AustCancer"). Das australische Spezialunternehmen für Krebsbehandlung (Onkologie) erwirbt die Nutzungsrechte für das Krebsmedikament RP101 in Nordamerika. Das Medikament ist der erste kommerzielle Durchbruch des Unternehmens. RESprotect forscht gegenwärtig an vier weiteren Krebspräparaten.
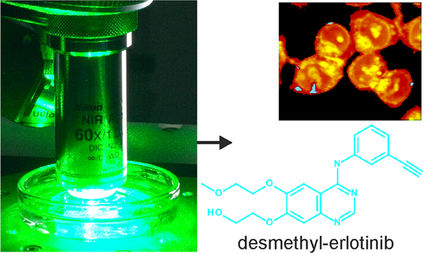
RP101 verhindert Resistenzen der Tumorzellen gegen Chemotherapien. Diese Resistenzen kommen bei längerer Behandlung bei fast allen Patienten vor und sind bislang das größte Problem in der Krebstherapie. Das Medikament wird während der Chemotherapie verabreicht und soll die Überlebenszeit verlängern sowie die Lebensqualität verbessern. In einer klinischen Phase I/II Pilotstudie hat das Medikament Erfolg versprechende Wirkungen gezeigt. AustCancer wird die klinische Prüfung vorantreiben und einen Orphan Drug Status bei der FDA in den USA beantragen.
2003 wurde eine Phase I/II Pilotstudie an sächsischen Kliniken durchgeführte. 30 Patienten, die mit verschiedenen Zytostatika behandelt wurden, erhielten RP 101 in Kobehandlung. Fünf Tumortypen waren eingeschlossen: metastasierter Brust- und Eierstockkrebs, kleinzelliger und nicht kleinzelliger Lungenkrebs sowie metastasierter Pankreas bzw. Bauchspeicheldrüsenkrebs. Die Studie wurde aufgrund auffälliger Befunde auf 13 Pankreaspatienten erweitert. Eine Interimsanalyse dieser Patienten zeigt, dass die Kobehandlung mit RP 101 zu einer deutlich verbesserten Wirkung führt. Nach dieser Analyse erscheint es möglich, die Überlebenszeit, die Remissionen, die Zeit bis zum erneuten Wachstum des Tumors und das Ansprechen auf die Chemotherapie zu erhöhen.
Der Gründer und Hauptanteilseigner von RESprotect, der Genetiker Prof. Dr. Rudolf Fahrig hält "die Resultate der Phase I/II Pilotstudie für sehr aussichtsvoll, insbesondere die Wirkung bei Patienten mit Pankreaskarzinom in der erweiterten Studie." "Die Kobehandlung mit RP 101 führt wahrscheinlich zum Erfolg, weil in Versuchen mit Tumorzellen (in Kultur) das Onkogen STAT3 und das DNA-Reparaturgen APEX - die in Pankreas-Krebszellen überexprimiert sind - herunter reguliert werden."
AustCancers Aufsichtsratvorsitzender, Dr. Roger Aston erklärt: "Obwohl die Zahl der Pankreaspatienten in der Studie sehr klein ist, scheinen die Resultate Erfolg versprechend zu sein. Wir glauben, dass das Arzneimittel die Behandlung von Pankreaskrebs verbessern wird. Dies dürfte zur Erteilung des "Orphan Drug" Status führen, wenn wir in den USA bei der FDA im nächsten Jahr den IND (Investigative New Drug application) einreichen.
Pankreaskrebs steht an fünfter Stelle der Krebserkrankungen, die zum Tod führen. Metastasierte Tumore führen im Schnitt nach 4-6 Monaten zum Tod und die 2-Jahres Überlebenszeit beträgt 10 %. In den USA bzw. Europa erkranken pro Jahr etwa 20.000 Menschen an Pankreaskrebs.
RESprotect kooperiert mit Forschern der Universitäten Leipzig, München, Wien und der TU Dresden. Das Basis-Patent wurde bei der Fraunhofer-Gesellschaft entwickelt, die bei der angewandten Forschung in Europa einen Spitzenplatz besetzt und bei der Prof. Fahrig bis zum Jahr 2000 tätig war.
Prof. Fahrig hat sein Einverständnis erklärt, dem "AustCancer Scientific Advisory Board" beizutreten.