Quantencomputer löst Protein-Puzzle
Interview mit Dr. Sandipan Mohanty vom Jülich Supercomputing Centre
Anzeigen
Der Physiker und Code-Spezialist Dr. Sandipan Mohanty arbeitet seit 20 Jahren an molekularbiologischen Simulationen für die schnellsten Superrechner der Welt. Sie helfen, die Bausteine des Lebens zu entschlüsseln und neue Einblicke in die Zellmaschinerie zu gewinnen. Gemeinsam mit Forschern der schwedischen Universität Lund ist er nun noch einen Schritt weiter gegangen und hat das Problem der Proteinfaltung auf einen Quantencomputer gebracht. Der D-Wave-Quantenannealer JUPSI der Quantencomputer-Infrastruktur JUNIQ am Forschungszentrum Jülich hat mehr als 5000 Qubits und ist das erste Gerät dieser Größe außerhalb Nordamerikas. Im Interview erklärt Mohanty, wie die Pionierarbeit einzuordnen ist.

D-Wave-Quantenannealer JUPSI der Quantencomputer-Infrastruktur JUNIQ am Forschungszentrum Jülich mit mehr als 5000 Qubits
Forschungszentrum Jülich / Sascha Kreklau
Worum ging es bei dieser Aufgabe, die Sie sich vorgenommen haben, Dr. Mohanty?
Ich würde sagen, was wirklich zählt, ist, dass wir die praktische Nutzbarkeit von Quantencomputern für nicht-triviale Forschungsfragen in unserem Feld aufgezeigt haben. Quantencomputer sind ja eine noch recht neuartige Technologie. Es ist noch nicht ganz sicher, wie man sie programmieren muss, um mit ihnen wissenschaftliche Probleme zu lösen. Das ist etwas vollkommen anderes als klassisches High-Performance-Computing (HPC) mit klassischen Superrechnern.
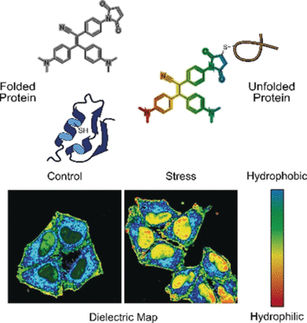
Konkret haben wir die Proteinfaltung anhand eines sehr einfachen Modells untersucht. Proteine sind wichtige Bausteine des Lebens. Sie erfüllen eine breite Palette von Aufgaben. Dazu gehören zum Beispiel der Transport von Stoffen und der Aufbau von Zellen. All diese Funktionen können sie nur erfüllen, wenn sie eine ganz bestimmte Form haben, die sie durch einen Prozess namens Proteinfaltung erreichen. Einer der vielen Gründe für das große Interesse an diesem Prozess ist der Zusammenhang zwischen neurodegenerativen Krankheiten wie Alzheimer oder Parkinson und der Fehlfaltung von Proteinen. Wir hoffen, dass Quantencomputer wichtige Vorteile haben werden, um das Verständnis solcher Phänomene weiter zu verbessern.
Warum ist die Vorhersage der Proteinfaltung so rechenintensiv?
Proteine sind lange, flexible Ketten von Aminosäuren. Eine ihrer faszinierenden Eigenschaften ist, dass sie sich spontan zu ganz bestimmten dreidimensionalen Formen zusammenballen, wenn man sie in eine Lösung gibt, z. B. in Wasser. Im Prinzip muss man also nur die Reihenfolge der Aminosäuren kennen, aus denen eine Proteinkette besteht. Die Kette weiß dann automatisch, in welche Form sie sich falten muss.
Wenn man diesen Faltungsprozess am Computer modelliert, gibt es eine Menge auszuprobieren. Man kann sich das so vorstellen, als würde man versuchen, alle verschiedenen Möglichkeiten zu berechnen, wie man eine Halskette zusammenstellen kann, um die "beste" Anordnung zu finden. Außerdem ist die Untersuchung jeder einzelnen Anordnung sehr rechenintensiv aufgrund der großen Anzahl von Teilchen, die involviert sind. Das macht Millionen von Wechselwirkungen, die berücksichtigt werden müssen.
Wie schneidet der Quantencomputer hier im Vergleich zu einem klassischen Superrechner oder Digitalrechner ab?
Die Aufgabe, die wir gelöst haben, ist von ihrer Komplexität her noch Jahre von den Problemen entfernt, die wir normalerweise mit klassischen Superrechnern lösen. Bei Letzteren geht es üblicherweise um groß angelegte, atomgenaue Simulationen. Auf dem D-Wave-Quantenannealer haben wir dagegen ein sehr reduziertes HP-Modell verwendet. Dieses vereinfacht das Problem massiv, indem es nur die wesentlichen physikalischen Eigenschaften des Faltungsprozesses beibehält. Wir ignorieren dabei das umgebende Medium. Die Aminosäuren werden in nur zwei Typen unterteilt und vereinfacht als Kugeln angesehen, die Positionen in einem Gitter einnehmen.
Entsprechende Simulationen können auch klassisch durchgeführt werden. Dazu reicht ein Notebook aus. Die Zeit für die Berechnung unterscheidet sich nicht wesentlich, in beiden Fällen dauert sie ein bis zwei Minuten. Allerdings ist dieser Wert eigentlich bedeutungslos. Viel wichtiger ist die Qualität der Ergebnisse. Und hier schneidet der Quantenannealer eindeutig besser ab. Es war relativ einfach, auf JUPSI eine Erfolgsrate von 100 Prozent beim Auffinden der Strukturen mit der niedrigsten Energie zu erreichen. Mit klassischen Computern hingegen kommen vergleichbare Simulationen für eine Kette aus 30 Aminosäuren nur auf 80 Prozent. Bei den komplexeren Proteinen, die aus 48 oder 64 Aminosäureblöcken bestehen, schneiden sie sogar noch deutlich schlechter ab. Der Quantenannealer lieferte auch hier immer das richtige Ergebnis.
Warum ist der Quantencomputer hier genauer als ein klassischer Rechner?
Weil er von bestimmten Aspekten dieser wissenschaftlichen Aufgabe profitiert. Der Rechenaufwand, um alle Protein-Konformationen auf einem klassischen Computer zu berücksichtigen, ist astronomisch hoch. Er wächst exponentiell mit der Länge der Proteinkette. Bei einer Kette aus zwei Teilchen gibt es vielleicht zehn Möglichkeiten. Bei drei Teilchen sind es schon hundert. Aber bei 100 Teilchen – was für ein Protein immer noch recht wenig ist – müsste man milliardenfach mehr Variationen berechnen, als es Atome im Universum gibt.
Um überhaupt eine sinnvolle Berechnung durchführen zu können, werden viele Tricks angewandt. Unsere Gruppe am Jülich Supercomputing Centre und meine Partner in Schweden haben sich dazu auf sogenannte Monte-Carlo-Simulationen spezialisiert. Das Verfahren basiert auf statistischer Physik und stochastischen Stichproben. Obwohl unendlich lange Simulationen garantiert korrekte Lösungen ergeben, können kurze Durchläufe große Fehler aufweisen. In der Praxis versucht man daher, die Simulationen "lange genug" durchzuführen, damit die geschätzten Fehler akzeptabel klein sind.
Hier liegt der Vorteil des Quantenannealers. Diese Maschine kann, wenn sie richtig programmiert ist, diese Annäherung auf sehr direkte Weise über ihre quantenmechanischen Kopplungen durchführen. Im Grunde handelt es sich um eine Art kompliziertes physikalisches Experiment, das die Gleichung automatisch löst. Bei unserem Problem führte dies anscheinend dazu, dass vergleichsweise kurze Laufzeiten benötigt werden, um sehr gute Antworten zu erhalten. Die Tatsache, dass es in der Praxis so gut funktioniert, hat uns tatsächlich etwas überrascht.
Welche perspektivischen Anwendungsmöglichkeiten ergeben sich damit jetzt für Quantencomputer?
Unsere Arbeit ist nur ein erster Schritt. Die meisten der heutigen Quantencomputer haben nur einige wenige Qubits. Das D-Wave-System hat bereits 5000, was eine Menge ist. Aber für die meisten interessanten Forschungsprobleme benötigt man noch mehr Qubits. Von Simulationen, wie sie in der Arzneimittelforschung auf Supercomputern durchgeführt werden, sind wir noch weit entfernt. Ich gehe davon aus, dass wir noch zwei oder drei Geräte-Generationen abwarten müssen, bevor wir solche Probleme mit einem Quantencomputer lösen können.
Aber ich bin hier hoffnungsvoll. Im Gegensatz zu bisherigen Forschungsarbeiten, von denen wir lernen konnten, behält unsere Formulierung ihre Einfachheit bei zunehmender Systemgröße bei. Dies eröffnet einen möglicherweise einfacheren Weg, um auch wesentlich komplexere Probleme auf Quantencomputern zu untersuchen.