Neues Puzzlestück gefunden: Wie regelt UHRF1 die Gen-Aktivität?
Anzeigen
Epigenetische Veränderungen spielen bei Krebserkrankungen oft eine wichtige Rolle, weil dadurch das Erbgut punktuell falsch abgelesen wird. Besonders kritisch sind Gene, die das Wachstum und den Tod von Zellen steuern können. Wissenschaftler des Helmholtz Zentrums München haben in diesem Zusammenhang neue Details über das Protein UHRF1 herausgefunden. Es katalysiert Teilschritte der epigenetischen Stummschaltung weiter Teile des Genoms. Wie sie in ‚Molecular Cell‘ berichten, könnte sich das Molekül als Zielstruktur für medikamentöse Therapien eignen, da es in Krebszellen in erhöhtem Maße produziert wird.
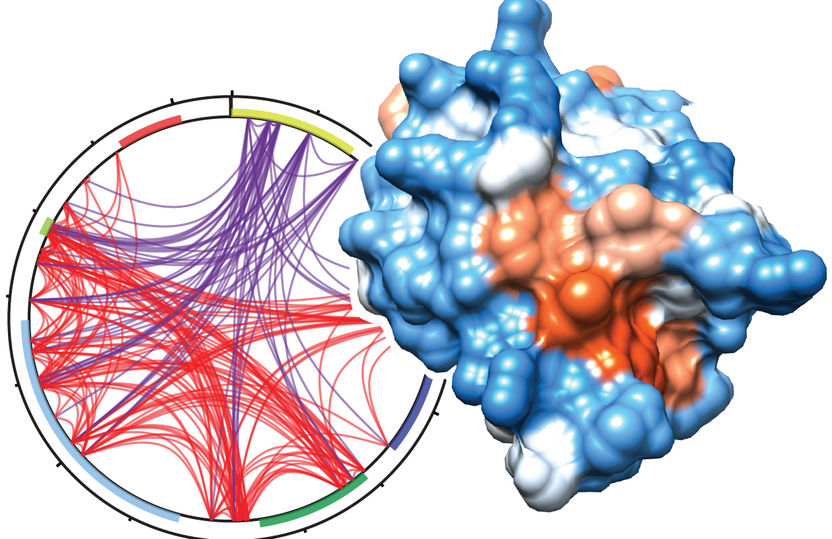
UHRF1 könnte sich als Zielstruktur für medikamentöse Therapien eignen.
© Helmholtz Zentrum München
Alle Zellen unseres Körpers haben das gleiche Erbgut, übernehmen aber unterschiedliche Aufgaben, da die Gene in den verschiedenen Zelltypen unterschiedlich abgelesen werden. Diese Steuerung der Gen-Aktivität findet nicht nur auf Ebene der DNA-Sequenz statt. Eine Vielzahl chemischer Modifizierungen der DNA und der Histone steuert die Aktivität von Genen auf der epigenetischen Ebene. „Histone sind Proteine, die die DNA-Fäden im Zellkern zu den Chromosomen ‚verpacken’. Sie sind aber auch für die Genexpression von Bedeutung“, sagt Prof. Dr. Robert Schneider, Direktor des Instituts für Funktionelle Epigenetik (IFE) des Helmholtz Zentrums München. Zusammen mit anderen Proteinen bilden DNA-Moleküle und Histone das Chromatin: eine chemische Möglichkeit, Erbinformationen auf geringem Volumen im Zellkern zu verpacken. Diese Regulierungsvorgänge, über die noch recht wenig bekannt ist, bilden die Grundlage der Forschung am IFE.
UHRF1: Ein Molekül steuert Schlüsselschritte bei der DNA-Methylierung
Bisher war bekannt, dass das Protein UHRF1 (Ubiquitin-like, containing PHD and RING finger domains) eine wichtige Rolle bei der Methylierung von DNA spielt. Methylierungen sind chemische Modifikationen am DNA-Molekül ohne Veränderung des genetischen Codes, sprich der Basenabfolge. Sie haben aber Auswirkungen auf die Aktivität der in der Basensequenz codierten Gene. Für gewöhnlich sorgt die Methylierung von DNA-Molekülen für deren Stummschaltung.
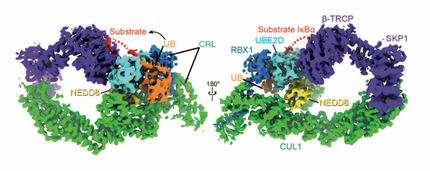
UHRF1 steuert die DNA-Methylierung, indem es dafür sorgt, dass ein Enzym, welches Methyl-Gruppen an die DNA knüpft, an neu entstandenes Chromatin bindet. Um diese Aufgabe zu erfüllen, muss UHRF1 zuerst selbst an das neu entstandene Chromatin andocken und im nächsten Schritt ein Ubiquitin-Molekül (ein kleines Protein, das die Eigenschaften anderer Proteine verändert) auf ein Histon-Protein übertragen. Hierfür verwendet UHRF1 unterschiedliche Protein-Domänen, Bereiche mit besonderen Raumstrukturen und Aufgaben im gleichen Molekül.
„Wie das genau funktioniert, war bislang nicht bekannt“, sagt Dr. Till Bartke, stellvertretender Direktor des IFE und Leiter der Studie. Zusammen mit seinem Kollegen Dr. Benjamin Foster (Wissenschaftlicher Mitarbeiter am IFE) hat er verschiedene Verfahren eingesetzt, um diesen Teilschritt zu erforschen. „Wir konnten zeigen, dass eine Ubiquitin-ähnliche Domäne (UBL) vorhanden sein muss, um Ubiquitin-Moleküle zu übertragen“, fasst Bartke zusammen: Ein besonderes Strukturelement, welches an Umlagerungen von UHRF1 beteiligt ist, nachdem es an das Chromatin angedockt hat. In Zusammenarbeit mit der Gruppe von Dr. Sebastian Bultmann an der Ludwig-Maximilians Universität München konnten die Forscher zudem zeigen, dass die UBL-Domäne notwendig ist, damit DNA in Zellen methyliert wird.
„Unsere Analyse des enzymatischen Mechanismus von UHRF1 zeigt eine unerwartete Funktion der UBL-Domäne auf und definiert eine neue Rolle für diese Domäne bei der DNA-Methylierung“, fasst der Wissenschaftler zusammen. Da andere Gruppen bei mehreren Tumoren, etwa Lungen- und Darmkrebs, erhöhte Mengen an UHRF1 gefunden hätten, sei das Protein eine denkbare Zielstruktur für künftige Therapien.