La découverte d'une nouvelle vulnérabilité dans le lymphome agressif pourrait modifier la thérapie future
Annonces
Des chercheurs ont découvert qu'une protéine clé, la cFLIP, est essentielle à la régulation de la mort cellulaire programmée dans les cellules de lymphome. Cette découverte permet de mieux comprendre les mécanismes d'évasion de la mort cellulaire de ce cancer et pourrait ouvrir de nouvelles voies thérapeutiques pour les patients qui ne répondent pas aux traitements / publication dans "Blood"
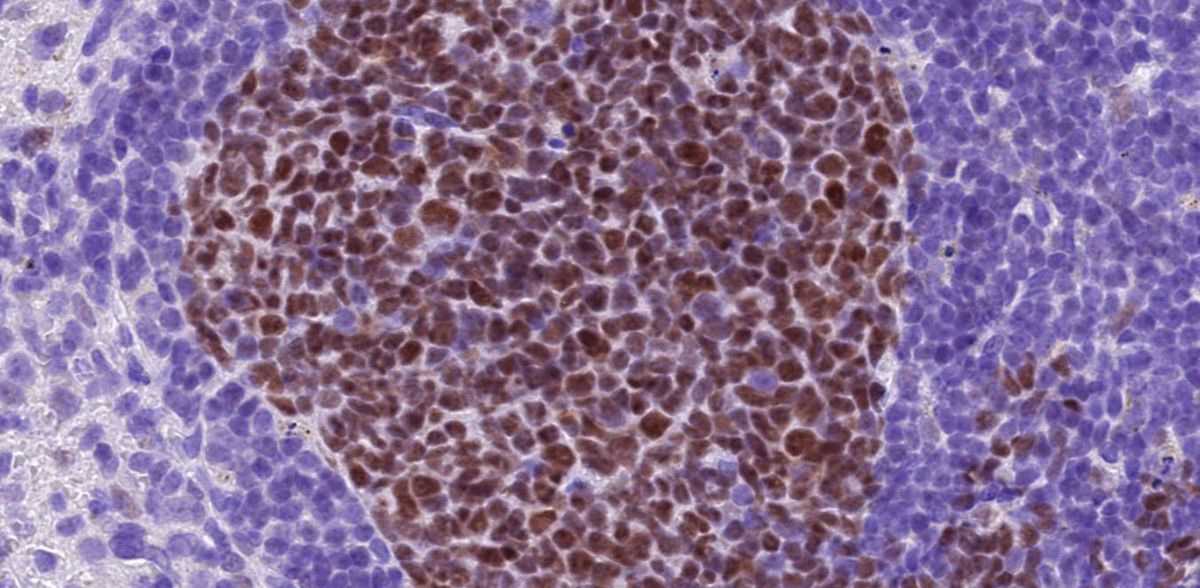
Une équipe de chercheurs du Centre de médecine moléculaire de l'Université de Cologne (CMMC) a découvert que la protéine cFLIP peut être utilisée pour contourner les défenses du lymphome diffus à grandes cellules B (DLBCL) contre la mort cellulaire programmée. Ces défenses rendent souvent les traitements inefficaces car elles permettent aux cellules cancéreuses de survivre. Les résultats sont particulièrement pertinents pour le DLBCL ABC, un sous-type spécifique de cancer du sang dont le pronostic et la survie sont médiocres. La nouvelle étude a été publiée sous le titre "Expression of cFLIP in B cells is essential for diffuse large B cell lymphoma pathogenesis" dans la revue Blood.
Le DLBCL est le type le plus courant de lymphome non hodgkinien, un cancer qui se développe à partir de globules blancs appelés lymphocytes. L'immunochimiothérapie de première ligne actuelle, qui associe l'anticorps rituximab à des agents de chimiothérapie, permet de guérir environ 60 % des patients. Malgré cette avancée majeure, environ 50 % des patients traités rechutent ou ne répondent pas au traitement, ce qui rend toute nouvelle tentative de thérapie risquée et difficile.
Il est donc urgent de trouver des thérapies alternatives en déterminant les vulnérabilités des cellules DLBCL. L'identification de ces vulnérabilités est compliquée par le fait que le DLBCL est très hétérogène et que les cellules DLBCL échappent à la mort cellulaire programmée (apoptose) en surexprimant un facteur anti-apoptose appelé BCL2. Ce faisant, ces cellules lymphomateuses acquièrent un avantage de survie qui leur permet de proliférer indéfiniment et de former des tumeurs, avec des conséquences néfastes pour la santé et la survie des patients. Il est donc essentiel de comprendre les mécanismes qui contrôlent la mort cellulaire dans les cellules de lymphome et de trouver des moyens de surmonter le blocage de l'apoptose imposé par la surexpression de la protéine BCL2 pour réactiver la mort cellulaire.
La protéine BCL2 contrôle étroitement l'une des voies de mort cellulaire appelée apoptose intrinsèque. Cependant, les cellules peuvent également mourir par une autre voie appelée apoptose extrinsèque, qui est étroitement contrôlée par la protéine cFLIP. L'équipe de recherche dirigée par le Dr Alessandro Annibaldi au CMMC a découvert qu'en plus de BLC2, les cellules DLBCL surexpriment également cFLIP. Ce faisant, elles sont capables de bloquer le bras apoptotique intrinsèque et extrinsèque et deviennent très résistantes à la mort.
"Les cellules DLBCL construisent des barrages pour interrompre les voies intrinsèques et extrinsèques de la mort cellulaire afin d'essayer d'atteindre l'immortalité et d'obtenir un avantage de survie par rapport aux cellules normales. Notre objectif était d'identifier puis de supprimer le barrage sur la voie extrinsèque de l'apoptose, afin de reprogrammer le destin de ces cellules et de les pousser à emprunter la voie qui mène finalement à leur mort. L'existence d'un tel obstacle est une hypothèse émise depuis de nombreuses années, mais notre groupe a été le premier à le découvrir et à comprendre sa pertinence clinique", déclare Alessandro Annibaldi.
Le groupe de recherche a utilisé des techniques de pointe en biologie cellulaire et moléculaire, ainsi qu'un modèle préclinique de souris pour le DLBCL. Ils ont découvert que le ciblage de la cFLIP pouvait contourner le blocage de l'apoptose médié par la surexpression de BCL2 et réactiver la mort cellulaire dans les cellules lymphomateuses. Leur étude révèle que cFLIP est surexprimé spécifiquement dans le sous-type ABC-DLBCL et que sa suppression génétique empêche le développement du lymphome en sensibilisant à nouveau les cellules lymphomateuses aux signaux de mort.
Ce résultat de recherche apporte la preuve de principe que la voie extrinsèque de l'apoptose peut être exploitée pour briser la résistance des cellules DLBCL à l'apoptose induite par la surexpression de BCL2 et le blocage de l'apoptose intrinsèque. Cette étude justifie donc le développement de médicaments ciblant cFLIP. Ces médicaments, seuls ou en combinaison avec d'autres, seraient capables de tuer les cellules ABC-DLBCL, quelles que soient les mutations qu'elles portent, tant qu'elles expriment la cFLIP.
Les chercheurs sont convaincus que le développement de molécules inhibitrices spécifiques de cFLIP et leur validation dans des modèles précliniques de DLBCL permettront de mieux comprendre le potentiel translationnel de cette découverte. "Cibler cFLIP en combinaison avec les thérapies existantes représente une option viable qui mérite d'être explorée pour les patients qui ne répondent pas au traitement standard de la DLBCL", déclare Kristie Bariboloka, la chercheuse doctorante qui a dirigé les travaux de recherche au laboratoire.
Ces travaux ont été menés dans le cadre du Centre de recherche collaborative (CRC) 1530 "Elucidation et ciblage des mécanismes pathogènes dans les tumeurs malignes à cellules B", financé par la Fondation allemande de la recherche (DFG). Le soutien important du CRC et des groupes de recherche associés a été décisif pour la réalisation de ce travail.
Note: Cet article a été traduit à l'aide d'un système informatique sans intervention humaine. LUMITOS propose ces traductions automatiques pour présenter un plus large éventail d'actualités. Comme cet article a été traduit avec traduction automatique, il est possible qu'il contienne des erreurs de vocabulaire, de syntaxe ou de grammaire. L'article original dans Anglais peut être trouvé ici.