El descubrimiento de una nueva vulnerabilidad en el linfoma agresivo podría cambiar la terapia futura
Anuncios
Unos investigadores han descubierto que una proteína clave, cFLIP, es esencial para regular la muerte celular programada en células de linfoma. Este descubrimiento permite comprender mejor los mecanismos de evasión de la muerte celular de este cáncer y podría abrir nuevas vías terapéuticas para los pacientes que no responden a las terapias / publicación en "Blood"
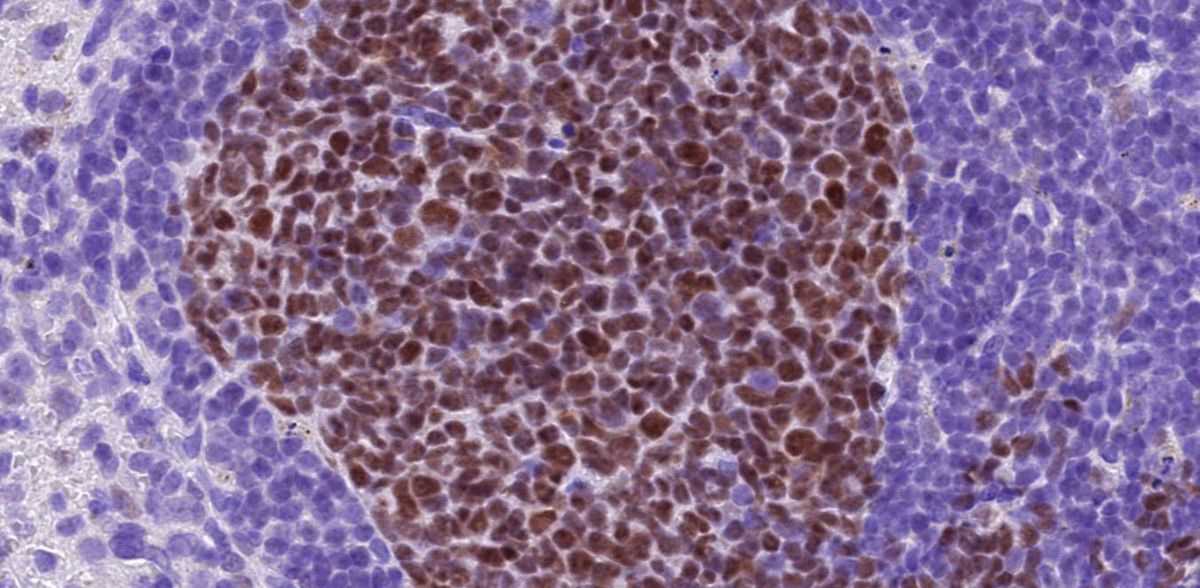
Un equipo de investigadores del Centro de Medicina Molecular de Colonia (CMMC) de la Universidad de Colonia ha descubierto que la proteína cFLIP puede utilizarse para anular las defensas del linfoma difuso de células B grandes (DLBCL) contra la muerte celular programada. Estas defensas suelen ser la causa de la ineficacia de los tratamientos, ya que permiten la supervivencia de las células cancerosas. Los resultados son especialmente relevantes para el linfoma difuso de células B grandes ABC-DLBCL, un subtipo específico de cáncer de la sangre con mal pronóstico y supervivencia. El nuevo estudio ha aparecido bajo el título "Expression of cFLIP in B cells is essential for diffuse large B cell lymphoma pathogenesis" en la revista Blood.
El linfoma difuso de células B grandes es el tipo más frecuente de linfoma no hodgkiniano, un cáncer que se desarrolla a partir de unos glóbulos blancos llamados linfocitos. La inmunoquimioterapia de primera línea actual, que combina el anticuerpo rituximab con agentes quimioterápicos, cura aproximadamente al 60% de los pacientes. A pesar de este importante logro, aproximadamente el 50 por ciento de los pacientes tratados recaen o no responden al tratamiento, lo que hace que los nuevos intentos terapéuticos sean arriesgados y supongan un reto.
Esto crea una necesidad urgente de encontrar terapias alternativas mediante la determinación de vulnerabilidades en las células DLBCL. Encontrar dichas vulnerabilidades se complica por el hecho de que la LDCB es muy heterogénea y las células de LDCB eluden la muerte celular programada (apoptosis) sobreexpresando un factor antiapoptosis denominado BCL2. Al hacerlo, estas células de linfoma obtienen una ventaja de supervivencia que les permite proliferar indefinidamente y formar tumores, con consecuencias perjudiciales para la salud y la supervivencia de los pacientes. Por lo tanto, es fundamental comprender los mecanismos que controlan la muerte celular en las células de linfoma y encontrar formas de superar el bloqueo de la apoptosis impuesto por la sobreexpresión de BCL2 para reactivar la muerte celular.
La proteína BCL2 controla estrechamente una rama de las vías de muerte celular denominada apoptosis intrínseca. Sin embargo, las células también pueden morir por otra vía llamada apoptosis extrínseca, que está estrechamente controlada por la proteína cFLIP. El equipo de investigación dirigido por el Dr. Alessandro Annibaldi en el CMMC descubrió que, además de BLC2, las células DLBCL también sobreexpresan cFLIP. Al hacerlo, son capaces de bloquear tanto el brazo apoptótico intrínseco como el extrínseco y se vuelven muy resistentes a la muerte.
"Las células DLBCL construyen barricadas para interrumpir las vías de muerte celular intrínseca y extrínseca para intentar alcanzar la inmortalidad y obtener una ventaja de supervivencia sobre las células normales. Nuestro objetivo era identificar y eliminar el bloqueo de la vía extrínseca de la apoptosis para reprogramar el destino de estas células y empujarlas a recorrer la vía que finalmente las conduce a la muerte. La existencia de esta barricada es una hipótesis desde hace muchos años, pero nuestro grupo ha sido el primero en encontrarla y comprender su importancia clínica", afirma Alessandro Annibaldi.
El grupo de investigación empleó técnicas celulares y de biología molecular de última generación, así como un modelo preclínico de ratón para el DLBCL. Descubrieron que la acción sobre cFLIP podía anular el bloqueo de la apoptosis mediado por la sobreexpresión de BCL2 y reactivar la muerte celular en células de linfoma. Su estudio revela que cFLIP se sobreexpresa específicamente en el subtipo ABC-DLBCL, y que su deleción genética previene el desarrollo del linfoma al resensibilizar las células del linfoma a las señales de muerte.
Este hallazgo de la investigación proporciona la prueba de principio de que la vía extrínseca de la apoptosis puede explotarse para romper la resistencia de las células DLBCL a la apoptosis impulsada por la sobreexpresión de BCL2 y el bloqueo intrínseco de la apoptosis. Así pues, este estudio justifica el desarrollo de fármacos dirigidos contra cFLIP. Tales fármacos, solos o en combinación con otros, serían capaces de destruir las células ABC-DLBCL, independientemente de las mutaciones que presenten, siempre que expresen cFLIP.
De cara al futuro, los investigadores confían en que el desarrollo de moléculas inhibidoras específicas de cFLIP y su validación en modelos preclínicos de DLBCL proporcionen más información sobre el potencial traslacional de este descubrimiento. "Dirigirse a cFLIP en combinación con las terapias existentes representa una opción viable que merece la pena explorar para los pacientes que no responden al tratamiento estándar del DLBCL", afirma Kristie Bariboloka, la investigadora doctoral que encabezó el trabajo de investigación en el laboratorio.
Este trabajo se llevó a cabo en el contexto del Centro de Investigación en Colaboración (CRC) 1530 "Elucidación y orientación de mecanismos patogénicos en neoplasias de células B", financiado por la Fundación Alemana para la Investigación (DFG). El amplio apoyo del CRC y de los grupos de investigación asociados fue decisivo para la realización de este trabajo.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.