Cómo los patógenos pasan a ser "peligrosos
Anuncios
Durante una infección, los patógenos se adaptan rápidamente a las condiciones del organismo para sobrevivir. Un equipo de investigadores de la Universidad de Basilea ha descubierto cómo una proteína activa en el patógeno Leptospira la maquinaria que le ayuda a sobrevivir en el organismo y provocar la enfermedad. El trabajo aporta datos hasta ahora desconocidos sobre la forma en que los patógenos controlan su virulencia y abre nuevos puntos de partida para terapias.
Desde finales del siglo pasado, las enfermedades que pasan de los animales a los humanos, conocidas como zoonosis, han ido en aumento. La leptospirosis es una zoonosis cada vez más frecuente como consecuencia del cambio climático. Cada año provoca en todo el mundo alrededor de un millón de casos graves de la enfermedad, con un número estimado de 60.000 muertos. Esta enfermedad es un grave problema sanitario, sobre todo en zonas con escasos recursos, pero también se dan casos en Suiza.
La leptospirosis está causada por la bacteria Leptospira. Las personas se infectan principalmente a través del agua y el suelo contaminados. Si la infección no se trata a tiempo con antibióticos, puede provocar un fallo orgánico potencialmente mortal. Cuando entra en el organismo, el patógeno activa los llamados factores de virulencia para sobrevivir. Esto está controlado por la proteína LvrB: sólo cuando está activa, la bacteria puede desarrollar su potencial patógeno.

Imagen del símbolo
AI-generated image
De inactiva a activa
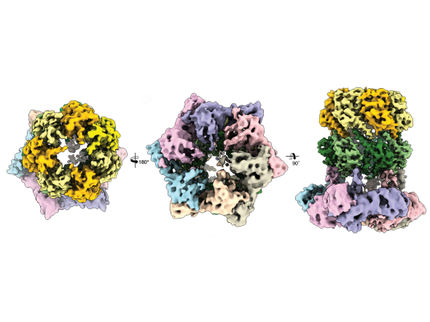
Hasta ahora no se sabía exactamente cómo se activa la LvrB. En un estudio publicado recientemente en "Nature Communications", el equipo dirigido por el profesor Sebastian Hiller, del Biozentrum de la Universidad de Basilea, ha logrado dilucidar la estructura tridimensional de la proteína y su modo de acción exacto.
"Ahora entendemos a nivel atómico cómo funciona este interruptor molecular, es decir, cómo se activa. Y lo que es más importante, hemos descubierto un mecanismo de activación general que afecta a un gran número de otras proteínas bacterianas", afirma Hiller. "Nuestros hallazgos también son importantes para el desarrollo de sustancias activas. Si logramos desactivar permanentemente la LvrB, podríamos impedir que el patógeno se vuelva virulento, es decir, peligroso, en el organismo."
Bloqueado e inactivo
LvrB forma parte de un sistema de comunicación que regula la actividad de cientos de genes relacionados con la virulencia del patógeno, es decir, su capacidad para causar enfermedades. "En estado desactivado, LvrB se fija en una forma simétrica y, por tanto, inactiva, en la que no puede activar factores de virulencia", explica Elia Agustoni, primera autora del estudio. "Esta posición off impide que el patógeno produzca factores de virulencia innecesariamente, es decir, cuando está fuera del organismo".
Activo y "peligroso"
Las señales del huésped desencadenan una reacción en cadena, como resultado de la cual LvrB se modifica químicamente. Esto, a su vez, conduce a reordenamientos de la estructura de la proteína. "LvrB cambia su forma, se rompe la simetría, lo que prácticamente activa la proteína", explica Agustoni. "En estado 'activado', LvrB transmite la señal a su proteína asociada, que los investigadores también pudieron identificar. Juntas activan genes de virulencia que permiten a la Leptospira multiplicarse y propagarse por el organismo".
Importancia para otras enfermedades infecciosas
Los agentes que mantienen LvrB o proteínas relacionadas en forma inactiva son presumiblemente un enfoque prometedor para atenuar la virulencia de los patógenos y prevenir las infecciones. Esto también podría reducir el riesgo de resistencia a los antibióticos.
Los descubrimientos sobre la activación de LvrB van mucho más allá de la comprensión de la leptospirosis. Este mecanismo afecta a un gran número de sistemas de señalización similares en bacterias, incluidos numerosos patógenos que infectan a humanos, animales y plantas. "A partir de nuestros resultados, ahora se podrán investigar muchos procesos celulares desconocidos hasta ahora", subraya Hiller. "También servirán para desarrollar nuevos antibióticos y productos agroquímicos, como los pesticidas".
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Alemán se puede encontrar aquí.
Publicación original
Elia Agustoni, Ariel Mechaly, Joaquín Dalla Rizza, David Beriashvili, Kristyna Pluhackova, Polina Isaikina, Felipe Trajtenberg, Thomas Müntener, Elsio A. Wunder, Albert I. Ko, Tilman Schirmer, Alejandro Buschiazzo, Sebastian Hiller; "Activation mechanism of the full-length histidine kinase LvrB from pathogenic Leptospira"; Nature Communications, 2026-4-16
Anuncios