Cómo las células reescriben su destino
El estudio podría ser el punto de partida de nuevos métodos para alterar los mecanismos moleculares del desarrollo del cáncer
Anuncios
Un equipo internacional de investigadores, entre los que se encuentra Achim Leutz, del Centro Max Delbrück, ha descubierto que una proteína específica controla la conversión de las células inmunitarias. Si fuera posible intervenir en este proceso, podría prevenirse el desarrollo del cáncer.
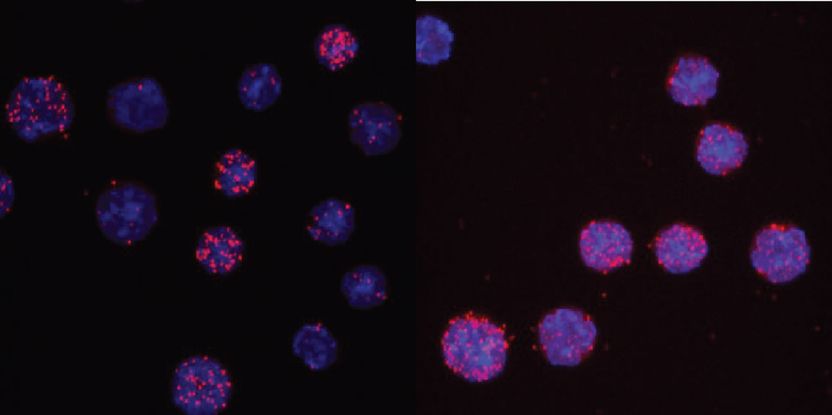
C/EBPαR35A interactúa más fuertemente con PU.1 que C/EBPα no apareado. Las imágenes muestran los núcleos de las células en azul claro y la lectura de la interacción como puntos rojos. Para el tipo salvaje sólo 3 de 13 células muestran señales, mientras que para el mutante 7 de 8 células son positivas.
Thomas Graf, Centre for Genomic Regulation
El destino celular determina en qué tipo celular se diferencia una célula y qué función asume en el organismo. Si las células toman una decisión equivocada en este proceso, puede desarrollarse un cáncer.
Investigadores del Centro de Regulación Genómica (CRG) de Barcelona y del Centro Max Delbrück de Berlín han investigado cómo las células pueden acelerar su destino. Presentan sus resultados en la revista científica "eLife". El estudio podría ser el punto de partida de nuevos métodos para alterar los mecanismos moleculares del desarrollo del cáncer.
Soltar la correa a los fagocitos
Un elemento central del estudio es C/EBPα (CCAAT/enhancer-binding protein alpha), una proteína que orquesta la conversión de linfocitos B en macrófagos. Los linfocitos B son glóbulos blancos que forman anticuerpos contra agentes patógenos. Los macrófagos también pertenecen a los glóbulos blancos. Denominados "células carroñeras", encuentran y eliminan patógenos y células patológicamente alteradas. C/EBPα es un factor de transcripción, un tipo de proteína que se une a secuencias específicas de ADN en las regiones reguladoras de los genes, donde activa o reprime la expresión de proteínas.
Como todas las proteínas, C/EBPα está formada por diferentes aminoácidos. Las enzimas pueden modificar las proteínas uniendo varios grupos metilo -que son pequeñas "pegatinas" formadas cada una por un átomo de carbono y tres de hidrógeno- a determinados aminoácidos. Este proceso se denomina metilación. De este modo, pueden influir notablemente en las interacciones entre proteínas. Los investigadores descubrieron que cuando un residuo de aminoácido específico de C/EBPα se deja sin metilar, acelera enormemente el proceso de conversión de linfocitos B en macrófagos. La metilación de este residuo de aminoácido específico está mediada por la enzima Carm1. Investigaciones anteriores han demostrado que los ratones deficientes en Carm1 son resistentes a las formas inducidas de leucemia mieloide aguda. Esto podría deberse a los mecanismos revelados por los investigadores en su estudio: la versión no metilada de C/EBPα es un inductor más potente de la diferenciación de los macrófagos en comparación con su homóloga metilada. Como los macrófagos son un tipo de célula que no se divide, esto podría impedir la formación de células cancerosas.
Nuevas ideas para tratar la leucemia
"Al comprender cómo se puede acelerar o dirigir la conversión del destino celular, descubrimos nuevas pistas para la investigación del cáncer", afirma el Dr. Thomas Graf, autor principal del CRG. "Por ejemplo, dirigir el equilibrio entre las formas metiladas y no metiladas de C/EBPα puede ayudarnos a comprender cómo se diferencian las células inmunitarias y, con el tiempo, dar lugar a nuevas ideas para tratar ciertas formas de leucemia."
La localización del aminoácido crítico dentro de C/EBPα se descubrió cuando los investigadores probaron una forma mutante de la proteína denominada C/EBPαR35A. Este mutante aceleraba drásticamente la velocidad a la que las células B podían convertirse en macrófagos. Para inducir una conversión celular, C/EBPα actúa interactuando con otro factor de transcripción denominado PU.1. Se descubrió que C/EBPαR35A interactuaba mucho más fuertemente con PU.1 que C/EBPα. Esto silenció más rápidamente los genes de las células B y activó en su lugar los genes de los macrófagos.
Fármacos contra las células "confundidas
La metilación de C/EBPα es un ejemplo de mecanismo epigenético. Se trata de mecanismos que modifican cómo se lee el genoma, el manual de instrucciones dentro de cada célula del cuerpo humano. "Los fármacos que afectan a los mecanismos epigenéticos pueden, en efecto, alterar la función de los factores de transcripción y corregir células descarriadas, como ocurre en el cáncer y la leucemia", afirma el Dr. Achim Leutz, autor principal y jefe del grupo de investigación "Diferenciación celular y tumorigénesis" del Centro Max Delbrück. "En este novedoso mecanismo, PU.1 es activado por C/EBPα para pasar de regulador de células B a regulador de macrófagos, un elegante mecanismo de 'encendido-apagado' que garantiza la formación fiel de un tipo celular maduro, evitando la formación de células 'confusas' que se observa con frecuencia en los cánceres de la sangre. Por tanto, podrían encontrarse fármacos dirigidos a este mecanismo para corregir tales defectos".
Aún se desconoce mucho sobre lo que determina la velocidad y direccionalidad de las decisiones sobre el destino celular. El trabajo sugiere que ambos procesos son dos caras de la misma moneda. Por ejemplo, ¿cómo se transforman secuencialmente las células madre en los distintos tipos de células del organismo? Entender mejor cómo cambian de identidad las células y cómo manipular el proceso podría tener aplicaciones que van desde la medicina regenerativa hasta la mejora de la eficacia de los fármacos contra el cáncer.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.