Cómo se forma espontáneamente la urea
Descubierta una nueva reacción: potencial para la síntesis de urea sostenible y de bajo consumo energético
La urea se considera una posible molécula clave en el origen de la vida. Investigadores de la ETH han descubierto una forma desconocida hasta ahora por la que este componente básico puede formarse espontáneamente en superficies acuosas sin necesidad de energía adicional.
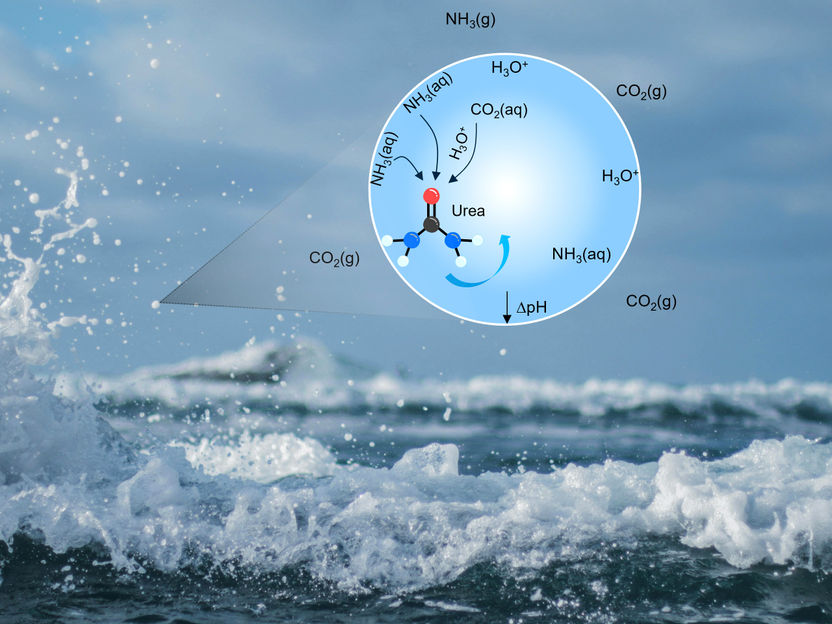
Representación gráfica de la formación de urea en una gota
Luis Quintero / ETH Zürich
La urea es uno de los productos químicos industriales más importantes del mundo. Se utiliza como fertilizante, para la producción de resinas sintéticas y explosivos y como aditivo para limpiar los gases de escape de los automóviles. También se cree que la urea es un posible elemento clave para la formación de moléculas biológicas como el ARN y el ADN, en relación con la cuestión del origen de la vida. Hasta ahora, el origen de la propia urea en la Tierra primitiva no se había aclarado de forma concluyente.
Un equipo de investigación dirigido por Ruth Signorell, catedrática de Química Física de la ETH de Zúrich, ha descubierto una vía de reacción hasta ahora desconocida para la formación de la urea que podría aportar una respuesta. El estudio acaba de publicarse en la revista Science.
Química en la superficie del agua
Para la producción industrial de urea a partir de amoníaco (NH₃) y dióxido de carbono (CO₂) se necesitan altas presiones y temperaturas o catalizadores químicos. Las enzimas permiten que se produzca la misma reacción en humanos y animales, eliminando el amoníaco tóxico procedente de la descomposición de proteínas como la urea. Dado que esta sencilla molécula contiene nitrógeno además de carbono y probablemente existía en la deshabitada Tierra primitiva, muchos investigadores ven la urea como un posible precursor de biomoléculas complejas.
"En nuestro estudio, mostramos una forma en la que la urea podría haberse formado en la Tierra prebiótica", afirma Signorell, "concretamente allí donde las moléculas de agua interactúan con los gases atmosféricos: en la superficie del agua".
Reactor en el borde de una gota
El equipo de Signorell estudió gotitas de agua diminutas como las que se encuentran en el rocío marino y la niebla fina. Los investigadores observaron que la urea puede formarse espontáneamente a partir de dióxido de carbono (CO₂) y amoníaco (NH₃) en la capa superficial de las gotitas en condiciones ambientales. La interfaz física entre el aire y el líquido crea un entorno químico especial en la superficie del agua que hace posible la reacción espontánea.
Como una gotita tiene una superficie muy grande en relación con su volumen, las reacciones químicas tienen lugar principalmente cerca de esta superficie. En esta zona se forman gradientes de concentración química que actúan como un reactor microscópico. El gradiente de pH a través de la capa interfacial de las gotas de agua crea el entorno ácido necesario, que abre vías no convencionales que de otro modo no tendrían lugar en los líquidos.
"Lo más destacable de esta reacción es que se produce en condiciones ambientales y sin energía externa", explica Mercede Mohajer Azizbaig, una de las dos primeras autoras. Esto no sólo hace que el proceso sea interesante desde el punto de vista técnico, sino que también aporta valiosos conocimientos sobre procesos que podrían ser importantes para la evolución".
Una ventana a los inicios de la Tierra
El origen de la vida es actualmente objeto de una amplia investigación, con diferentes enfoques que se están explorando. El primer autor, Pallab Basuri, explica: "Dado un campo de investigación tan controvertido, era importante para nosotros respaldar nuestras observaciones". Los cálculos teóricos de los coautores Evangelos Miliordos y Andrei Evdokimov, de la Universidad de Auburn, respaldaron los hallazgos experimentales y confirmaron que la reacción de la urea en las gotitas tiene lugar sin ningún suministro externo de energía.
Los resultados sugieren que esta reacción natural también podría haber sido posible en la atmósfera de la Tierra primitiva, una atmósfera rica en CO₂ y que probablemente contenía pequeñas trazas de amoníaco. En tales entornos, los aerosoles acuosos o las gotas de niebla podrían haber actuado como reactores naturales en los que se formaran moléculas precursoras como la urea. "Nuestro estudio muestra cómo interfaces aparentemente mundanas pueden convertirse en espacios dinámicos de reacción, lo que sugiere que las moléculas biológicas pueden tener un origen más común de lo que se pensaba", afirma Signorell.
A largo plazo, la reacción directa de CO₂ y amoníaco en condiciones ambientales también podría tener potencial para la producción respetuosa con el clima de urea y productos derivados.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.






































