Zellgewebe darf nicht einfrieren
Als Frostschutzmittel-Ersatzprotein schützt Polyprolin einlagige Zellkulturen vor Frostschäden
Anzeigen
Mit Zuckern, Aminosäuren und speziellen Antifrostproteinen verhindert die Natur Frostschäden an Zellen. Um Zellkulturen vor Schäden durch Einfrieren zu bewahren, versetzen Menschen diese mit Lösungsmitteln und synthetischen Polymeren. Britische Wissenschaftler haben jetzt Natur und Synthese kombiniert: In einer Arbeit, die in der Zeitschrift Angewandte Chemie veröffentlicht wurde, führen sie das rein aus der natürlichen Aminosäure bestehende Polyprolin als wirkungsvolles Frostschutzmittel für einlagige Zellkulturen ein.
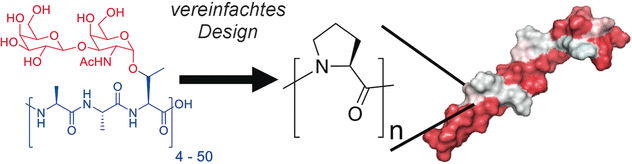
© Wiley-VCH
Die lebende Zelle ist gegenüber Einfrieren und Auftauen extrem empfindlich. Eiskristalle können die Zellmembran und Organellen mechanisch schädigen, und der Wasserentzug kann die osmotischen Verhältnisse bis zum Platzen der Zellen verändern. Andererseits werden Zellkulturen routinemäßig im tiefgefrorenen, „vitrifizierten“ Zustand gelagert, bevor sie zum Beispiel in der Transplantationsmedizin oder Grundlagenforschung gebraucht werden. Zum Zweck der Kryokonservierung fügt man Frostschutzmittel wie Dimethylsulfoxid hinzu. Ein Nachteil sind jedoch die notwendigen großen Mengen dieser Lösungsmittel, und längst nicht alle Zellen lassen sich auf diese Weise lebensfähig wiedergewinnen.
Die Natur hat ihre eigenen Frostschutzmittel: Organismen im eiskalten Meerwasser produzieren zum Beispiel Antifrost-Glycoproteine, um die Bildung von Eiskristallen zu vermeiden. Deren Verfügbarkeit für biomedizinische Anwendungen ist jedoch nicht immer gegeben, und die Immuntoleranz ist ein wiederkehrendes Problem. Mit synthetischen Polymeren kann man, wie man herausgefunden hat, die Antifrostwirkung der Glycoproteine nachahmen. Interessanter wäre jedoch ein einfaches, peptidisches Rückgrat für ein solches Polymer. Diesen Ansatz verfolgt die Gruppe um Matthew Gibson an der Universität Warwick, Großbritannien. Die Wissenschaftler schlagen Polyprolin als vielseitiges alternatives Kryokonservierungsmittel vor. Polyprolin besteht rein aus der natürlichen Aminosäure Prolin.
Die Besonderheit von Prolin ist seine Eigenschaft, im Gegensatz zu anderen Aminosäuren keine Wasserstoffbrücken zu anderen Struktursegmenten ausbilden zu können, wenn es in einem Peptid eingebaut ist. „Infolgedessen ist es gleichzeitig wasserlöslich und ziemlich wasserabweisend, genau wie AFP I“, schreiben die Autoren. AFP I ist ein natürliches Frostschutzprotein. Den Ergebnissen zufolge hat Polyprolin eine ähnlich strukturierte Oberfläche wie natürliche Frostschutzproteine. Dieses „fleckenartige“ löslich-unlösliche Strukturmotiv scheint beim Auftauen hilfreich zu sein, um die Umkrstallisation von Eis zu unterbinden. Die freie Aminosäure Prolin ist übrigens selbst ein natürliches Frostschutzmittel: Pflanzenzellen produzieren besonders viel Prolin, um bei kalten Temperaturen ihr osmotisches Gleichgewicht zu behalten und sich vor Austrocknung zu schützen.
Diese Kombination von Prolin/Polyprolin setzten die Wissenschaftler dann für ein Gefrier-Tau-Testsystem von adhärenten Zellkulturen ein. Zunächst inkubierten sie die Zell-Einzelschicht mit einer Mischung aus Dimethylsulfoxid und Prolin, dann fügten sie Polyprolin hinzu. Gegenüber der Kontrolle ohne Polyprolin, nur mit Dimethylsulfoxid, hatten doppelt so viele Zellen überlebt. Das bedeutet, dass für die Kryokonservierung deutlich weniger Lösungsmittel verwendet werden muss und die Zellen in einer möglichst natürlichen Umgebung bleiben können. Obwohl weitere Analysen zeigen müssen, ob tatsächlich alle Zellfunktionen erhalten bleiben, präsentierten die Autoren mit dieser Arbeit Polyprolin als höchst interessantes Biopolymer, das nur aus natürlichen Bausteinen besteht und die Eiskristallbildung für die biologische Lagerung wirkungsvoll unterbindet.