Wer hat 2018 den Nobelpreis für Physiologie oder Medizin erhalten und wofür?
Anzeigen
Der Nobelpreis für Physiologie oder Medizin konzentriert sich auf die Erforschung von Krebsimmuntherapien. Zwei Pioniere auf diesem Gebiet wurden für ihre fast lebenslange Forschung auf diesem Gebiet ausgezeichnet.
Nobel Foundation
Die Preisträger
James P. Allison
Die 1948 geborenen Wissenschaftler arbeiteten an mehreren renommierten und großen Krebsforschungsinstituten. Seine Karriere hat Stationen in Berkely, Scripps und MD Anderson Cancer Research Center, in seiner texanischen Heimat, gesehen.
Tasuku Honjo
Der japanische Wissenschaftler wurde 1942 geboren. Zu seinen Karrierestationen gehören Forschungseinrichtungen in den USA und Japan. Er arbeitete am NIH, der Carnegie Institution und an Universitäten in Tokio, Osaka und Kyoto, seinem Geburtsort.
Die Wissenschaft
Krebs tötet jedes Jahr Millionen von Menschen und ist eine der größten gesundheitlichen Herausforderungen der Menschheit. Durch die Stimulierung der inhärenten Fähigkeit unseres Immunsystems, Tumorzellen anzugreifen, haben die diesjährigen Nobelpreisträger ein völlig neues Prinzip für die Krebstherapie etabliert.
James P. Allison studierte ein bekanntes Protein, das als Bremse für das Immunsystem fungiert. Er erkannte das Potenzial, die Bremse zu lösen und damit unsere Immunzellen zu befreien, um Tumore anzugreifen. Dieses Konzept entwickelte er dann zu einem völlig neuen Ansatz für die Behandlung von Patienten.
Parallel dazu entdeckte Tasuku Honjo ein Protein auf Immunzellen und zeigte nach sorgfältiger Erforschung seiner Funktion schließlich, dass es auch als Bremse wirkt, jedoch mit einem anderen Wirkmechanismus. Die auf seiner Entdeckung basierenden Therapien erwiesen sich als bemerkenswert wirksam im Kampf gegen Krebs.
Allison und Honjo zeigten, wie verschiedene Strategien zur Hemmung der Bremsen des Immunsystems bei der Behandlung von Krebs eingesetzt werden können. Die wegweisenden Entdeckungen der beiden Preisträger sind ein Meilenstein in unserem Kampf gegen den Krebs.
Kann unsere Immunabwehr für die Krebsbehandlung eingesetzt werden?
Krebs umfasst viele verschiedene Krankheiten, die alle durch unkontrollierte Vermehrung von abnormalen Zellen mit der Fähigkeit zur Ausbreitung auf gesunde Organe und Gewebe gekennzeichnet sind. Für die Krebsbehandlung stehen eine Reihe von therapeutischen Ansätzen zur Verfügung, darunter Chirurgie, Bestrahlung und andere Strategien, von denen einige mit früheren Nobelpreisen ausgezeichnet wurden. Dazu gehören Methoden zur Hormonbehandlung von Prostatakrebs, Chemotherapie und Knochenmarktransplantation bei Leukämie. Allerdings ist die Behandlung von fortgeschrittenem Krebs nach wie vor immens schwierig, und neue therapeutische Strategien sind dringend erforderlich.
Ende des 19. und Anfang des 20. Jahrhunderts entstand das Konzept, dass die Aktivierung des Immunsystems eine Strategie zum Angriff auf Tumorzellen sein könnte. Es wurde versucht, Patienten mit Bakterien zu infizieren, um die Abwehr zu aktivieren. Diese Bemühungen hatten nur geringe Auswirkungen, aber eine Variante dieser Strategie wird heute bei der Behandlung von Blasenkrebs eingesetzt. Es wurde festgestellt, dass mehr Wissen benötigt wurde. Viele Wissenschaftler betreiben intensive Grundlagenforschung und entdeckten grundlegende Mechanismen, die die Immunität regulieren und zeigten auch, wie das Immunsystem Krebszellen erkennen kann. Trotz bemerkenswerter wissenschaftlicher Fortschritte erwies sich der Versuch, verallgemeinerbare neue Strategien gegen Krebs zu entwickeln, als schwierig.
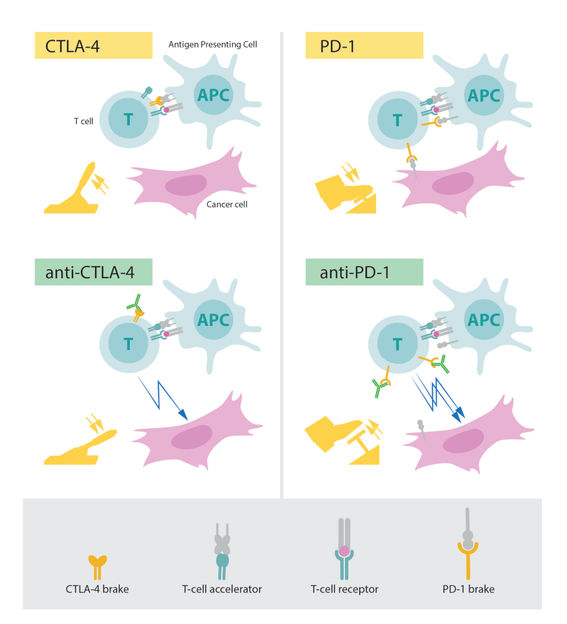
Beschleuniger und Bremsen in unserem Immunsystem
Die grundlegende Eigenschaft unseres Immunsystems ist die Fähigkeit, "Selbst" von "Nicht-Selbst" zu unterscheiden, so dass eindringende Bakterien, Viren und andere Gefahren angegriffen und beseitigt werden können. T-Zellen, eine Art weiße Blutkörperchen, sind Schlüsselpersonen bei dieser Verteidigung. Es wurde gezeigt, dass T-Zellen Rezeptoren haben, die an als nicht selbst erkannte Strukturen binden, und solche Wechselwirkungen lösen das Immunsystem aus, sich in der Abwehr zu engagieren. Aber auch zusätzliche Proteine, die als T-Zell-Beschleuniger wirken, sind erforderlich, um eine vollständige Immunantwort auszulösen. Viele Wissenschaftler haben zu dieser wichtigen Grundlagenforschung beigetragen und andere Proteine identifiziert, die als Bremsen auf den T-Zellen wirken und die Immunaktivierung hemmen. Diese komplizierte Balance zwischen Gaspedalen und Bremsen ist für eine strenge Kontrolle unerlässlich. Es stellt sicher, dass das Immunsystem ausreichend gegen fremde Mikroorganismen vorgeht und vermeidet gleichzeitig die übermäßige Aktivierung, die zur Zerstörung gesunder Zellen und Gewebe durch Autoimmunerkrankungen führen kann.
Ein neues Konzept für die Immuntherapie
In den 90er Jahren studierte James P. Allison in seinem Labor an der University of California, Berkeley, das T-Zell-Protein CTLA-4. Er war einer von mehreren Wissenschaftlern, die die Beobachtung gemacht hatten, dass CTLA-4 als Bremse auf T-Zellen wirkt. Andere Forscherteams nutzten den Mechanismus als Ziel bei der Behandlung von Autoimmunerkrankungen. Allison hatte jedoch eine ganz andere Idee. Er hatte bereits einen Antikörper entwickelt, der an CTLA-4 binden und dessen Funktion blockieren konnte. Er machte sich nun auf den Weg, um zu untersuchen, ob die CTLA-4-Blockade die T-Zellen-Bremse lösen und das Immunsystem zum Angriff auf Krebszellen aktivieren könnte. Allison und seine Mitarbeiter führten Ende 1994 ein erstes Experiment durch, das in ihrer Begeisterung in der Weihnachtspause sofort wiederholt wurde. Die Ergebnisse waren spektakulär. Mäuse mit Krebs wurden durch die Behandlung mit den Antikörpern geheilt, die die Bremse hemmen und die Antitumor-T-Zellaktivität freisetzen. Trotz des geringen Interesses der Pharmaindustrie setzte Allison seine intensiven Bemühungen fort, die Strategie zu einer Therapie für den Menschen zu entwickeln. Aus mehreren Gruppen traten bald vielversprechende Ergebnisse hervor, und 2010 zeigte eine wichtige klinische Studie markante Effekte bei Patienten mit fortgeschrittenem Melanom, einer Art von Hautkrebs. Bei mehreren Patienten verschwanden die Anzeichen von Restkrebs. Solche bemerkenswerten Ergebnisse waren in dieser Patientengruppe noch nie zuvor zu sehen gewesen.
Entdeckung von PD-1 und seiner Bedeutung für die Krebstherapie
1992, einige Jahre vor der Entdeckung von Allison, entdeckte Tasuku Honjo PD-1, ein weiteres Protein, das auf der Oberfläche von T-Zellen exprimiert wird. Entschlossen, seine Rolle zu entwirren, untersuchte er seine Funktion akribisch in einer Reihe von eleganten Experimenten, die er über viele Jahre in seinem Labor an der Universität Kyoto durchführte. Die Ergebnisse zeigten, dass PD-1, ähnlich wie CTLA-4, als T-Zellen-Bremse funktioniert, aber mit einem anderen Mechanismus arbeitet. Im Tierversuch erwies sich die PD-1-Blockade auch als vielversprechende Strategie im Kampf gegen Krebs, wie Honjo und andere Gruppen zeigen. Die klinische Entwicklung folgte, und 2012 zeigte eine Schlüsselstudie eine klare Wirksamkeit bei der Behandlung von Patienten mit verschiedenen Krebsarten. Die Ergebnisse waren dramatisch, was zu einer langfristigen Remission und einer möglichen Heilung bei mehreren Patienten mit metastasierendem Krebs führte, einer Erkrankung, die bisher als im Wesentlichen unbehandelbar galt.
Immun-Checkpoint-Therapie bei Krebs heute und in Zukunft
Nach den ersten Studien, die die Auswirkungen der CTLA-4- und PD-1-Blockade zeigten, war die klinische Entwicklung dramatisch. Wir wissen heute, dass die Behandlung, die oft als "Immun-Checkpoint-Therapie" bezeichnet wird, das Ergebnis für bestimmte Gruppen von Patienten mit fortgeschrittenem Krebs grundlegend verändert hat. Ähnlich wie bei anderen Krebstherapien treten unerwünschte Nebenwirkungen auf, die schwerwiegend und sogar lebensbedrohlich sein können. Sie werden durch eine überaktive Immunantwort verursacht, die zu Autoimmunreaktionen führt, sind aber meist beherrschbar. Die intensive Weiterarbeit konzentriert sich auf die Aufklärung von Wirkungsmechanismen mit dem Ziel, die Therapie zu verbessern und Nebenwirkungen zu reduzieren.
Von den beiden Behandlungsstrategien hat sich die Checkpoint-Therapie gegen PD-1 als effektiver erwiesen und es werden positive Ergebnisse bei verschiedenen Krebsarten beobachtet, darunter Lungenkrebs, Nierenkrebs, Lymphom und Melanom. Neue klinische Studien zeigen, dass eine Kombinationstherapie, die sowohl auf CTLA-4 als auch auf PD-1 abzielt, noch effektiver sein kann, wie bei Patienten mit Melanom gezeigt wird. So haben Allison und Honjo Anstrengungen unternommen, verschiedene Strategien zu kombinieren, um die Bremsen des Immunsystems zu lösen und Tumorzellen noch effizienter zu eliminieren. Gegenwärtig laufen eine Vielzahl von Kontrollpunkt-Therapie-Studien gegen die meisten Krebsarten, und neue Kontrollpunkt-Proteine werden als Zielmoleküle getestet.
Seit mehr als 100 Jahren versuchen Wissenschaftler, das Immunsystem in den Kampf gegen Krebs einzubeziehen. Bis zu den bahnbrechenden Entdeckungen der beiden Preisträger war der Fortschritt in der klinischen Entwicklung bescheiden: Die Checkpoint-Therapie hat die Krebsbehandlung revolutioniert und die Art und Weise, wie wir Krebs behandeln, grundlegend verändert.
Originalveröffentlichung
Y Ishida, Y Agata, K Shibahara, and T Honjo; "Induced expression of PD-1, a novel member of the immunoglobulin gene superfamily, upon programmed cell death"; EMBO J; 1992
Dana R. Leach, Matthew F. Krummel, James P. Allison; "Enhancement of Antitumor Immunity by CTLA-4 Blockade"; Science; 1996
Eugene D. Kwon, Arthur A. Hurwitz, Barbara A. Foster, Christopher Madias, Andrew L. Feldhaus, Norman M. Greenberg, Maurice B. Burg, and James P. Allison; "Manipulation of T cell costimulatory and inhibitory signals for immunotherapy of prostate cancer"; PNAS; 1997
Hiroyuki Nishimura, Masato Nose, Hiroshi Hiai, Nagahiro Minato, Tasuku Honjo; "Development of Lupus-like Autoimmune Diseases by Disruption of the PD-1 Gene Encoding an ITIM Motif-Carrying Immunoreceptor"; Immunity; 1999
Gordon J. Freeman et al.; "Engagement of the Pd-1 Immunoinhibitory Receptor by a Novel B7 Family Member Leads to Negative Regulation of Lymphocyte Activation"; J Exper Med; 2000
F. Stephen Hodi et al.; "Biologic activity of cytotoxic T lymphocyte-associated antigen 4 antibody blockade in previously vaccinated metastatic melanoma and ovarian carcinoma patients"; PNAS; 2003
Yoshiko Iwai, Seigo Terawaki, Tasuku Honjo; "PD-1 blockade inhibits hematogenous spread of poorly immunogenic tumor cells by enhanced recruitment of effector T cells"; Int Immunology; 2004
Weitere News aus dem Ressort Wissenschaft
Meistgelesene News
Weitere News von unseren anderen Portalen
Verwandte Inhalte finden Sie in den Themenwelten
Themenwelt Antikörper
Antikörper sind spezialisierte Moleküle unseres Immunsystems, die gezielt Krankheitserreger oder körperfremde Substanzen erkennen und neutralisieren können. Die Antikörperforschung in Biotech und Pharma hat dieses natürliche Abwehrpotenzial erkannt und arbeitet intensiv daran, es therapeutisch nutzbar zu machen. Von monoklonalen Antikörpern, die gegen Krebs oder Autoimmunerkrankungen eingesetzt werden, bis hin zu Antikörper-Drug-Konjugaten, die Medikamente gezielt zu Krankheitszellen transportieren – die Möglichkeiten sind enorm.
Themenwelt Antikörper
Antikörper sind spezialisierte Moleküle unseres Immunsystems, die gezielt Krankheitserreger oder körperfremde Substanzen erkennen und neutralisieren können. Die Antikörperforschung in Biotech und Pharma hat dieses natürliche Abwehrpotenzial erkannt und arbeitet intensiv daran, es therapeutisch nutzbar zu machen. Von monoklonalen Antikörpern, die gegen Krebs oder Autoimmunerkrankungen eingesetzt werden, bis hin zu Antikörper-Drug-Konjugaten, die Medikamente gezielt zu Krankheitszellen transportieren – die Möglichkeiten sind enorm.