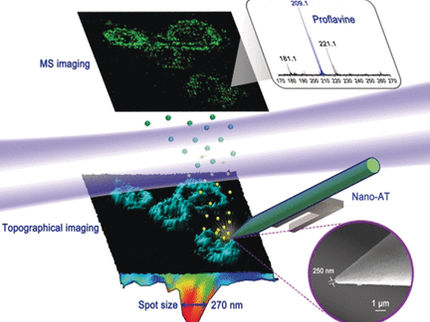
Die Abbildung des dynamischen zellulären Zoos wird erleichtert
Diese Arbeit wird die Möglichkeiten zur gleichzeitigen Überwachung vieler Prozesse in Zellen erweitern
Anzeigen
Stellen Sie sich die Schwierigkeit vor, fünf in einem Stadion verstreute Personen visuell zu verfolgen. Forscher vollbringen weitaus erstaunlichere Leistungen, indem sie viele verschiedene zelluläre Faktoren gleichzeitig verfolgen, aber sie benötigen ein erweitertes Fluoreszenz-Toolkit, um die derzeitigen Möglichkeiten zu verbessern.
Symbolbild
Computer-generated image
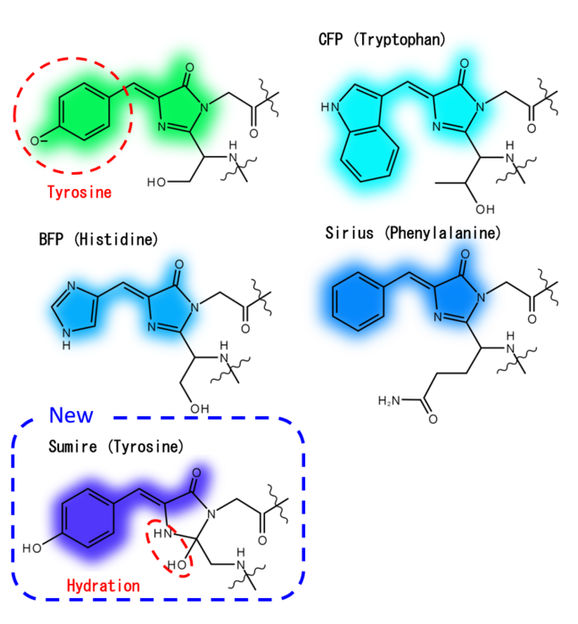
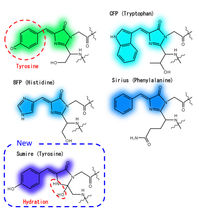
Chromophorstruktur von avGFP-Mutanten mit kurzer Wellenlänge
Kazunori Sugiura
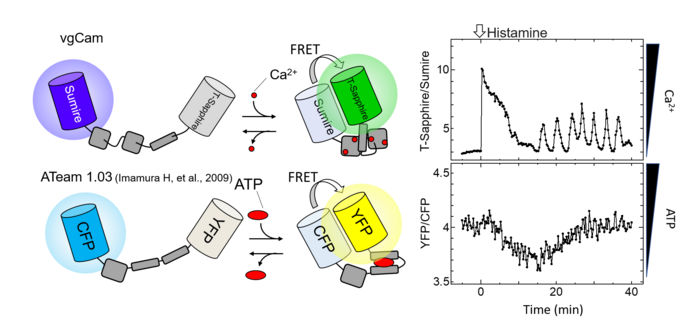
Schematische Darstellung der FRET-Sonde (links) sowie der Veränderungen der Kalzium- und ATP-Konzentration in derselben Zelle (rechts). Zugabe von Histamin bei 0 min.
Kazunori Sugiura
In einer kürzlich in Communications Biology veröffentlichten Studie haben Forscher des SANKEN (Institute of Scientific and Industrial Research) an der Universität Osaka ein Protein genetisch so verändert, dass es die kürzeste derzeit verfügbare Fluoreszenz-Emissionswellenlänge aufweist.
Fluoreszenz ist ein gängiges Mittel, um das Innenleben von Zellen mikroskopisch sichtbar zu machen. Ein Biomolekül von Interesse kann zum Beispiel genetisch mit einem fluoreszierenden Protein (d. h. einem Fluorophor) versehen werden, das eine bestimmte Lichtfarbe (d. h. Wellenlänge) aussendet. Indem man verschiedene Arten von Biomolekülen mit unterschiedlichen Fluorophoren versieht, die jeweils eine andere Lichtwellenlänge aussenden, kann man all diese verschiedenen Biomoleküle gleichzeitig identifizieren und verfolgen. Durch die Erweiterung des Spektrums der möglichen emittierten Wellenlängen kann die Anzahl der Biomoleküle, die gleichzeitig verfolgt werden können, erhöht werden. Dies ist das Problem, das die Forscher angehen wollten.
"Die Grenze der kurzen Emissionswellenlänge von fluoreszierenden Proteinen ist in den letzten 10 Jahren gleich geblieben", erklärt Kazunori Sugiura, Hauptautor. "Das liegt daran, dass sich frühere Forscher in der Regel darauf konzentrierten, geringfügige Änderungen an einer der Aminosäuren der grün fluoreszierenden Proteinmutanten vorzunehmen.
Die Forscher der Universität Osaka konzentrierten sich stattdessen auf die Optimierung der Wechselwirkungen zwischen dem Fluoreszenzzentrum (d. h. dem Chromophor) und den umgebenden Wassermolekülen und Aminosäuren. Durch die Verhinderung der Ionisierung und die Stabilisierung der Hydratisierung des Chromophors zeigte das resultierende Fluorophor - Sumire genannt - mehrere bemerkenswerte Fluoreszenzeigenschaften: (1) Emission bei 414 Nanometern, ein neuer Rekord; (2) eine Helligkeit, die fast das Vierfache des Standes der Technik beträgt; und (3) stabile Emission von pH 5,5-9,0, was den größten Teil des pH-Bereichs umfasst, der in den meisten Zellen vorkommt.
"Wir haben auch den Fluoreszenz-Resonanz-Energie-Transfer, eine gängige biomolekulare Bildgebungstechnik, zwischen Sumire und handelsüblichen Protein-Fluorophoren erreicht", sagt Takeharu Nagai, leitender Autor. "Dies zeigt die Kompatibilität von Sumire mit der modernen Multiparameteranalyse."
Mit dieser Arbeit ist es gelungen, das Instrumentarium für die zelluläre Bildgebung mit Hilfe der Gentechnik zu erweitern, indem das Chromophor eines fluoreszierenden Proteins in einer Weise verändert wurde, die bisher nicht in Betracht gezogen worden war. Der Ansatz der Forscher der Universität Osaka wird nützlich sein, um den Bereich der erreichbaren Fluoreszenzwellenlängen von künstlich hergestellten Proteinen weiter zu erweitern, was den Forschern helfen wird, biologische Prinzipien aufzudecken, die für normale Gesundheit und Krankheit wichtig sind.
Hinweis: Dieser Artikel wurde mit einem Computersystem ohne menschlichen Eingriff übersetzt. LUMITOS bietet diese automatischen Übersetzungen an, um eine größere Bandbreite an aktuellen Nachrichten zu präsentieren. Da dieser Artikel mit automatischer Übersetzung übersetzt wurde, ist es möglich, dass er Fehler im Vokabular, in der Syntax oder in der Grammatik enthält. Den ursprünglichen Artikel in Englisch finden Sie hier.
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft
Meistgelesene News
Weitere News von unseren anderen Portalen
Verwandte Inhalte finden Sie in den Themenwelten
Themenwelt Zellanalyse
Die Zellanalyse ermöglicht es uns, Zellen in ihren vielfältigen Facetten zu erforschen und zu verstehen. Von der Einzelzellanalyse über die Durchflusszytometrie bis hin zur Bildgebungstechnologie – die Zellanalyse bietet uns wertvolle Einblicke in die Struktur, Funktion und Interaktion von Zellen. Ob in der Medizin, der biologischen Forschung oder der Pharmakologie – die Zellanalyse revolutioniert unser Verständnis von Krankheiten, Entwicklung und Behandlungsmöglichkeiten.
Themenwelt Zellanalyse
Die Zellanalyse ermöglicht es uns, Zellen in ihren vielfältigen Facetten zu erforschen und zu verstehen. Von der Einzelzellanalyse über die Durchflusszytometrie bis hin zur Bildgebungstechnologie – die Zellanalyse bietet uns wertvolle Einblicke in die Struktur, Funktion und Interaktion von Zellen. Ob in der Medizin, der biologischen Forschung oder der Pharmakologie – die Zellanalyse revolutioniert unser Verständnis von Krankheiten, Entwicklung und Behandlungsmöglichkeiten.