DNA-Klau stärkt die Immunvielfalt
„Diebstahl“ des fremden Erbmaterials folgt einem gewissen Plan
Anzeigen
Um gegen Krankheitserreger vorgehen zu können, braucht das Immunsystem eine riesige Zahl passender Antikörper. In einer MDC-Studie beschreibt die Gruppe der BIH-Professorin Kathrin de la Rosa im Fachblatt PNAS einen „diebischen“ Mechanismus, der zur Vielfalt dieser Abwehrstoffe beiträgt.
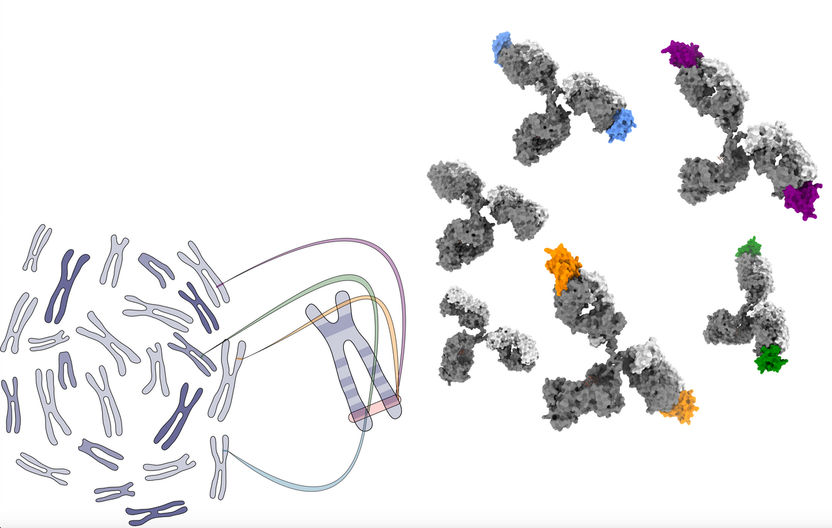
Die Abbildung illustriert die Diversifizierung von Antikörpern durch den Austausch von DNA zwischen Chromosomen. DNA, die auf entfernten Loci verschiedener Chromosomen kodiert wird, kann in den Locus der schweren Kette der Antikörper integriert werden (sowohl in das mütterliche als auch das väterliche Allel). Auf diese Weise tragen andere Teile unseres Erbguts zur Bildung von Antikörpern bei, die zusätzliche Fragmente enthalten (hier farblich hervorgehoben).
© AG de la Rosa, MDC
Vor einigen Jahren machten Professorin Kathrin de la Rosa und ihre Kolleg*innen im Labor des Schweizer Immunologen Antonio Lanzavecchia eine ungewöhnliche Entdeckung. Das Team stieß im Blut von Malaria-Patient*innen auf Antikörper, für deren Herstellung der Bauplan eines Gens verwendet worden war, das eigentlich eine völlig andere Aufgabe besaß. „Gewöhnlich kodiert dieses Gen für einen Rezeptor, der das Immunsystem bremst – was der Malaria-Erreger wahrscheinlich nutzt, um sich leichter zu vermehren“, erklärt die Leiterin der Arbeitsgruppe „Immunmechanismen und humane Antikörper“ am Berliner Max-Delbrück-Centrum für Molekulare Medizin in der Helmholtz-Gemeinschaft (MDC) und dem Berlin Institute of Health in der Charité (BIH).
Das Immunsystem der an Malaria erkrankten Menschen hatte aber ganz offensichtlich zurückgeschlagen: „Die Antikörper, die wir bei ihnen fanden, hatten einen Teil dieses Rezeptors namens LAIR1 integriert und konnten dadurch die Parasiten effektiver erkennen“, sagt die Forscherin, die eine Johanna Quandt-Professur für Immunmechanismen in der Translation am BIH innehat, die von der Stiftung Charité gefördert wird.
Die Strategie ist weit verbreitet
Der Fund warf bei Kathrin de la Rosa damals viele Fragen auf: War vielleicht ausschließlich das Immunsystem von Malaria-Patient*innen zu diesem Trick fähig? Oder allein das von Menschen afrikanischer Abstammung? Konnte lediglich der LAIR1-Rezeptor in die Antikörper integriert werden? Oder war man womöglich auf einen noch völlig unbekannten Mechanismus gestoßen, den die menschliche Körperabwehr generell nutzt, um in ihren B-Zellen möglichst passgenaue Antikörper herzustellen?
In einer Studie, die jetzt im Fachblatt „Proceedings of the National Academy of Sciences“ (PNAS) erschienen ist, geben de la Rosa und ihr Team erste Antworten auf diese Fragen.
„Wir haben bei mehr als 80 Prozent der untersuchten Personen aus Afrika und Europa Antikörper ausmachen können, bei deren Herstellung auf fremde Gene oder andere weit entfernt liegende DNA-Fragmente zurückgegriffen wurde“, berichtet der Erstautor der Studie, Mikhail Lebedin aus de la Rosas Arbeitsgruppe am MDC. „Dabei war es unerheblich, ob diese Menschen zuvor an Malaria erkrankt gewesen waren oder welcher ethnischen Gruppe sie angehörten.“
Der Diebstahl folgt einem Plan
Das fremde Material habe man zudem ausschließlich in einer bestimmten Region der Antikörper gefunden, den sogenannten schweren Ketten der Y-förmigen Eiweißmoleküle, sagt Lebedin. Für ihn und seine Kolleg*innen war dies ein wichtiger Hinweis darauf, dass der „Diebstahl“ des fremden Erbmaterials offenbar einem gewissen Plan folgte. Das Indiz hierfür fanden die Forschenden, als sie die entwendeten Fragmente auf dem menschlichen Genom kartierten und dabei auffällige Muster ihrer Herkunft entdeckten. „Sie stammten zum Beispiel besonders oft aus den Mitochondrien der Zellen oder aus den Enden der Chromosomen im Zellkern“, erläutert Lebedin.
Für ihre Studie hatten die Forscher*innen eigens eine Technik entwickelt, um das Transkript der Antikörper – also die RNA-Matrize, die bei der Proteinherstellung abgelesen wird – im Hochdurchsatz zu untersuchen. „Wir brauchten ein besonders empfindliches Verfahren, da Antikörper mit fremden Bausteinen in der breiten Masse dieser Abwehrstoffe ansonsten leicht untergehen“, sagt de la Rosa. „Denn nur etwa einer von zehn- bis hunderttausend Antikörpern im Blut besitzt diese speziellen Merkmale.“ Aber anscheinend reiche das aus, um das Immunsystem unter gewissen Umständen – wie bei Malaria – besonders kampffähig zu machen.
Das Ziel ist ein zellulärer Impfstoff
„Bislang war man davon ausgegangen, dass die Vielfalt der Antikörper allein durch Mutationen innerhalb der Antikörper-Gene entsteht“, erklärt de la Rosa. Doch offenbar sei diese Annahme falsch gewesen. „Trotzdem wirft unsere Studie nun eigentlich mehr Fragen auf, als dass sie Antworten liefert“, sagt die Forscherin. Die beiden für de la Rosa wichtigsten Fragen lauten: Wie funktioniert der DNA-Diebstahl im Detail? Und lässt er sich womöglich nutzen, um künftig gezielt neuartige Antikörper und B-Zellen, die diese produzieren, künstlich im Labor herzustellen?
„Während der Corona-Pandemie haben Millionen Menschen weltweit gelernt und auch persönlich erlebt, wie wichtig Antikörper sind, denn sie schützen uns vor Krankheitserregern wie SARS-CoV-2. Sie werden gebildet, wenn wir infiziert oder geimpft sind“, sagt die Immunologin. „Für mich ist es sehr bedeutsam zu verstehen, wie die Vielfalt der Antikörper zustande kommt, denn nur so können wir neue Ansätze entwickeln, die uns in Zukunft zu noch besseren Impfstoffen verhelfen.“ Unter anderem schwebt Kathrin de la Rosa ein zellulärer Impfstoff vor. Für ihn möchte sie körpereigene B-Zellen in ihrem Labor so verändern, dass sie Antikörper produzieren, die noch schlagkräftiger sind als ihre natürlichen Vorbilder.
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft
Meistgelesene News
Weitere News von unseren anderen Portalen
Verwandte Inhalte finden Sie in den Themenwelten
Themenwelt Antikörper
Antikörper sind spezialisierte Moleküle unseres Immunsystems, die gezielt Krankheitserreger oder körperfremde Substanzen erkennen und neutralisieren können. Die Antikörperforschung in Biotech und Pharma hat dieses natürliche Abwehrpotenzial erkannt und arbeitet intensiv daran, es therapeutisch nutzbar zu machen. Von monoklonalen Antikörpern, die gegen Krebs oder Autoimmunerkrankungen eingesetzt werden, bis hin zu Antikörper-Drug-Konjugaten, die Medikamente gezielt zu Krankheitszellen transportieren – die Möglichkeiten sind enorm.
Themenwelt Antikörper
Antikörper sind spezialisierte Moleküle unseres Immunsystems, die gezielt Krankheitserreger oder körperfremde Substanzen erkennen und neutralisieren können. Die Antikörperforschung in Biotech und Pharma hat dieses natürliche Abwehrpotenzial erkannt und arbeitet intensiv daran, es therapeutisch nutzbar zu machen. Von monoklonalen Antikörpern, die gegen Krebs oder Autoimmunerkrankungen eingesetzt werden, bis hin zu Antikörper-Drug-Konjugaten, die Medikamente gezielt zu Krankheitszellen transportieren – die Möglichkeiten sind enorm.