Un nouveau matériau ouvre la voie aux médicaments télécommandés et aux pilules électroniques
Les résultats des chercheurs de Chalmers ont été transmis au développement de produits, effectué par la société spin-off Nyctea Technologies.
Annonces
Les biomédicaments sont produits par des cellules vivantes et sont utilisés, entre autres, pour traiter le cancer et les maladies auto-immunes. L'une des difficultés réside dans le fait que ces médicaments sont très coûteux à produire, ce qui en limite l'accès au niveau mondial. Des chercheurs de Chalmers ont inventé un matériau qui utilise des signaux électriques pour capturer et libérer des biomolécules. Cette nouvelle méthode efficace pourrait avoir un impact majeur sur le développement des biomédicaments et ouvrir la voie au développement de pilules électroniques et d'implants médicamenteux.
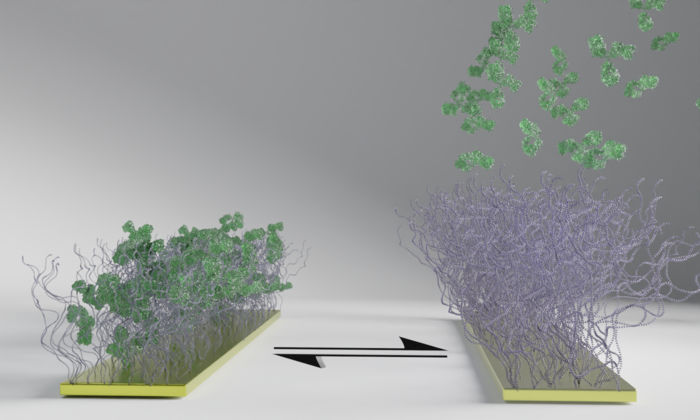
La surface polymère, représentée par des brosses sur l'image, réagit à une impulsion électrique en changeant d'état, passant de la capture à la libération des biomolécules vertes. La surface polymère capture d'abord les biomolécules (à gauche), puis les libère lorsque l'électricité est activée (à droite). Contrairement aux biomolécules, les brosses en polymère restent attachées malgré l'impulsion électrique, et le processus peut être répété.
Illustration: Chalmers University of Technology | Gustav Ferrand-Drake del Castillo
Le nouveau matériau est une surface polymère qui, sous l'effet d'une impulsion électrique, change d'état, passant de la capture à la libération de biomolécules. Cela a plusieurs applications possibles, y compris l'utilisation comme outil pour la séparation efficace d'un médicament des autres biomolécules que les cellules créent dans la production de médicaments biologiques. Les résultats de l'étude ont été récemment publiés dans la revue scientifique Angewandte Chemie.
Les biomédicaments sont très coûteux à produire en raison de l'absence d'une technique de séparation efficace. De nouvelles techniques offrant un rendement plus élevé des médicaments sont nécessaires pour réduire les coûts de production et, au final, le coût du traitement des patients.
"Nos surfaces polymères offrent une nouvelle façon de séparer les protéines en utilisant des signaux électriques pour contrôler la façon dont elles sont liées à une surface et libérées de celle-ci, sans affecter la structure de la protéine", explique Gustav Ferrand-Drake del Castillo, qui a soutenu publiquement sa thèse de doctorat en chimie à Chalmers et qui est l'auteur principal de l'étude.
La technique de séparation classique - la chromatographie - lie étroitement les biomolécules à la surface et des produits chimiques puissants sont nécessaires pour les faire libérer, ce qui entraîne des pertes et un faible rendement. De nombreux nouveaux médicaments se sont révélés très sensibles aux produits chimiques puissants, ce qui pose un problème de production majeur pour la prochaine génération de biomédicaments. La moindre consommation de produits chimiques se traduit par un avantage pour l'environnement, tandis que le fait que les surfaces du nouveau matériau puissent également être réutilisées à travers plusieurs cycles est une propriété essentielle. Le processus peut être répété des centaines de fois sans affecter la surface.
Fonctions dans les fluides biologiques
Le matériau fonctionne également dans les fluides biologiques avec un pouvoir tampon, c'est-à-dire des fluides ayant la capacité de contrecarrer les changements de la valeur du pH. Cette propriété est remarquable car elle ouvre la voie à la création d'une nouvelle technique d'implants et de "pilules" électroniques qui libèrent le médicament dans l'organisme par activation électronique.
"On peut imaginer un médecin, ou un programme informatique, mesurant le besoin d'une nouvelle dose de médicament chez un patient, et un signal télécommandé activant la libération du médicament à partir de l'implant situé dans le tissu ou l'organe même où il est nécessaire", explique Gustav Ferrand-Drake del Castillo.
La libération locale et activée de médicaments est aujourd'hui disponible sous la forme de matériaux qui changent d'état en cas de modification du milieu chimique environnant. Par exemple, on produit des comprimés de matériaux sensibles au pH lorsqu'on veut contrôler la libération d'un médicament dans le tractus gastro-intestinal, qui est un environnement présentant des variations naturelles de la valeur du pH. Mais dans la plupart des tissus de l'organisme, la valeur du pH ou d'autres paramètres chimiques ne varient pas.
"Pouvoir contrôler la libération et l'absorption de protéines dans le corps avec des interventions chirurgicales minimales et sans injection d'aiguilles est, selon nous, une propriété unique et utile. Le développement d'implants électroniques n'est qu'une des nombreuses applications concevables dans plusieurs années. La recherche qui nous aide à lier l'électronique à la biologie au niveau moléculaire est une pièce importante du puzzle dans cette direction", déclare Gustav Ferrand-Drake del Castillo.
Un autre avantage de la nouvelle méthode est qu'elle ne nécessite pas de grandes quantités d'énergie. La faible consommation d'énergie est due au fait que l'épaisseur du polymère à la surface de l'électrode est très fine, à l'échelle du nanomètre, ce qui signifie que la surface réagit immédiatement aux petits signaux électrochimiques.
"L'électronique dans les environnements biologiques est souvent limitée par la taille de la batterie et les pièces mécaniques mobiles. L'activation au niveau moléculaire réduit à la fois les besoins en énergie et la nécessité de pièces mobiles", explique Gustav Ferrand-Drake del Castillo.
La percée a commencé par une thèse de doctorat
Les recherches à l'origine de cette technique ont été menées à l'époque où Gustav Ferrand-Drake del Castillo était doctorant dans l'équipe de recherche du professeur Andreas Dahlin de l'Université Chalmers, dans la division de la chimie des surfaces appliquées. Le projet portait sur des surfaces polymères qui changent d'état, passant de neutre à chargé, en fonction du pH de la solution environnante. Les chercheurs ont ensuite réussi à créer un matériau suffisamment solide pour rester sur la surface lorsqu'il est soumis à des signaux électriques répétés, tout en étant suffisamment fin pour changer réellement de valeur de pH suite à l'électrochimie sur la surface.
"Peu après, nous avons découvert que nous pouvions utiliser les signaux électriques pour contrôler la liaison et la libération des protéines et des biomolécules, et que le matériau de l'électrode fonctionnait dans des solutions biologiques telles que le sérum et le sang centrifugé. Nous pensons et espérons que nos découvertes pourront être d'une grande utilité pour le développement de nouveaux médicaments", déclare Andreas Dahlin.
Au cours de l'année écoulée, les résultats des chercheurs de Chalmers sont passés au développement de produits, effectué par la société spin-off Nyctea Technologies. La société compte déjà des clients parmi les principaux chercheurs et entreprises pharmaceutiques.
Note: Cet article a été traduit à l'aide d'un système informatique sans intervention humaine. LUMITOS propose ces traductions automatiques pour présenter un plus large éventail d'actualités. Comme cet article a été traduit avec traduction automatique, il est possible qu'il contienne des erreurs de vocabulaire, de syntaxe ou de grammaire. L'article original dans Anglais peut être trouvé ici.
Publication originale
Autres actualités du département science
Actualités les plus lues
Plus actualités de nos autres portails
Il se trame quelque chose dans le secteur des sciences de la vie…
Voilà à quoi ressemble le véritable esprit pionnier : De nombreuses start-ups innovantes apportent des idées fraîches, de la passion et un esprit d'entreprise pour changer positivement le monde de demain. Plongez dans l'univers de ces jeunes entreprises et profitez de la possibilité d'entrer en contact avec leurs fondateurs.