Reparatur statt Neubau: Beschädigte Zell-Kraftwerke haben eigenen “Werkstatt-Modus”
Molekularen Reparaturweg für zelluläre Energiegewinnung gefunden
Anzeigen
Eine durch Schäden gestörte Energieversorgung der Zelle kann sich selbst vor Funktionseinbußen schützen und in einer Art Werkstatt-Modus reparieren. Das zeigt ein neues Paper von der Molekularbiologin Professorin Dr. Aleksandra Trifunovic und Dr. Karolina Szcepanowska, einer leitenden Wissenschaftlerin in ihrem Team, die am Exzellenzcluster für Alternsforschung CECAD der Universität zu Köln mitwirken.
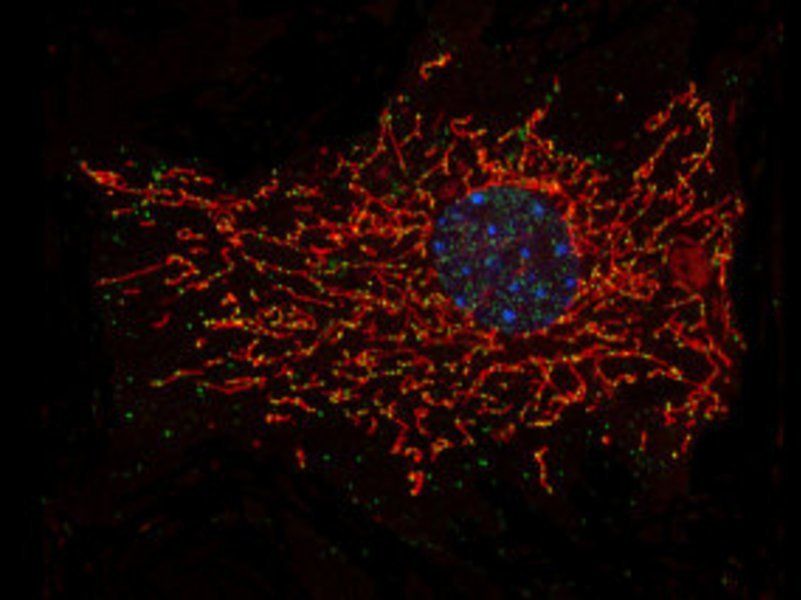
Bildgebung einer Zelle: Zellkern in blau, Mitochondrienstruktur in rot, und mitochondriale DNA in grün.
(c) Alexandra Kukat
Trifunovic arbeitet an sogenannten Mitochondrien, den Energie-Kraftwerken, die einer jeden Zelle innewohnen. Zu den Aufgaben von Mitochondrien gehören ganz grundlegende Prozesse wie die konstante Versorgung der Zelle mit Energie. Die Kraftwerksmaschine in den Mitochondrien besteht aus fünf Bauteilen, den so genannten Komplexen I – V. In ihnen wird schlussendlich die Nahrung, die wir essen, in nutzbare Energie umgewandelt. Ist die zelluläre Energieversorgung aufgrund von Störungen in Signalprozessen nicht mehr gewährleistet, zieht dies schwerwiegende Folgen für den gesamten Organismus und Krankheiten nach sich.
“In unserer jüngsten Arbeit haben wir einen Rettungsweg entdeckt, mit dessen Hilfe Zellen Störungen eines besonders empfindlichen Anteils des Komplex I reparieren können”, so Trifunovic. “Etwas zu reparieren ist dabei ein weitaus ressourcenschonenderer Selbsthilfe-Mechanismus im Vergleich zu dem Aufwand, den eine vollständige Zerstörung und ein Neuaufbau dieses gesamten Bauteils bedeuten würde.”
Der von Trifunovic identifizierte spezifische Rettungsweg wirke für die Zelle zudem wie ein Sicherheitsventil. Wird der Rettungsweg aktiv, schaltet sich das aus der Funktion geratene Bauteil ganz zügig in einen Shutdown-Modus und kommt “in die Werkstatt”. So verhindern die Zellen direkt, dass in der Kraftwerksmaschine schädliche reaktive Sauerstoffspezies produziert und abgegeben werden. Trifunovic: “Bislang ist nur sehr wenig darüber bekannt, wie diese Maschinerie gewartet und reguliert wird. Unsere Ergebnisse werfen Licht auf diesen Prozess und erlauben uns, weitere therapeutische Möglichkeiten zu erforschen.”
Für anschließende Fragen hat die Molekularbiologin Trifunovic bereits einen Anhaltspunkt. Neben der allgemeinen Neuheit des gesamten Mechanismus habe sie besonders erstaunt, dass es für den Organismus oftmals besser ist, einige Kraftwerksmaschinen-Bauteile trotz Schäden am Laufen zu halten und nicht alle geschädigten Bauteile gleichzeitig in den Reparatur-Modus zu stellen oder ganz abzubauen. Dabei spielen möglicherweise Funktionen auch von einzelnen Komponenten eine Rolle, die über die Energieversorgung hinausgehen. Wie weitreichend und vielseitig der jetzt entdeckte molekulare Reparaturpfad wirkt, möchte Trifunovic weiter erforschen, um sein volles Potenzial für mögliche Krankheitstherapien zu erkennen.
Trifunovic betonte, dass diese Forschung nicht ohne den Beitrag ihrer Kollegin Dr. Karolina Szczepanowska möglich gewesen wäre. Sie war eine treibende Kraft hinter der Projekt. Auch die Zusammenarbeit mit anderen Forschungsgruppen und Universitäten hat das Kölner Team entscheidend vorangebracht.



























































