Tierversuche: Die Alternative aus der Kulturschale
Anzeigen
Bis ein Medikament auf den Markt kommt, vergehen Jahre, werden hohe Millionenbeträge ausgegeben und finden viele Tierversuche statt. Fehlschläge während der Entwicklung sind keine Seltenheit. Der häufigste Grund: Die Substanzen sind giftig für die Leber. Um das Risiko besser zu bewerten und die Zahl der Tierversuche zu reduzieren, wird an Testsystemen in der Kulturschale geforscht. In einer aktuellen Studie des Leibniz-Instituts für Arbeitsforschung mit einem internationalen Team wird eine Methode vorgestellt, mit der in der Zellkultur das Risiko einer Substanz eingeschätzt werden kann, die Leber zu schädigen.
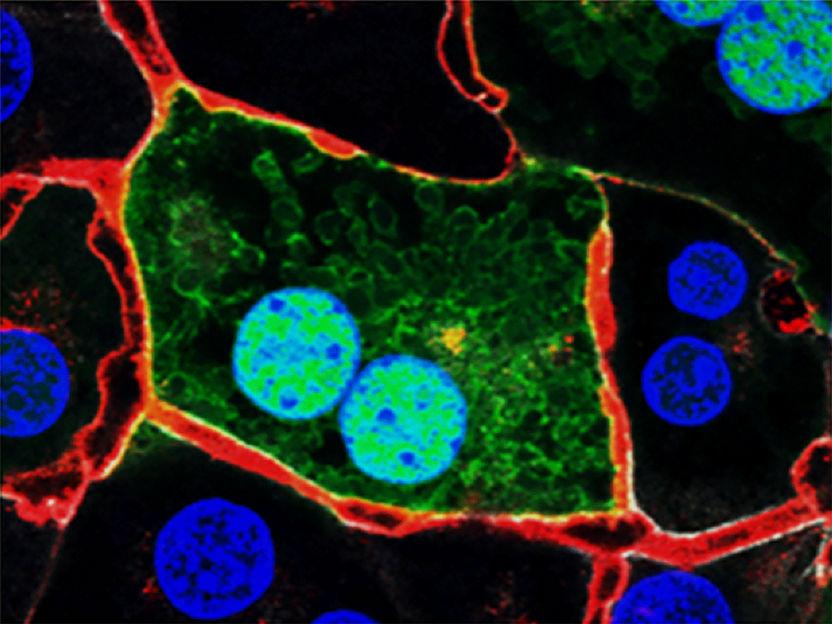
Leberzellen in der Kulturschale: In Grün der Zellkörper der Leberzelle, in Blau die Zellkerne, in Rot das Gallenkanälchen, in welches die Leberzelle Gallensalze und Fremdstoffe ausschüttet.
IfADo
Entgiftungszentrale und größtes Stoffwechselorgan: Die Leber übernimmt im Körper überlebenswichtige Aufgaben. Medikamente können das Organ schädigen. Diese Leberschäden sind die häufigste Ursache dafür, dass Studien mit Arzneimittelkandidaten abgebrochen und zugelassene Medikamente vom Markt genommen oder angepasst werden müssen. Zwar werden Medikamente zunächst in zahlreichen Tierversuchen getestet – doch ist es schwierig, das Risiko von Leberschäden für den Menschen in allen Fällen korrekt vorherzusagen. Testsysteme aus menschlichen Leberzellen in der Kulturschale (in vitro) könnten eine Alternative zu Tierversuchen in der toxikologischen Risikobewertung sein.
Allerdings können Forscher mit den bislang entwickelten Zellsystemen nicht immer treffsicher bestimmen, ob eine Substanz für den Menschen lebertoxisch oder harmlos ist. Bisher kann zudem in der Kulturschale nur gemessen werden, welche Konzentrationen einer Substanz die Zellen schädigt. Wissen möchte man aber, welche Menge ein Mensch zu sich nehmen kann, ohne dass es zu giftigen Wirkungen kommt, beziehungsweise ab welcher Dosis es gefährlich wird. Ein internationales Team unter Beteiligung des Leibniz-Instituts für Arbeitsforschung an der TU Dortmund (IfADo) hat nun eine Methode entwickelt, mit der die Leistungsfähigkeit von in-vitro-Testsystemen verbessert werden kann.
Messbare Anhaltspunkte für Optimierung des Testsystems
Um Testsysteme zu optimieren, kann an unterschiedlichen Stellschrauben gedreht werden. Denn es werden zahlreiche Parameter in der Zellkultur erfasst, zum Beispiel ob wichtige Funktionen gestört sind, wie die Produktion von Proteinen. Bislang konnte aber nicht zuverlässig beurteilt werden, welche Parameter in Zellsystemen am besten geeignet sind, um die Situation im Organismus abzubilden. Um das zu ändern, werden in der aktuellen Forschungsarbeit geeignete Maßzahlen vorgeschlagen: Mithilfe dieser mathematischen Methoden kann u.a. berechnet werden, welche der zahlreichen Parameter die beste Unterscheidung von lebertoxischen und nicht-toxischen Substanzen ermöglichen.
Die Forscher untersuchten zunächst 28 Trainingssubstanzen mittels im Labor kultivierten, menschlichen Leberzellen. Dabei war bekannt, ob die jeweilige Substanz für den Menschen lebertoxisch wirkt oder nicht, sowie bei welcher Dosis das Risiko einer Leberschädigung besteht. Die neuen mathematischen Methoden gaben Hinweise, wie eine Unterscheidung toxischer und nicht-toxischer Substanzen am zuverlässigsten gelingt. „Es zeigte sich beispielsweise, dass eine Inkubationszeit der Substanz auf die Zellen von 48 Stunden die besten Ergebnisse ermöglichte und dass nur bestimmte Gene für eine Beurteilung hilfreich waren“, erklärt Wiebke Albrecht, Studienautorin und IfADo-Doktorandin.
Mit diesem Wissen wurde das Testsystem optimiert: Alle lebertoxischen Substanzen wurden anschließend richtig erkannt. Bei zwei nicht toxischen Substanzen gab das System hingegen falschen Alarm. „Nach dieser Optimierungsphase haben wir weitere Stoffe getestet, alle wurden richtig eingestuft. Um herauszufinden, wie zuverlässig das System wirklich funktioniert, müssen wir noch mehr Substanzen untersuchen“, so Albrecht.
Das langfristige Ziel: Substanzen, die bereits in der Zellkultur bei beabsichtigten Therapiedosen toxisch wirken, würden vor einer weiteren Medikamentenentwicklung ausgeschlossen und müssten somit nicht mehr am Tier getestet werden.
Maschinelles Lernen unterstützt bei Datenverarbeitung
Mit dem Testsystem konnten die Forscher zudem für eine ihnen unbekannte Substanz bestimmen, welche Menge der Mensch täglich ohne erkennbares Gesundheitsrisiko aufnehmen kann. Ein Computerprogramm half aus der niedrigsten, in der Zellkultur toxischen Konzentration sowohl die Dosis, die oral aufgenommen beim Menschen Schaden anrichten werden, als auch die für Menschen verträgliche Aufnahmemenge zu berechnen. Dabei berücksichtigte das Programm, wie der menschliche Organismus eine Substanz verarbeitet.
„Wir sind mit unserem in-vitro-System auf ähnliche Aufnahmemengen gekommen, die bisher nur auf Basis von aufwendigen Fütterungsstudien an Tieren gewonnen werden“, sagt IfADo-Studienautor Tim Brecklinghaus. „Allerdings müssen wir viele weitere Substanzen untersuchen, um zu verstehen, wie exakt die neue Methode ist.“
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft
Meistgelesene News
Weitere News von unseren anderen Portalen
Verwandte Inhalte finden Sie in den Themenwelten
Themenwelt Zellkulturtechnik
Die Zellkulturtechnik ist ein zentraler Pfeiler in der biotechnologischen und pharmazeutischen Forschung und Entwicklung. Sie ermöglicht das Wachstum und die Pflege von Zellen unter kontrollierten Laborbedingungen und bietet so ein Fenster in die molekularen und zellulären Prozesse des Lebens.

Themenwelt Zellkulturtechnik
Die Zellkulturtechnik ist ein zentraler Pfeiler in der biotechnologischen und pharmazeutischen Forschung und Entwicklung. Sie ermöglicht das Wachstum und die Pflege von Zellen unter kontrollierten Laborbedingungen und bietet so ein Fenster in die molekularen und zellulären Prozesse des Lebens.

























































