Nanocarrier con reflejo de escape
Liberación de fármacos específicos para tumores mediante escape endosomal controlado
Anuncios
Los fármacos basados en proteínas deben transportarse al interior de las células de forma que se impida su degradación inmediata. Un nuevo enfoque pretende garantizar que sólo permanezcan intactos en determinadas células, como las cancerosas. En la revista Angewandte Chemie, un equipo de investigación japonés ha presentado un nanotransportador que puede "escapar" de los endosomas antes de que su carga se destruya allí. Esta capacidad de escape sólo se desencadena dentro de los endosomas de ciertas células tumorales.
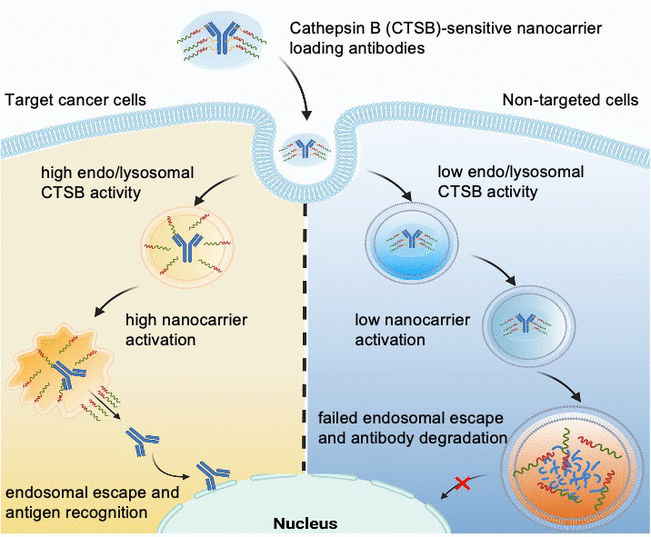
© Wiley-VCH
La captación de nanotransportadores en las células se produce por endocitosis: cuando un nanotransportador aterriza en la superficie celular, la membrana de la célula se pliega y lo encierra en una burbuja, llamada endosoma, que luego deriva hacia el interior celular. En su fase tardía, el endosoma se fusiona con lisosomas que contienen enzimas, formando un endolisosoma. Dentro de esta estructura, las enzimas descomponen tanto el material del organismo como el material extraño. Un fármaco proteínico sólo puede activarse si "escapa" del endolisosoma antes de descomponerse. Es lo que se conoce como "escape endosómico". Algunos nanotransportadores pueden abrir la membrana endo/lisosomal y, por tanto, tienen capacidad de escape endosomal.
Dirigido por Kazunori Kataoka y Horacio Cabral, el equipo pretende dar un paso más produciendo nanotransportadores cuyo escape endosómico sólo se desencadene cuando entren en células muy específicas, como las tumorales. Esto protegería a las células sanas. Los investigadores aprovechan el hecho de que los distintos tipos de células tienen actividades enzimáticas endolisomales muy diferentes. Por ejemplo, la actividad de la proteasa catepsina B (CTSB) es especialmente alta en las células cancerosas.
Con el uso de moléculas especiales de sonda de fluorescencia, el equipo de la Universidad de Tokio y el Instituto de Promoción Industrial de Kawasaki estudió inicialmente la actividad de la CTSB y la degradación de proteínas en los endosomas. Determinaron que en las células cancerosas con endosomas muy ácidos, la actividad de CTSB ya es muy alta en su fase inicial, mucho antes de que se produzca la degradación de las proteínas. Los investigadores aprovechan esta ventana temporal utilizando nanotransportadores cuya capacidad de escape endosomal es activada por el CTSB en las células cancerosas.
El equipo construyó nanotransportadores a base de poli(etilenglicol) con grupos diaminoetano capaces de "desgarrar" las membranas endo/lisosomales. Utilizando un enlazador, unieron anticuerpos para que actuaran como modelo de un fármaco proteico. El nanotransportador protege las "herramientas de desgarro" para que estén inactivas al principio. El enlazador está diseñado para ser dividido por el CTSB en los endolisosomas. Esto separa la carga del portador y activa las herramientas de desgarro. Éstas abren la membrana endolisosómica y liberan anticuerpos intactos en el interior de la célula, pero sólo en las células tumorales que tienen una actividad CTSB endosómica elevada.
Este método podría representar una nueva estrategia para la liberación celular específica de fármacos a través de nanotransportadores sensibles a estímulos con escape endosomal controlado.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.