Experimenteller monoklonaler Antikörper zur Behandlung von Ebola ist bei Erwachsenen sicher
Anzeigen
Die experimentelle Ebola-Behandlung mAb114 ist sicher, gut verträglich und einfach zu verabreichen, wie die Ergebnisse einer klinischen Frühphasenstudie zeigen. Achtzehn gesunde Erwachsene erhielten den monoklonalen Antikörper als Teil einer klinischen Phase-1-Studie, die im Mai 2018 am National Institutes of Health (NIH) Clinical Center in Bethesda, Maryland, begann. Das National Institute of Allergy and Infectious Diseases (NIAID) Vaccine Research Center (VRC), Teil des NIH, entwickelte die Prüfbehandlung und führte und sponserte die klinische Studie.
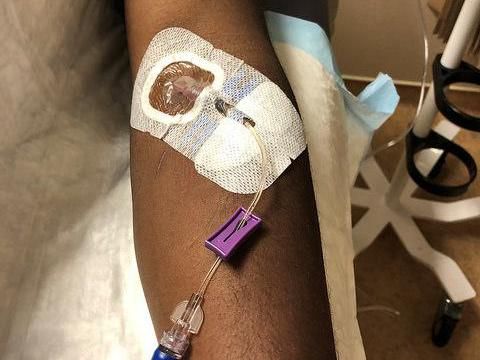
Ein gesunder Freiwilliger erhält eine intravenöse Infusion von mAb114 - eine experimentelle Behandlung der Ebola-Virus-Krankheit - in einer klinischen Phase-1-Studie im NIH Clinical Center in Bethesda, Md.
NIAID
Die Behandlung wird derzeit Ebola-Patienten in der Demokratischen Republik Kongo (DRK) unter einvernehmlichem Einsatz und im Rahmen einer klinischen Phase-2/3-Studie mit mehreren Studienbehandlungen angeboten. mAb114, ein einzelner monoklonaler Antikörper, bindet an die Kernrezeptorbindungsdomäne des zairischen Ebolavirus-Oberflächenproteins und verhindert, dass das Virus menschliche Zellen infiziert. Wissenschaftler isolierten den Antikörper aus einem menschlichen Überlebenden des Ebola-Ausbruchs von 1995 in Kikwit, DRK. Frühere Studien zeigten, dass mAb114 Affen vor der tödlichen Ebola-Virus-Krankheit schützen kann, wenn es erst fünf Tage nach der Infektion gegeben wird.
Die Teilnehmer der klinischen Phase-1-Studie erhielten eine einzige intravenöse Infusion von mAb114, die über etwa 30 Minuten verabreicht wurde. Drei Teilnehmer erhielten eine Dosis von 5 Milligramm (mg)/Kilogramm (kg), fünf Teilnehmer erhielten eine Dosis von 25 mg/kg und 10 Teilnehmer eine Dosis von 50 mg/kg. Alle Infusionen waren gut verträglich. Vier Teilnehmer berichteten von leichten Nebenwirkungen wie Unbehagen, Muskel- oder Gelenkschmerzen, Kopfschmerzen, Übelkeit und Schüttelfrost in den drei Tagen nach der Infusion.
Wie erwartet, stiegen die Werte von mAb114 im Blut mit zunehmender Dosierung. Die Forscher beobachteten auch relativ einheitliche Niveaus der Absorption, Verteilung und Eliminierung von mAb114 unter den Teilnehmern.
Die Autoren stellen mehrere Vorteile für den Einsatz von mAb114 in einer Ausbruchssituation fest, darunter die einfache und schnelle Verabreichung und die Formulierung als gefriergetrocknetes Pulver, das keine Lagerung im Gefrierschrank erfordert. Das Pulver wird mit sterilem Wasser rekonstituiert und der Kochsalzlösung zur Verabreichung zugesetzt.
Zusätzlich zur laufenden klinischen Phase-2/3-Studie mit mAb114 in der DRK plant das VRC, eine weitere Phase-1-Studie mit der Prüfbehandlung in Afrika zu starten.
Originalveröffentlichung
Martin R Gaudinski et al.; "Safety, tolerability, pharmacokinetics, and immunogenicity of the therapeutic monoclonal antibody mAb114 targeting Ebola virus glycoprotein (VRC 608): an open-label phase 1 study"; The Lancet; 2019
Weitere News aus dem Ressort Wissenschaft
Meistgelesene News
Weitere News von unseren anderen Portalen
Verwandte Inhalte finden Sie in den Themenwelten
Themenwelt Antikörper
Antikörper sind spezialisierte Moleküle unseres Immunsystems, die gezielt Krankheitserreger oder körperfremde Substanzen erkennen und neutralisieren können. Die Antikörperforschung in Biotech und Pharma hat dieses natürliche Abwehrpotenzial erkannt und arbeitet intensiv daran, es therapeutisch nutzbar zu machen. Von monoklonalen Antikörpern, die gegen Krebs oder Autoimmunerkrankungen eingesetzt werden, bis hin zu Antikörper-Drug-Konjugaten, die Medikamente gezielt zu Krankheitszellen transportieren – die Möglichkeiten sind enorm.
Themenwelt Antikörper
Antikörper sind spezialisierte Moleküle unseres Immunsystems, die gezielt Krankheitserreger oder körperfremde Substanzen erkennen und neutralisieren können. Die Antikörperforschung in Biotech und Pharma hat dieses natürliche Abwehrpotenzial erkannt und arbeitet intensiv daran, es therapeutisch nutzbar zu machen. Von monoklonalen Antikörpern, die gegen Krebs oder Autoimmunerkrankungen eingesetzt werden, bis hin zu Antikörper-Drug-Konjugaten, die Medikamente gezielt zu Krankheitszellen transportieren – die Möglichkeiten sind enorm.




























































