Medikamententests in Europa werden leichter
Anzeigen
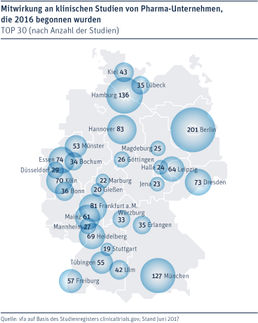
(dpa-AFX) Pharma-Firmen sollen künftig leichter grenzüberschreitende Medikamententests in Europa machen können. Entsprechende Regeln beschlossen die EU-Agrarminister am Montag in Luxemburg. Damit soll Europa attraktiver als Standort für klinische Studien werden, also Medikamententests an Menschen. Zwischen 2007 und 2011 war die Zahl der in der Europäischen Union durchgeführten Studien laut EU um ein Viertel gesunken. Künftig müssen Pharmaunternehmen länderübergreifende Tests zum Beispiel nur noch in einem EU-Land anmelden.
Die Agrarminister sind zwar eigentlich nicht für das Thema zuständig. Diesen rein formalen Beschluss konnten aber auch fachfremde Minister treffen, weil sich die EU-Staaten zuvor bereits mit dem Europaparlament geeinigt hatten.
Die Vorschläge waren zeitweise sehr umstritten gewesen. Insbesondere in Deutschland hatte es Befürchtungen gegeben, der Spielraum für Ethikkommissionen könne schwinden. Solche Gremien des Bundes und der Länder müssen die Studien in Deutschland genehmigen. Dafür haben sie nach den neuen Regeln nun 60 Tage Zeit - die Bedenken der Bundesregierung sind damit nach Aussagen von Diplomaten ausgeräumt. Die neuen Regeln sollen nach Auskunft des EU-Parlaments spätestens 2016 in Kraft treten.
Meistgelesene News
Weitere News aus dem Ressort Forschung & Entwicklung

Holen Sie sich die Life-Science-Branche in Ihren Posteingang
Mit dem Absenden des Formulars willigen Sie ein, dass Ihnen die LUMITOS AG den oder die oben ausgewählten Newsletter per E-Mail zusendet. Ihre Daten werden nicht an Dritte weitergegeben. Die Speicherung und Verarbeitung Ihrer Daten durch die LUMITOS AG erfolgt auf Basis unserer Datenschutzerklärung. LUMITOS darf Sie zum Zwecke der Werbung oder der Markt- und Meinungsforschung per E-Mail kontaktieren. Ihre Einwilligung können Sie jederzeit ohne Angabe von Gründen gegenüber der LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlin oder per E-Mail unter widerruf@lumitos.com mit Wirkung für die Zukunft widerrufen. Zudem ist in jeder E-Mail ein Link zur Abbestellung des entsprechenden Newsletters enthalten.