Organisiertes Chaos im Enzymkomplex: überraschende Einsichten und neue Angriffspunkte
Geordnet läuft es in der Zelle meist nicht ab
Anzeigen
Für Eiweißmoleküle, die Substanzen für den Stoffwechsel umwandeln, ist es oft entscheidend, wie sie mit den anderen Komponenten ihres Stoffwechselwegs interagieren. Wissenschaftler vom Max-Planck-Institut für Entwicklungsbiologie in Tübingen haben einen natürlichen Enzymkomplex untersucht, der zehn Enzyme mit fünf unterschiedlichen Aktivitäten zusammenfasst. Das Ergebnis: Die Struktur ist erstaunlich kompakt und bietet den einzelnen Enzymen dennoch die maximale Flexibilität. Diese Architektur eröffnet neue Perspektiven für die Wirkstoffforschung. Ihre Ergebnisse veröffentlichen die Wissenschaftler jetzt in nature chemical biology.
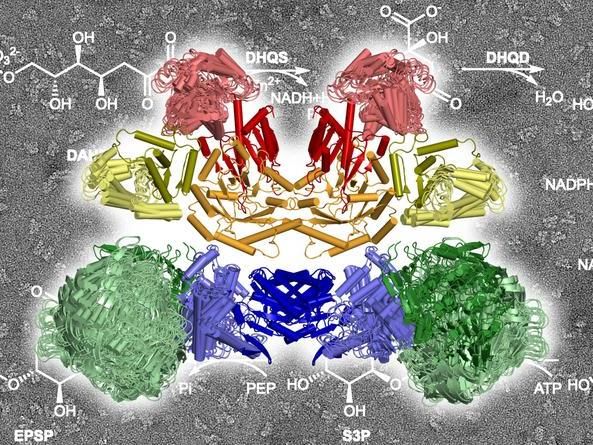
Die zehn Enzymkomponenten im AROM Komplex bei der Arbeit. Sie katalysieren die im Hintergrund skizzierten chemischen Reaktionen.
Marcus Hartmann
Stoffwechselwege sehen im Lehrbuch immer ein wenig nach Fließbandarbeit aus. Wie auf einer Perlenschnur reiht sich in den Abbildungen ein Enzym an das andere. Zwischenprodukte werden abtransportiert oder von einer Station an die andere weitergereicht. „So geordnet läuft es in der Zelle jedoch meist nicht ab“, sagt Marcus Hartmann, Gruppenleiter am Max-Planck-Institut für Entwicklungsbiologie. „Die einzelnen Komponenten eines Stoffwechselwegs können sich an sehr unterschiedlichen Stellen in der Zelle befinden, und in den meisten Fällen verstehen wir nicht, ob und wie sie sich zu geordneten Strukturen zusammenfinden.“
Wer die Funktion und Dynamik von Stoffwechselwegen verstehen will, muss sich deshalb mit dem Zusammenspiel und den Hierarchien der einzelnen Komponenten auseinander setzen. Nur so lässt sich das Gesamtbild erfassen.
Unter diesem Aspekt haben Hartmann und sein Team einen sonst gut untersuchten Stoffwechselweg unter die Lupe genommen: Den Shikimat-Weg. Dabei handelt es sich um einen Stoffwechselweg, der in Pflanzen und Mikroorganismen einschließlich pathogener Pilze und parasitärer Protisten wie den Erregern von Toxoplasmose oder Malaria vorkommt. Seine Aufgabe ist es unter anderem, Vorstufen der für Tiere und Menschen essentiellen Aminosäuren Phenylalanin, Tyrosin und Tryptophan zu synthetisieren. Traurige Berühmtheit erlangte der Stoffwechselweg dadurch, dass das Herbizid Glyphosat hier eingreift.
Das Interessante für die Tübinger Forscher: Während in Pflanzen- und Bakterienzellen die meisten Enzyme des Shikimat-Wegs einzeln vorliegen, sind bei Pilzen und Protisten fünf der sieben Komponenten in einem großen Enzymkomplex zusammengelagert, AROM genannt. „Wir wollten wissen, wie dieser große Komplex aufgebaut ist, und welchen Vorteil diese Organismen aus ihm ziehen“, sagt Hartmann. „Ob die Katalyse im Komplex beispielsweise effizienter ist.“
Den Wissenschaftlern gelang es, eine Kristallstruktur des gesamten Proteinkomplexes aufzuklären.
Dabei zeigte sich, dass sich die fünf Enzymkomponenten in doppelter Ausführung zu einem kompakten Gebilde mit insgesamt zehn Komponenten auf engstem Raum zusammenfügen. „Eine derart kompakte Architektur hatten wir nicht erwartet“, sagt Hartmann. „Viele Enzyme des Shikimat-Wegs brauchen für ihre Arbeit recht viel Bewegungsfreiheit.“
Dank einer ausgefeilten Architektur ist der verfügbare Platz im AROM Komplex jedoch ausreichend. Zwar hatten die Wissenschaftler mit der Kristallstruktur lediglich eine Momentaufnahme zur Verfügung. „Aber die einzelnen Komponenten sind so gut untersucht, dass wir im Computermodell simulieren können, wie sie sich innerhalb des Komplexes bewegen“, erklärt der Wissenschaftler. Dabei stellte sich heraus, dass der notwendige Bewegungsfreiraum für die einzelnen Enzyme so zugeschnitten ist, dass sie sich unabhängig voneinander bewegen können, ohne mit den anderen Komponenten zu kollidieren. „Tatsächlich haben wir keine Hinweise für eine Koordination der einzelnen Enzymbewegungen“, so Harshul Arora Verasztó, Erstautorin der Studie. „Es ist eher eine Form von organisiertem Chaos.“
Bei weiteren Untersuchungen stellte sich heraus, dass die bloße Zusammenlagerung der Enzyme zum AROM Komplex alleine keinen katalytischen Vorteil für den Shikimat-Weg der Pilze bietet – zumindest auf der Grundlage bisheriger Daten. „Ein Vergleich unter Laborbedingungen hat ergeben, dass der Durchsatz im Komplex nicht höher ist, als wenn die Komponenten einzeln vorliegen“, so Hartmann. „Gerade für Biotechnologen, die versuchen, durch Zusammenlagerung von Enzymen die Effizienz katalytischer Kaskaden zu erhöhen, mag das eine überraschende Nachricht sein.“
Die Ergebnisse der Tübinger Wissenschaftler dienen zunächst einmal der Grundlagenforschung – dem Erkenntnisgewinn darüber, wie Enzyme und insbesondere Enzymkomplexe in Stoffwechselwegen zusammenspielen. Gleichzeitig aber eröffnen sie völlig neue Perspektiven für die Wirkstoffforschung. „Die enge Anordnung der besonders flexiblen Enzymkomponenten im AROM Komplex ist hierfür besonders interessant“, erläutert Hartmann. Meist greifen Wirkstoffe an den katalytischen Zentren an, also an der Stelle, an der Enzyme Substanzen umwandeln. „Für den AROM Komplex wäre es denkbar, nach Substanzen zu suchen, die sich wie ein Keil zwischen die Komponenten schieben und sie so blockieren.“ Gelänge das, ließen sich Hemmstoffe entwickeln, die ausschließlich bei Pilzen oder Protisten, etwa den Erregern von Toxoplasmose oder Malaria, wirken, den Shikimat-Weg von Pflanzen und Bakterien jedoch nicht beeinträchtigen.

























































