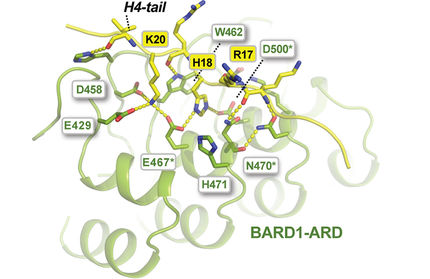
Neuer Reparaturmechanismus für alkoholinduzierte DNA-Schäden entdeckt
Wissen unterstreicht Zusammenhang zwischen Alkoholkonsum und Krebs
Anzeigen
Forscher des Hubrecht Institute (KNAW) in Utrecht, Niederlande, und des MRC Laboratory of Molecular Biology in Cambridge, Vereinigtes Königreich, haben eine neue Art und Weise entdeckt, wie der menschliche Körper DNA-Schäden, die durch ein Abbauprodukt von Alkohol verursacht werden, repariert. Dieses Wissen unterstreicht den Zusammenhang zwischen Alkoholkonsum und Krebs. Die Forschungsgruppen von Puck Knipscheer und Ketan J. Patel arbeiteten gemeinsam an dieser Studie und veröffentlichten die Ergebnisse am 4. März in Nature.
Künstlerischer Eindruck einem alkoholinduzierten "interstrand crosslink" (ICL). Der ICL ist die gelbe Verbindung zwischen den beiden DNA-Strängen, die sie zusammenhalten.
Image copyright: MRC Laboratory of Molecular Biology or MRC LMB
Unsere DNA ist ein tägliches Ziel für eine Flut von Schäden, die durch Strahlung oder toxische Substanzen wie Alkohol verursacht werden. Bei der Verstoffwechselung von Alkohol wird Acetaldehyd gebildet. Acetaldehyd verursacht eine gefährliche Art von DNA-Schäden - interstrand crosslink (ICL) - die die beiden DNA-Stränge zusammenhält. Dadurch behindert es die Zellteilung und die Proteinproduktion. Letztendlich kann eine Anhäufung von ICL-Schäden zum Zelltod und zu Krebs führen.
Abwehr von DNA-Schäden
Glücklicherweise verfügt jede Zelle in unserem Körper über ein Instrumentarium, mit dem sie diese Art von Schäden an der DNA reparieren kann. Die erste Verteidigungslinie gegen die durch Acetaldehyd verursachten ICLs ist das ALDH2-Enzym, das Acetaldehyd weitgehend abbaut, bevor es Schaden anrichtet. Doch nicht jeder profitiert von diesem Enzym - etwa die Hälfte der asiatischen Bevölkerung, weltweit mehr als 2 Milliarden Menschen, besitzt eine Mutation in dem für dieses Enzym kodierenden Gen. Da sie nicht in der Lage sind, Acetaldehyd abzubauen, sind sie anfälliger für alkoholbedingten Krebs.
Neue Verteidigungslinie
Wissenschaftler aus den Gruppen von Puck Knipscheer (Hubrecht-Institut) und Ketan J. Patel (MRC Laboratory of Molecular Biology) untersuchten die zweite Verteidigungslinie gegen alkoholinduzierte ICLs: Mechanismen, die den Schaden von der DNA entfernen. Die Forscher untersuchten diese Mechanismen anhand von Proteinextrakten aus den Eiern des Krallenfrosches (Xenopus laevis), einem in der biologischen Forschung häufig verwendeten Tiermodell. Indem sie diese Extrakte zur Reparatur einer durch Acetaldehyd gebildeten ICL nutzten, entdeckten sie zwei Mechanismen, die ICL-Schäden reparieren: den bisher bekannten Fanconi-Anämie (FA)-Weg und einen neuartigen, schnelleren Weg. Diese beiden Mechanismen unterscheiden sich voneinander: Beim FA-Weg wird die DNA geschnitten, um die ICL zu entfernen, während die Enzyme des neu entdeckten Weges die Vernetzung selbst schneiden.
Spezifische Schäden
Mit dieser Forschung bieten die Wissenschaftler einen mechanistischen Einblick in den Prozess der Reparatur von DNA-Schäden. Wir wissen jetzt, dass der Körper ICLs in der DNA auf vielfältige Weise reparieren kann", sagt Co-Leitautor Puck Knipscheer. Sie glaubt, dass diese Art von Forschung zu einem besseren Verständnis der Behandlung alkoholbedingter Krebsarten führen kann. Doch bevor wir das tun können, müssen wir zunächst genau wissen, wie dieser neuartige Mechanismus für die Reparatur von ICLs funktioniert".
Hinweis: Dieser Artikel wurde mit einem Computersystem ohne menschlichen Eingriff übersetzt. LUMITOS bietet diese automatischen Übersetzungen an, um eine größere Bandbreite an aktuellen Nachrichten zu präsentieren. Da dieser Artikel mit automatischer Übersetzung übersetzt wurde, ist es möglich, dass er Fehler im Vokabular, in der Syntax oder in der Grammatik enthält. Den ursprünglichen Artikel in Englisch finden Sie hier.