Attaque par les chemins de traverse
Nouvelles perspectives pour le traitement des tumeurs, des maladies auto-immunes ou des états inflammatoires chroniques
Annonces
L'augmentation de la prolifération cellulaire est une caractéristique essentielle de maladies telles que le cancer. Une équipe de recherche de l'université de Würzburg et de deux instituts Leibniz a maintenant réussi à influencer indirectement ce processus.
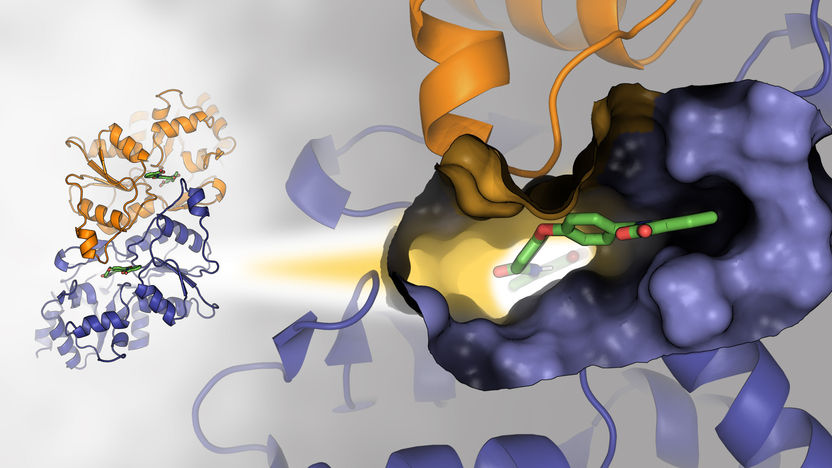
Structure dimérique de la phosphatase phosphoglycolate. La section agrandie à droite montre la poche de liaison au ligand en complexe avec la petite molécule inhibitrice CP1.
Natalia Yuan-Chen
Aussi différents que soient les cancers ou les maladies auto-immunes comme la sclérose en plaques, la polyarthrite rhumatoïde ou le psoriasis, ils ont tous une caractéristique commune : ils s'accompagnent d'une prolifération cellulaire accrue. En conséquence, les cellules malades doivent augmenter vigoureusement leur production de blocs de construction moléculaires, ce qui est inévitablement lié à une demande énergétique fortement accrue.
Par conséquent, le contrôle de la production cellulaire des éléments constitutifs de la synthèse des macromolécules et de l'homéostasie énergétique est une stratégie importante pour le développement de nouveaux médicaments contre ces maladies. Une équipe de scientifiques de la Julius-Maximilians-Universität Würzburg (JMU) a réussi à faire un pas important dans cette direction. En utilisant une cible pharmacologique jusqu'alors inexploitée, ils ont pu influencer ces processus cellulaires.
Publication dans Nature Communications
L'auteur principal de cette étude, qui vient d'être publiée dans la revue Nature Communications, est Antje Gohla, professeur de pharmacologie biochimique au département de pharmacologie et de toxicologie de la JMU. Des équipes du Centre Rudolf Virchow (RVZ) pour l'imagerie intégrative et translationnelle, du Biocentre et de l'Institut de pharmacie de la JMU, ainsi que de l'Institut Leibniz de pharmacologie moléculaire-FMP Berlin et de l'Institut Leibniz des sciences analytiques-ISAS Dortmund ont également participé à ces travaux.
"Une cible typique pour le développement de nouveaux médicaments est la préférence de nombreuses cellules pour le sucre sous forme de glucose comme l'un des principaux fournisseurs d'énergie et d'éléments constitutifs, car le glucose est une molécule polyvalente, quasi universelle, dans le métabolisme", explique Antje Gohla. Cependant, le succès thérapeutique de cette stratégie a été limité jusqu'à présent.
Un aspect important du métabolisme humain a été longtemps ignoré par les chercheurs : Parallèlement aux voies bien connues de dégradation et de conversion du glucose, de nombreux "processus de réparation" se déroulent en arrière-plan, et ces processus sont essentiels au bon fonctionnement du métabolisme", explique Mme Gohla.
Inhibition d'importants processus de réparation
L'équipe de recherche s'est concentrée sur ces processus dans son étude. Plus précisément, les scientifiques ont cherché à savoir si ces processus de réparation pouvaient servir de cibles médicamenteuses. La réponse est claire : "Pour la première fois, nous avons pu identifier un composé qui inhibe sélectivement l'activité de la phosphoglycolate phosphatase, une enzyme de réparation importante dans le métabolisme du sucre", explique le pharmacologue. Dans le tube à essai, le composé bloque effectivement la prolifération des cellules tumorales.
Les phosphatases sont généralement considérées comme des cibles pharmacologiques difficiles. L'équipe est donc particulièrement heureuse d'avoir réussi à identifier et à caractériser un inhibiteur de phosphatase structurellement nouveau.
Soutien important de la biologie structurale
Dans cette recherche, Mme Gohla a reçu le soutien d'experts en criblage à haut débit, en métabolomique, en biologie structurale et en chimie médicinale. Avec leur aide, dit-elle, il a été possible d'élucider en détail le mécanisme d'action moléculaire d'un inhibiteur de la phosphoglycolate phosphatase.
Le professeur Hermann Schindelin, du Centre Rudolf Virchow, a apporté une contribution importante en élucidant la structure tridimensionnelle de la phosphoglycolate phosphatase en complexe avec l'inhibiteur à l'aide de l'analyse de la structure cristalline aux rayons X. "La visualisation du médicament dans la structure tridimensionnelle de l'inhibiteur a permis d'obtenir une meilleure compréhension de l'action de l'inhibiteur. "La visualisation du médicament à proximité spatiale du site actif explique non seulement les données cinétiques de l'enzyme, mais fournit surtout un point de départ pour le développement futur d'une nouvelle génération d'inhibiteurs aux propriétés de liaison améliorées", explique le biologiste structurel.
Perspectives de nouvelles thérapies
Globalement, les résultats montrent qu'il existe encore des cibles pharmacologiques inexploitées dans le métabolisme cellulaire des sucres. Alors que la recherche s'est jusqu'à présent concentrée sur les principales voies métaboliques du glucose, qui sont également vitales pour de nombreuses cellules saines, cette nouvelle approche cible le besoin accru des cellules associées à la maladie pour les processus de réparation. "Le concept consiste à cibler pharmacologiquement les besoins accrus des cellules tumorales ou des cellules immunitaires mal orientées en matière de processus de réparation métabolique, de sorte que ces cellules s'empoisonnent en accumulant des sous-produits métaboliques toxiques", explique Gohla.
Cependant, il reste encore un long chemin à parcourir avant que de tels composés puissent être utilisés comme médicaments. Les auteurs de l'étude espèrent néanmoins que, sur la base de leurs découvertes fondamentales, de nouvelles perspectives s'ouvriront à l'avenir pour le traitement des tumeurs, des maladies auto-immunes ou des états inflammatoires chroniques.
Note: Cet article a été traduit à l'aide d'un système informatique sans intervention humaine. LUMITOS propose ces traductions automatiques pour présenter un plus large éventail d'actualités. Comme cet article a été traduit avec traduction automatique, il est possible qu'il contienne des erreurs de vocabulaire, de syntaxe ou de grammaire. L'article original dans Anglais peut être trouvé ici.
Publication originale
Glycolytic flux control by drugging phosphoglycolate phosphatase. Elisabeth Jeanclos, Jan Schlötzer, Kerstin Hadamek, Natalia Yuan-Chen, Mohammad Alwahsh, Robert Hollmann, Stefanie Fratz, Dilan Yesilyurt-Gerhards, Tina Frankenbach, Daria Engelmann, Angelika Keller, Alexandra Kaestner, Werner Schmitz, Martin Neuenschwander, Roland Hergenröder, Christoph Sotriffer, Jens Peter von Kries, Hermann Schindelin, Antje Gohla. Nature Communications; 2022












































