El comienzo de la vida: El embrión temprano está en el asiento del conductor
Los blastoides resolvieron un dilema de "huevo o gallina"
Anuncios
A menudo se piensa que el embrión temprano es frágil y necesita apoyo. Sin embargo, en las primeras fases del desarrollo, tiene el poder de alimentar a la futura placenta e instruir al útero para que pueda anidar. Utilizando "blastoides", modelos de embriones in vitro formados con células madre, el laboratorio de Nicolas Rivron en el IMBA demostró que las primeras señales moleculares que inducen el desarrollo de la placenta y preparan el útero proceden del propio embrión. Los hallazgos, publicados ahora en Cell Stem Cell, podrían contribuir a una mejor comprensión de la fertilidad humana.
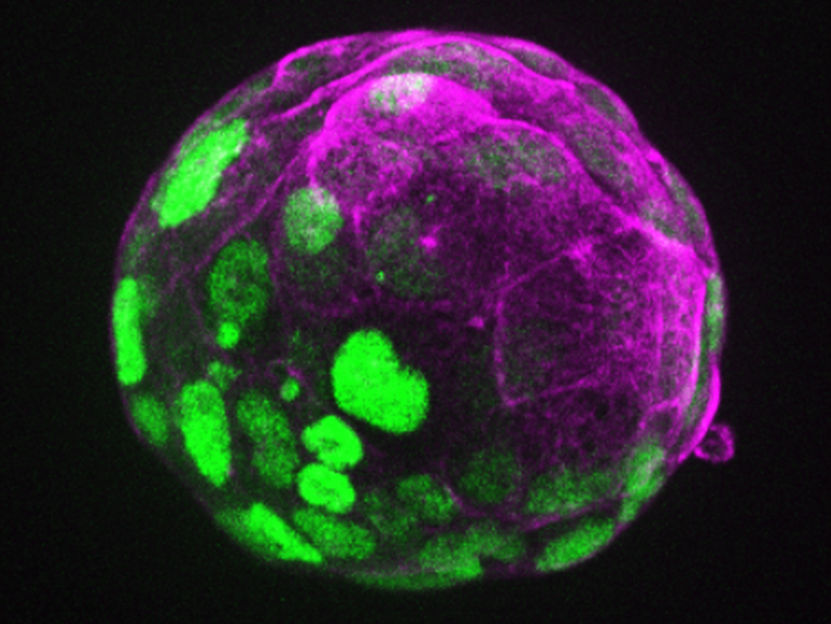
Un eje de expresión de proteínas en un blastoide de ratón
©Rivron/CellStemCell/IMBA
¿Quién cuida a quién en el inicio de la vida?
La placenta y el útero nutren y albergan al feto. Pero la situación en la fase más temprana del desarrollo, cuando el blastocisto aún flota en el útero, no estaba clara hasta ahora. Ahora, el grupo de investigación de Nicolas Rivron en el IMBA (Instituto de Biotecnología Molecular de la Academia Austriaca de Ciencias) ha descubierto los principios básicos del desarrollo temprano utilizando blastoides.
Los blastoides son modelos in vitro del blastocisto, el embrión de los mamíferos en los primeros días tras la fecundación. Estos modelos de embriones fueron desarrollados primero por el laboratorio de Rivron a partir de células madre de ratón (Nature, 2018) y luego de células madre humanas (Nature, 2021). Los blastoides proporcionan una alternativa ética al uso de embriones para la investigación y, lo que es más importante, permiten realizar múltiples descubrimientos.
Ahora, los blastoides resolvieron el dilema del "huevo o la gallina". Utilizando blastoides de ratón, los investigadores descubrieron que la parte embrionaria temprana (~10 células) ordena la formación de la futura parte placentaria (~100 células) y el cambio de los tejidos uterinos. "De este modo, el embrión invierte en su propio futuro: promueve la formación de los tejidos que pronto se encargarán de su desarrollo. El embrión tiene el control, instruyendo la creación de un entorno de apoyo", afirma Nicolas Rivron.
En efecto, el equipo descubrió varias moléculas segregadas por las pocas células a partir de las cuales se desarrolla el feto, los epiblasto. Observaron que estas moléculas indican a otras células, los trofoblastos que más tarde formarán la placenta, que se autorrenoven y proliferen, dos propiedades de las células madre que son esenciales para que la placenta crezca.
El equipo también descubrió que estas moléculas inducen a los trofoblastos a secretar otras dos moléculas, WNT6 y WNT7B. WNT6 y WNT7B indican al útero que envuelva el blastocisto. "Otros investigadores ya habían visto que las moléculas WNT están implicadas en la reacción uterina. Ahora demostramos que estas señales son WNT6/7B y que son producidas por los trofoblastos del blastocisto para notificar al útero que reaccione. La relevancia podría ser alta porque hemos comprobado que estas dos moléculas también son expresadas por los trofoblastos del blastocisto humano", afirma Nicolas Rivron.
El equipo hizo sus descubrimientos examinando en parte el grado de implantación de los blastocitos de ratón en un modelo de implantación in vivo. "Me sorprendió mucho la eficacia con la que nuestros blastoides se implantaron en el útero. Y al cambiar las propiedades de los trofoblastos dentro de los blastoides, incluidos los niveles de secreción de WNT6/7B, pudimos cambiar claramente el tamaño del capullo uterino", dice el coautor Jinwoo Seong, becario postdoctoral en el laboratorio de Rivron, que realizó estos experimentos.
Dado que la implantación es el cuello de botella en los embarazos humanos -alrededor del 50% de los embarazos fracasan en ese momento- y que WNT6 y WNT7B también están presentes en los blastocitos humanos, estos hallazgos podrían explicar por qué, a veces, las cosas van mal. "Actualmente estamos repitiendo estos experimentos con blastocitos humanos y células uterinas, todo ello en una placa, para estimar la conservación de estos principios básicos del desarrollo. Estos descubrimientos podrían contribuir, en última instancia, a mejorar los procedimientos de fecundación in vitro y a desarrollar medicamentos para la fertilidad y anticonceptivos", afirma Nicolas Rivron.
El trabajo en equipo también fue impulsado por otros dos coprimeros autores: Javier Frías Aldeguer, antiguo estudiante de doctorado, y Viktoria Holzmann, actual estudiante de doctorado. "Comprender estos principios fundamentales del desarrollo embrionario contribuirá, en última instancia, a que las mujeres puedan controlar mejor su fertilidad, lo que no sólo mejoraría la planificación familiar, sino que también repercutiría en la igualdad de género en la sociedad", afirma Viktoria Holzmann.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.