G-Proteine: Schaltmechanismus zeigt Wege zu neuen Medikamenten
Anzeigen
G-Proteine sind molekulare Schalter an der Innenwand der Zelle, die wichtige Signale ins Zellinnere weiter leiten. Die mit ihnen verbundenen Rezeptoren sind Ziel eines Großteils aller Medikamente. Nun konnten Wissenschaftler der Technischen Universität München (TUM) erstmals nachvollziehen, wie sich die einzelnen Aminosäuren im G-Protein während des Schaltprozesses genau bewegen. Die entdeckten Mechanismen geben Hinweise für das Design neuer Wirkstoffe.

Prof. Franz Hagn Prof. Franz Hagn mit einer Kernspinresonanzspektroskopie-Probe am Supraleitenden Magneten mit 950 MHz Feldstärke.
Uli Benz / TUM
Der menschliche Körper ähnelt einem großen Teamprojekt. Millionen von Zellen, strukturiert in Geweben und Organen, übernehmen unterschiedlichste Aufgaben, arbeiten sich zu, koordinieren und regulieren sich gegenseitig. Damit diese intensive Zusammenarbeit funktioniert, müssen die Zellen Informationen miteinander austauschen. Bestimmte Proteine regulieren diese Kommunikation. Als "Boten" leiten sie von außen ankommende Signale ins Zellinnere weiter.
Ein Bote und sein Rezeptor im Fokus der Pharmaindustrie
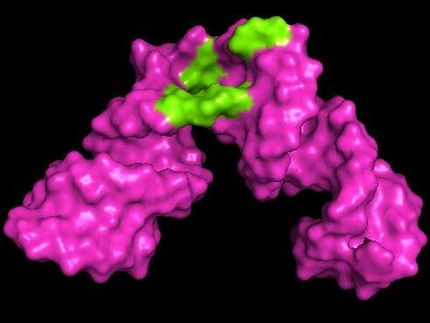
Eine wichtige Klasse solcher Botenproteine sind die sogenannten G-Proteine. Sie fungieren als kleine molekulare Schalter: Bindet ein Signalstoff an den G-Protein gekoppelten Rezeptor, wird ein Teil des G-Proteins, die sogenannte Alpha-Untereinheit, "eingeschaltet". Sie löst sich vom Rezeptor und den anderen Untereinheiten ab und aktiviert weitere Proteine.
Es ist der erste Schritt einer Signalkaskade, an deren Ende die gewünschte Reaktion steht. Bei einer ganzen Reihe von Krankheiten ist die Regulation dieser Signalkaskade gestört. Daher greifen über 30 Prozent aller hergestellten Medikamente an den mit den G-Proteinen gekoppelten Rezeptoren an, darunter Betablocker, Medikamente gegen Bluthochdruck und Psychopharmaka. Auch Wirkstoffe, die direkt auf die G-Proteine wirken, sind denkbar.
Mehr als nur eine Momentaufnahme – wie genau wird der Schalter betätigt?
Nun haben Wissenschaftler um Franz Hagn, Professor für Strukturelle Membranbiochemie der TU München herausgefunden, was genau in der Alpha-Untereinheit beim "Umlegen" des Schalters vor sich geht.
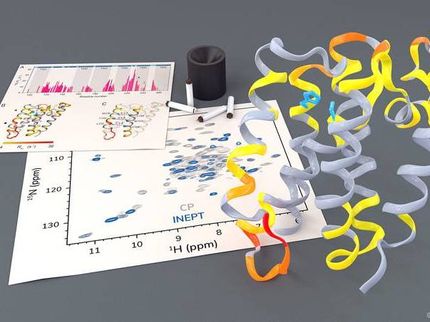
Mit Hilfe der Kernmagnetischen-Resonanzspektroskopie klärten sie Schritt für Schritt auf, wie sich die einzelnen Aminosäuren in der Alpha-Untereinheit bei der Aktivierung bewegen. "Herstellern von Medikamenten könnte dieses Wissen helfen Wirkstoffe zu kreieren, die auf genau die einzelnen Schritte zugeschnitten sind, was bis dato sehr schwierig ist", erläutert Franz Hagn.
Erstmals G-Proteine in natürlichem Zustand untersucht
In ihrer Arbeit gelang es den Forschern um Hagn zum ersten Mal, die Bewegungen in der Alpha-Untereinheit des G-Proteins in ihrer natürlichen Umgebung, also an die Zellmembran gebunden, zu betrachten. Dies ist sehr schwierig, da Membranproteine nicht löslich sind, dies aber für die spektroskopische Untersuchung notwendig ist.
Um das G-Protein dennoch erforschen zu können, entwickelten die Wissenschaftler kleine Lipid-Doppelmembran-Stücke, bei denen Lipid-bindende Proteine die wasserabweisenden Kanten abschirmen. In diese sogenannten Phospholipid-Nanodisks setzten sie dann den G-Protein gekoppelten Rezeptor ein und untersuchten die Interaktion mit dem löslichen G-Protein.
Die Wissenschaftler fanden heraus, dass die Rezeptor-gebundene Form der Alpha-Untereinheit, in der Stellung "Aus" sehr offen vorliegt. Bindet das aktivierende Guanosintriphosphat (GTP) an das Protein, klappt es zu und der Schalter wird aktiv. Nun liegen die Teile der Untereinheit fest aneinander gelagert vor. Der Komplex ist starr und kaum mehr veränderlich, was für die Aktivierung weiterer Signalproteine essenziell ist.
Voraussetzungen für künftiges Wirkstoffdesign
Noch liegt die Entwicklung eines direkt an G-Proteinen angreifenden Medikaments in weiter Ferne. Jedoch geben die neuen Erkenntnisse den Hinweis, dass die offene Form geeigneter für den Angriff durch Wirkstoffe sein könnte als die starre, geschlossene Form des Proteins.
In kommenden Arbeiten wollen die Wissenschaftler um Professor Hagn auch den Einfluss des G-Protein-gekoppelten Rezeptors auf die Struktur des G-proteins untersuchen sowie die Rolle der anderen Untereinheiten des G-Proteins beim Schaltprozess erforschen. Entscheidend für diese Arbeiten ist dabei die exzellente Ausstattung des Bayerischen NMR-Zentrums, welche in den nächsten zwei Jahren auf dem Garchinger Campus der TU München um ein weiteres Hochfeld-Spektrometer erweitert wird.
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft
Meistgelesene News
Weitere News von unseren anderen Portalen
Verwandte Inhalte finden Sie in den Themenwelten
Themenwelt Spektroskopie
Durch die Untersuchung mit Spektroskopie ermöglicht uns einzigartige Einblicke in die Zusammensetzung und Struktur von Materialien. Von der UV-Vis-Spektroskopie über die Infrarot- und Raman-Spektroskopie bis hin zur Fluoreszenz- und Atomabsorptionsspektroskopie - die Spektroskopie bietet uns ein breites Spektrum an analytischen Techniken, um Substanzen präzise zu charakterisieren. Tauchen Sie ein in die faszinierende Welt der Spektroskopie!

Themenwelt Spektroskopie
Durch die Untersuchung mit Spektroskopie ermöglicht uns einzigartige Einblicke in die Zusammensetzung und Struktur von Materialien. Von der UV-Vis-Spektroskopie über die Infrarot- und Raman-Spektroskopie bis hin zur Fluoreszenz- und Atomabsorptionsspektroskopie - die Spektroskopie bietet uns ein breites Spektrum an analytischen Techniken, um Substanzen präzise zu charakterisieren. Tauchen Sie ein in die faszinierende Welt der Spektroskopie!