Natürliche Membranen für die Wasserstoffproduktion anpassen
Anzeigen
Ein für die Pflanzenbiologie zentraler chemischer Reaktionsweg wurde angepasst, um das Rückgrat eines neuen Prozesses zu bilden, der Wasser mit Hilfe von Sonnenenergie in Wasserstoff umwandelt.
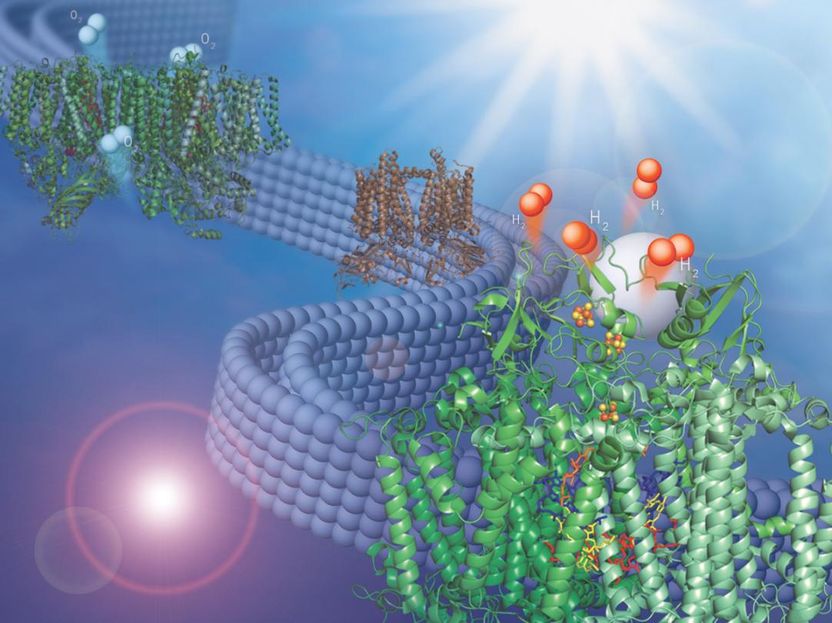
Dieses Bild zeigt zwei membrangebundene Proteinkomplexe, die zusammen mit einem synthetischen Katalysator Wasserstoff aus Wasser erzeugen.
Olivia Johnson and Lisa Utschig
In einer aktuellen Studie des U.S. Department of Energy's (DOE) Argonne National Laboratory haben Wissenschaftler zwei membrangebundene Proteinkomplexe kombiniert, um eine vollständige Umwandlung von Wassermolekülen in Wasserstoff und Sauerstoff durchzuführen.
Die Arbeit baut auf einer früheren Studie auf, die einen dieser Proteinkomplexe untersuchte, genannt Photosystem I, ein Membranprotein, das Energie aus Licht nutzen kann, um Elektronen an einen anorganischen Katalysator zu liefern, der Wasserstoff herstellt. Dieser Teil der Reaktion stellt jedoch nur die Hälfte des gesamten Prozesses dar, der für die Wasserstofferzeugung benötigt wird.
Mit einem zweiten Proteinkomplex, der Energie aus Licht nutzt, um Wasser zu spalten und Elektronen aus ihm zu entnehmen, dem Photosystem II, konnten die Argonne-Chemikerin Lisa Utschig und ihre Kollegen Elektronen aus dem Wasser nehmen und an Photosystem I weiterleiten.
"Die Schönheit dieses Designs liegt in seiner Einfachheit - Sie können den Katalysator selbst mit der natürlichen Membran zusammenbauen, um die Chemie zu machen, die Sie wollen" - Lisa Utschig, Chemikerin Argonne.
In einem früheren Experiment versorgten die Forscher Photosystem I mit Elektronen von einem Opfer-Elektronendonator. "Der Trick war, wie man zwei Elektronen in schneller Folge an den Katalysator bringt", sagte Utschig.
Die beiden Proteinkomplexe sind in Thylakoidmembranen eingebettet, wie sie in den sauerstoffbildenden Chloroplasten höherer Pflanzen vorkommen. "Die Membran, die wir direkt aus der Natur entnommen haben, ist für die Paarung der beiden Photosysteme unerlässlich", sagte Utschig. "Es unterstützt strukturell beide gleichzeitig und bietet einen direkten Weg für den Elektronentransfer zwischen Proteinen, behindert aber nicht die Bindung des Katalysators an das Photosystem I."
Das Z-Schema - so der technische Name für die lichtgesteuerte Elektronentransportkette der natürlichen Photosynthese in der Thylakoidmembran - und der synthetische Katalysator kommen laut Utschig recht elegant zusammen. "Die Schönheit dieses Designs liegt in seiner Einfachheit - Sie können den Katalysator selbst mit der natürlichen Membran zusammenbauen, um die Chemie zu machen, die Sie wollen", sagte sie.
Eine weitere Verbesserung war die Substitution von kobalt- oder nickelhaltigen Katalysatoren durch den teuren Platinkatalysator, der in der früheren Studie verwendet worden war. Die neuen Kobalt- oder Nickelkatalysatoren könnten die potenziellen Kosten drastisch senken.
Der nächste Schritt für die Forschung, so Utschig, sei die Integration des membrangebundenen Z-Schemas in ein lebendiges System. "Sobald wir ein in vivo-System haben - eines, in dem der Prozess in einem lebenden Organismus abläuft - werden wir wirklich sehen können, wie der Gummi in Bezug auf die Wasserstoffproduktion auf die Straße trifft", sagte sie.