COVID-19 neu ins Visier nehmen
Die verschlungenen RNA-Stränge des Coronavirus könnten neue Wege zur Behandlung von Infizierten eröffnen
Anzeigen
Für das ungeschulte Auge sehen die Schleifen, Knicke und Falten des einzigen RNA-Strangs, aus dem das Genom des Coronavirus besteht, wie ein Wirrwarr aus Spaghetti oder verheddertem Garn aus. Doch für Forscher wie Amanda Hargrove, Chemieprofessorin an der Duke University, könnten die komplexen Formen, die die RNA bei ihrer Faltung annimmt, ein bisher ungenutztes therapeutisches Potenzial im Kampf gegen Covid-19 haben.
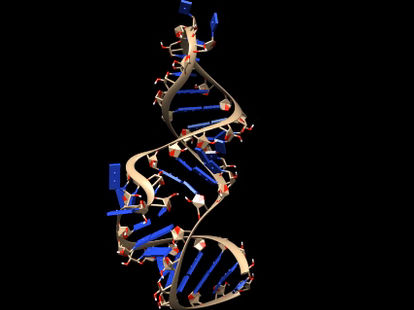
Die Forscher arbeiten an neuen Wegen zur Heilung von COVID-19-Infektionen, indem sie Moleküle verwenden, die an dreidimensionale Falten im genetischen Material des Virus binden.
Martina Zafferani, Duke University
In einer Studie haben Hargrove und Kollegen chemische Verbindungen identifiziert, die sich an diese 3D-Strukturen anheften und die Fähigkeit des Virus zur Replikation blockieren können.
"Dies sind die ersten Moleküle mit antiviraler Aktivität, die speziell auf die RNA des Virus abzielen, also ein völlig neuer Mechanismus", so Hargrove.
Selbst mehr als 18 Monate nach Beginn der Pandemie ist das eine gute Nachricht. Wir verfügen über Impfstoffe zur Vorbeugung von COVID-19, aber wirksame, einfach zu verabreichende Medikamente, die Menschen nach einer Infektion beim Überleben und bei der Genesung helfen, sind nach wie vor begrenzt.
Das Virus ist in einigen Teilen der Welt auf dem Rückzug, aber in anderen Regionen, in denen Impfstoffe knapp sind, häufen sich die Fälle immer noch. Und selbst in Regionen, in denen Impfstoffe leicht zugänglich sind, bedeutet das Zögern bei der COVID-19-Impfung, dass viele der acht Milliarden Menschen auf der Welt weiterhin anfällig für eine Infektion sind.
Um Ihre Zellen zu infizieren, muss das Coronavirus eindringen, seine genetischen Anweisungen in Form von RNA übermitteln und die molekulare Maschinerie des Körpers kapern, um neue Kopien von sich selbst herzustellen. Die infizierte Zelle wird zu einer Virusfabrik, die die 30.000 Nukleotid-"Buchstaben" des genetischen Codes des Virus abliest und die Proteine produziert, die das Virus zur Replikation und Verbreitung benötigt.
Die meisten antiviralen Medikamente - darunter Remdesivir, Molnupiravir und Paxlovid, die einzigen antiviralen Medikamente für COVID-19, die von der FDA zugelassen wurden oder zur Zulassung anstehen - wirken durch Bindung an diese Proteine. Hargrove und Kollegen verfolgen jedoch einen anderen Ansatz. Sie haben die ersten Moleküle identifiziert, die auf das virale Genom selbst abzielen - und zwar nicht nur auf die lineare Abfolge der A's, C's, G's und U's, sondern auf die komplexen dreidimensionalen Strukturen, in die sich der RNA-Strang faltet.
Als die ersten erschreckenden Hinweise auf die Pandemie Schlagzeilen machten, untersuchte das Team um Hargrove, Blanton Tolbert von der Case Western Reserve University sowie Gary Brewer und Mei-Ling Li von der Rutgers University bereits potenzielle Wirkstoffkandidaten zur Bekämpfung eines anderen RNA-Virus - des Enterovirus 71, das häufig die Hand-Fuß-Mund-Krankheit bei Kindern verursacht.
Sie hatten eine Klasse kleiner Moleküle, die so genannten Amiloride, identifiziert, die sich an haarnadelartige Falten im genetischen Material des Virus binden und die Replikation des Virus stören können.
Um herauszufinden, ob die gleichen Verbindungen auch gegen Coronaviren wirken könnten, testeten sie zunächst 23 Moleküle auf Amiloridbasis gegen ein anderes, weit weniger tödliches Coronavirus, das für viele Erkältungen verantwortlich ist. Sie identifizierten drei Verbindungen, die, wenn sie infizierten Affenzellen zugefügt wurden, die Virusmenge innerhalb von 24 Stunden nach der Infektion reduzierten, ohne dabei Kollateralschäden an den Wirtszellen zu verursachen. Außerdem zeigten sie bei höheren Dosen eine stärkere Wirkung. Ähnliche Ergebnisse erzielten die Forscher, als sie die Moleküle an Zellen testeten, die mit SARS-CoV-2, dem Virus, das COVID-19 verursacht, infiziert waren.
Weitere Arbeiten zeigten, dass die Moleküle den Aufbau des Virus durch Bindung an eine Stelle in den ersten 800 Buchstaben des viralen Genoms stoppten. Der größte Teil dieses RNA-Abschnitts kodiert nicht für Proteine selbst, sondern steuert deren Produktion.
Die Region faltet sich in sich selbst und bildet mehrere Ausbuchtungen und haarnadelartige Strukturen. Mithilfe von Computermodellen und einer Technik namens kernmagnetische Resonanzspektroskopie konnten die Forscher diese 3D-RNA-Strukturen analysieren und genau feststellen, wo die chemischen Verbindungen gebunden haben.
Die Forscher versuchen immer noch herauszufinden, wie genau diese Verbindungen das Virus an der Vermehrung hindern, sobald sie an sein Genom gebunden sind.
Was die Verwendung von RNA als Angriffspunkt für Medikamente betrifft, so befindet sich das Feld laut Hargrove noch in den Anfängen. Das liegt unter anderem daran, dass RNA-Strukturen instabil sind. Sie sind viel instabiler als ihre Protein-Gegenstücke, was es schwierig macht, Moleküle zu entwickeln, die mit ihnen auf spezifische Weise interagieren können.
"Die Bindungstasche, nach der man sucht, ist vielleicht die meiste Zeit gar nicht vorhanden", so Hargrove.
Hinzu kommt, dass 85 % der RNA in einer infizierten Zelle nicht zum Virus, sondern zu den Ribosomen - zelluläre Partikel, die aus RNA und Proteinen bestehen - des menschlichen Wirts gehören. "Die Konkurrenz ist riesig", so Hargrove.
Aber Hargrove ist hoffnungsvoll. Das erste niedermolekulare Medikament, das nicht an Proteine, sondern direkt an nicht-ribosomale RNA bindet, wurde erst im vergangenen August von der FDA zur Behandlung von Menschen mit einer verheerenden Krankheit namens spinaler Muskelatrophie zugelassen. "Es gibt zwar viele Herausforderungen, aber es ist nicht unmöglich", sagte Hargrove.
Die Forscher haben ein Patent auf ihre Methode angemeldet. Sie wollen die Verbindungen modifizieren, um sie wirksamer zu machen, und sie dann an Mäusen testen, "um zu sehen, ob dies ein brauchbarer Arzneimittelkandidat sein könnte", so Hargrove.
Dies ist nicht das erste Mal, dass Coronaviren einen Ausbruch verursacht haben, und es wird wahrscheinlich auch nicht das letzte Mal sein, sagen die Forscher. In den letzten zwei Jahrzehnten war dieselbe Virusfamilie für SARS verantwortlich, das 2002 in China auftrat und sich in mehr als zwei Dutzend Ländern ausbreitete, sowie für MERS, das 2012 erstmals in Saudi-Arabien gemeldet wurde.
Die Forscher stellten fest, dass die Schleifen und Ausbuchtungen der RNA, die sie identifizierten, durch die Evolution bei verwandten Coronaviren in Fledermäusen, Ratten und Menschen im Wesentlichen unverändert geblieben sind, einschließlich der Viren, die die Ausbrüche von SARS und MERS verursachten. Das bedeutet, dass ihre Methode möglicherweise mehr als nur SARS-CoV-2, das Virus, das COVID-19 verursacht, bekämpfen kann.
Es liegt auf der Hand, dass mehr antivirale Mittel eine wertvolle Waffe wären, damit wir bei der nächsten Pandemie besser vorbereitet sind. Mehr Medikamente zur Verfügung zu haben, hätte einen weiteren Vorteil: die Bekämpfung von Resistenzen. Viren mutieren mit der Zeit. Wenn man in der Lage wäre, Medikamente mit unterschiedlichen Wirkmechanismen zu kombinieren, wäre es unwahrscheinlicher, dass das Virus gegen alle gleichzeitig eine Resistenz entwickelt und damit unbehandelbar wird, so Hargrove.
"Dies ist eine neue Art, über antivirale Mittel für RNA-Viren nachzudenken", sagte Hargrove.
Hinweis: Dieser Artikel wurde mit einem Computersystem ohne menschlichen Eingriff übersetzt. LUMITOS bietet diese automatischen Übersetzungen an, um eine größere Bandbreite an aktuellen Nachrichten zu präsentieren. Da dieser Artikel mit automatischer Übersetzung übersetzt wurde, ist es möglich, dass er Fehler im Vokabular, in der Syntax oder in der Grammatik enthält. Den ursprünglichen Artikel in Englisch finden Sie hier.