Zellen vor schädlichem Eis retten
Eis kann Zellen in Kryo-Lagern auseinanderreißen: Polymere können die Lage retten
Anzeigen
Zelltherapien sind viel versprechend, um die Behandlung von Krebs- und Autoimmunerkrankungen zu revolutionieren. Aber diese Multimilliarden-Dollar-Industrie erfordert eine langfristige Lagerung der Zellen bei superkalten kryogenen Bedingungen, wobei sichergestellt werden muss, dass sie auch nach dem Auftauen noch funktionieren. Diese kalten Temperaturen lösen jedoch die Bildung und das Wachstum von Eis aus, das Zellen durchbohren und zerreißen kann. Die von den Chemikern Pavithra Naullage und Valeria Molinero von der University of Utah im Journal of the American Chemical Society veröffentlichten Forschungsergebnisse bilden die Grundlage für die Entwicklung effizienter Polymere, die das Wachstum von zellschädigendem Eis verhindern können.

Symbolisches Bild
Free-Photos, pixabay.com, CC0

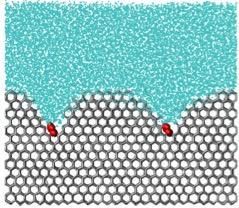
Eine Simulation eines eishemmenden Moleküls. Das Molekül, in rot, ist wie ein Gewicht auf der Oberfläche des Eiskristalls, das ihn krümmt und weiteres Eiskristallwachstum verhindert.
University of Utah

Frostschutzmittel der Natur
Aktuelle Strategien zur Kryokonservierung von Zellen und Organen beinhalten das Baden mit großen Mengen Dimethylsulfoxid, einer giftigen Chemikalie, die die Eisbildung verunreinigt, aber die Zellen belastet und ihre Überlebenschancen verringert.
Die Natur hat jedoch einen Weg gefunden, Organismen unter extremen Kältebedingungen am Leben zu erhalten: Frostschutzproteine. Fische, Insekten und andere kaltblütige Organismen haben starke Frostschutzglykoproteine entwickelt, die sich an Eiskristallite binden und diese am Wachstum und an der Schädigung von Zellen hindern.
Der wachsende Bereich der zellbasierten Therapeutika erfordert die Entwicklung potenter Inhibitoren der Eisrekristallisation, die in ihrer Aktivität mit natürlichen Frostschutzglykoproteinen konkurrieren können, aber nicht die Kosten und die Toxizität von Dimethylsulfoxid aufweisen. Diese Forderung hat die Synthese von Polymeren vorangetrieben, die die Wirkung von Frostschutzglykoproteinen imitieren. Aber der potenteste bisher gefundene synthetische Eis-Rekristallisationshemmer, Polyvinylalkohol (PVA), ist um Größenordnungen weniger potent als natürliche Glykoproteine.
"Die Bemühungen, stärkere Hemmstoffe für das Eiswachstum zu identifizieren, scheinen ins Stocken geraten zu sein, da es noch kein molekulares Verständnis der Faktoren gibt, die die Effizienz der Eisrekristallisationshemmung von Polymeren begrenzen", sagt Molinero.
Eine verborgene Polymer-Konstruktionsvariable
Wie verhindern Moleküle, dass Eiskristalle größer werden? Moleküle, die sich stark an das Eis binden, heften sich an dessen Oberfläche - wie Steine auf einem Kissen - und lassen die Eisfront eine gekrümmte Oberfläche um die Moleküle herum entstehen. Diese Krümmung destabilisiert den Eiskristall und stoppt sein Wachstum. Moleküle, die länger an Eis gebunden bleiben als die Zeit, die für die Bildung von Eiskristallen benötigt wird, verhindern erfolgreich weiteres Wachstum und Rekristallisation.
Molinero und Naullage verwendeten groß angelegte Molekularsimulationen, um die molekularen Grundlagen zu klären, wie Flexibilität, Länge und Funktionalisierung von Polymeren ihre Bindung an Eis und ihre Effizienz zur Verhinderung von Eiswachstum steuern. Ihre Studie zeigt, dass die Bindungszeit der Moleküle an der Eisoberfläche durch die Stärke ihrer Eisbindung in Verbindung mit der Länge des Polymers und der Geschwindigkeit ihrer Ausbreitung auf der Eisoberfläche gesteuert wird.
"Wir haben festgestellt, dass die Effizienz flexibler Polymere beim Stoppen des Eiswachstums durch die langsame Ausbreitung ihrer Bindung an Eis begrenzt ist", sagt Molinero.
Die Studie untersucht die verschiedenen Faktoren, die die Bindung von flexiblen Polymeren an Eis steuern und die die Lücke in der Wirksamkeit von PVA und natürlichen Frostschutzglykoproteinen erklären. Kurz gesagt, jeder Block der Frostschutzglykoproteine bindet stärker an Eis als PVA und wird auch durch ihre sekundäre Molekularstruktur begünstigt, die die bindenden und nicht bindenden Blöcke voneinander trennt, damit sie sich schneller an Eis anlagern können, um dessen Wachstum zu stoppen.
"Unseres Wissens nach ist diese Arbeit die erste, die den Zeitpunkt der Ausbreitung der Bindung als Schlüsselvariable für die Gestaltung effizienter eisbindender flexibler Polymere identifiziert", sagt Naullage. "Unsere Studie schafft die Voraussetzungen für das De-Novo-Design von flexiblen Polymeren, die die Effizienz von Frostschutzglykoproteinen erreichen oder sogar übertreffen und in der biomedizinischen Forschung einen Einfluss ausüben können.
Hinweis: Dieser Artikel wurde mit einem Computersystem ohne menschlichen Eingriff übersetzt. LUMITOS bietet diese automatischen Übersetzungen an, um eine größere Bandbreite an aktuellen Nachrichten zu präsentieren. Da dieser Artikel mit automatischer Übersetzung übersetzt wurde, ist es möglich, dass er Fehler im Vokabular, in der Syntax oder in der Grammatik enthält. Den ursprünglichen Artikel in Englisch finden Sie hier.





























































