Protein CD30 – vom Zeugen zum Täter
Anzeigen
Zellen bestimmter Blutkrebsformen wie des Hodgkin-Lymphoms tragen auf ihrer Oberfläche das Protein CD30. Das Molekül gilt aber nicht nur als Indikator für bestimmte bösartige Erkrankungen des Immunsystems, sondern erhöht selbst das Risiko für deren Entstehung, berichten Forscher des Helmholtz Zentrums München in der Zeitschrift Blood. Wie aus einer von der Deutschen Krebshilfe unterstützten Studie hervorgeht, wird eine stark erhöhte Anzahl an CD30-tragenden Zellen nach bestimmten viralen Infektionen, wie z.B. durch Epstein-Barr Virus (EBV) und bei Autoimmunerkrankungen, gebildet.
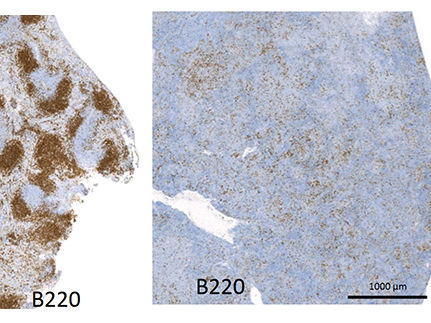
Gewebeschnitte der Milz eines gesunden Organismus (li.) und mit aktiviertem CD30 in den B-Lymphozyten (re.). Die B-Lymphozyten wurden jeweils spezifisch angefärbt (braun).
© Dr. Annette Feuchtinger, Abteilung Analytische Pathologie (AAP), HMGU
Die Studienergebnisse legen daher nahe, dass eine Impfung gegen EBV das Risiko für die Entstehung von Hodgkin-Lymphomen senken könnte. Zudem gibt die Studie Einblicke in neue Zielstrukturen für Arzneistoffe in der Tumortherapie.
Ärzte kennen das Protein CD30 bislang als diagnostischen Marker für bestimmte Blutkrebszellen, die B-Zell-Lymphome wie das Hodgkin-Lymphom. „Bisher war völlig unklar, ob die Bildung von CD30 auf der Oberfläche von Lymphom-Zellen nur Folge der Krebsentstehung ist oder ursächlich dazu beiträgt“, berichtet Privatdozentin Dr. Ursula Zimber-Strobl. Sie ist stellvertretende Leiterin der Abteilung Genvektoren (AGV) am Helmholtz Zentrum München. Zusammen mit ihrem Team hat sie deshalb ein Mausmodell entwickelt, um zu untersuchen, ob anhaltende CD30-Signale zur Blutkrebsentstehung führen.
Aktivierung von CD30 als Risikofaktor für Lymphome
„Im Experiment fanden wir heraus, dass die Wahrscheinlichkeit für die Entstehung eines B-Zell-Lymphoms stark erhöht ist, wenn B-Lymphozyten auf ihrer Oberfläche dauerhaft aktivierte CD30-Moleküle tragen“, berichtet Stefanie Sperling. Die Erstautorin ist Doktorandin in der AGV und Mitglied der Graduiertenschule HELENA. Diese dauerhafte Aktivierung von CD30 kann beim Menschen dadurch ausgelöst werden, dass das Immunsystem über einen längeren Zeitraum gefordert wird, wie beispielsweise beim Ausbruch des Pfeifferschen Drüsenfiebers (infektiöse Mononukleose) nach einer Infektion durch das Epstein-Barr Virus. Dann vermehren sich B-Lymphozyten, die CD30 auf ihrer Oberfläche tragen, sehr stark. In den meisten Fällen werden diese CD30-positiven Zellen schnell wieder eliminiert, können aber in seltenen Fällen durch fehlgeleitete Prozesse zu Tumoren führen. So ist das Risiko, direkt nach einem Pfeifferschen Drüsenfieber an einem Hodgkin-Lymphom zu erkranken, erhöht.
Details des Signalwegs noch unbekannt
Die Studienergebnisse eröffnen Zimber-Strobl zufolge Perspektiven für die Humanmedizin: „Die von CD30 ausgehenden Signalwege könnten sich als Zielstrukturen für neue Therapien bei Lymphomen eignen, sobald wir diese Wege genauer untersucht haben.“ Außerdem sei bei EBV die Entwicklung eines Impfstoffs zur Prävention einer Lymphom-Entstehung denkbar – ein Aspekt, den Forschende an der AGV gerade im Detail untersuchen.