Cartílago artificial con ayuda de la impresión 3D
Un nuevo enfoque para producir tejido artificial funciona con células en microestructuras de la impresora 3D
Anuncios
¿Es posible cultivar tejidos en el laboratorio, por ejemplo para sustituir cartílagos lesionados? En la TU Wien (Viena) se ha dado un paso importante hacia la creación de tejidos de sustitución en el laboratorio, utilizando una técnica que difiere significativamente de otros métodos utilizados en todo el mundo.
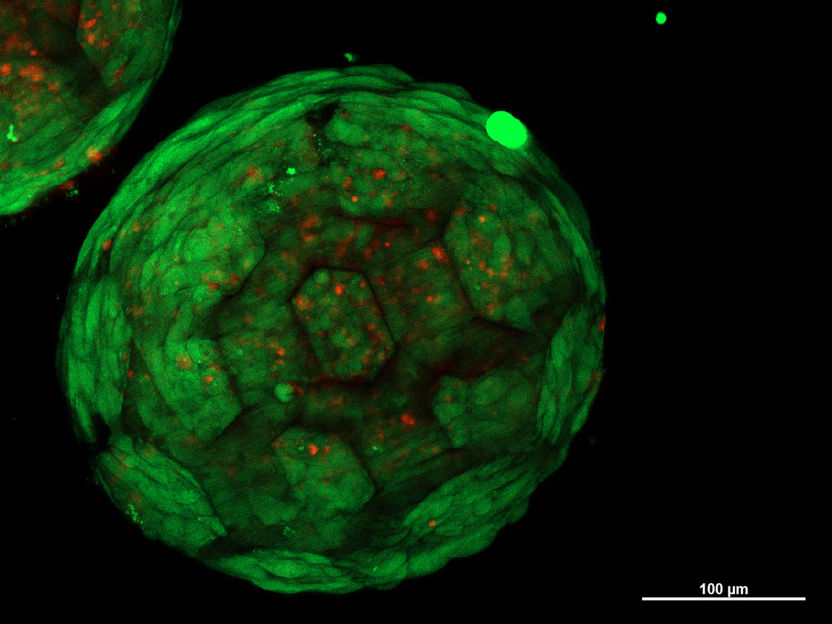
Uno de los esferoides
TU Wien
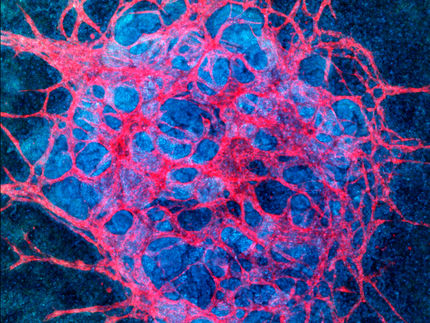
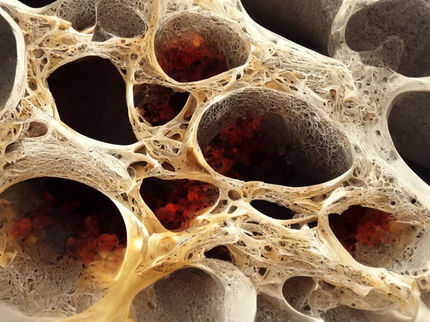
Mediante un proceso especial de impresión 3D de alta resolución se crean diminutas esferas porosas de plástico biocompatible y degradable, que luego se colonizan con células. A continuación, estos esferoides pueden disponerse en cualquier geometría, y las células de las distintas unidades se combinan a la perfección para formar un tejido vivo uniforme. El tejido cartilaginoso, con el que ahora se ha demostrado el concepto en la TU Wien, se consideraba hasta ahora especialmente difícil en este sentido.
Jaulas esféricas diminutas como andamio para las células
"Cultivar células de cartílago a partir de células madre no es el mayor reto. El principal problema es que normalmente se tiene poco control sobre la forma del tejido resultante", afirma Oliver Kopinski-Grünwald, del Instituto de Ciencia y Tecnología de Materiales de la Universidad Técnica de Viena, uno de los autores del presente estudio. "Esto también se debe al hecho de que tales aglomeraciones de células madre cambian su forma con el tiempo y a menudo se encogen".
Para evitarlo, el equipo de investigación de la TU Wien trabaja con un nuevo enfoque: se utilizan sistemas de impresión 3D de alta resolución basados en láser especialmente desarrollados para crear diminutas estructuras en forma de jaula que parecen mini balones de fútbol y tienen un diámetro de apenas un tercio de milímetro. Sirven de estructura de soporte y forman bloques compactos que pueden ensamblarse en cualquier forma.
Las células madre se introducen primero en estas mini jaulas con forma de balón de fútbol, que rápidamente llenan por completo el diminuto volumen. "De este modo, podemos producir de forma fiable elementos de tejido en los que las células están distribuidas uniformemente y la densidad celular es muy alta. Esto no habría sido posible con los métodos anteriores", explica el profesor Aleksandr Ovsianikov, director del grupo de investigación sobre impresión 3D y biofabricación de la Universidad Técnica de Viena.
Crecer juntos a la perfección
El equipo utilizó células madre diferenciadas, es decir, células madre que ya no pueden desarrollarse en ningún tipo de tejido, sino que ya están predeterminadas para formar un tipo específico de tejido, en este caso tejido cartilaginoso. Este tipo de células son especialmente interesantes para aplicaciones médicas, pero la construcción de tejidos más grandes supone un reto cuando se trata de células cartilaginosas. En el tejido cartilaginoso, las células forman una matriz extracelular muy pronunciada, una estructura en forma de malla entre las células que a menudo impide que diferentes esferoides celulares crezcan juntos de la forma deseada.
Si los esferoides porosos impresos en 3D se colonizan con células de la forma deseada, los esferoides pueden disponerse en cualquier forma deseada. La pregunta crucial ahora es: ¿se combinan también las células de diferentes esferoides para formar un tejido uniforme y homogéneo?
"Esto es exactamente lo que hemos podido demostrar por primera vez", afirma Kopinski-Grünwald. "Al microscopio se ve muy claramente: los esferoides vecinos crecen juntos, las células migran de un esferoide a otro y viceversa, se conectan sin fisuras y dan lugar a una estructura cerrada sin cavidades, a diferencia de otros métodos que se han utilizado hasta ahora, en los que quedan interfaces visibles entre los grupos de células vecinas."
Los diminutos andamios impresos en 3D confieren a la estructura general estabilidad mecánica mientras el tejido sigue madurando. Al cabo de unos meses, las estructuras de plástico se degradan, simplemente desaparecen, dejando tras de sí el tejido acabado con la forma deseada.
Primer paso hacia la aplicación médica
En principio, el nuevo enfoque no se limita al tejido cartilaginoso, sino que también podría utilizarse para adaptar distintos tipos de tejidos más grandes, como el tejido óseo. Sin embargo, aún quedan algunas tareas por resolver en el camino: después de todo, a diferencia del tejido cartilaginoso, en estos tejidos también habría que incorporar vasos sanguíneos a partir de cierto tamaño.
"Un objetivo inicial sería producir pequeñas piezas de tejido cartilaginoso a medida que pudieran insertarse en el material cartilaginoso existente tras una lesión", afirma Oliver Kopinski-Grünwald. "En cualquier caso, ahora hemos podido demostrar que nuestro método de producción de tejido cartilaginoso mediante microandamios esféricos funciona en principio y tiene ventajas decisivas sobre otras tecnologías."
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.