Amira Pharmaceuticals gibt positive Ergebnisse der Phase 1 für den führenden Produktkandidaten AM103 bekannt
Amira leitet klinische Studien für das 2. Eintrittmolekül zur Behandlung von Atemwegs- und Herz-Kreislauf-Erkrankungen ein
Amira Pharmaceuticals, Inc. gab den Abschluss der klinischen Prüfung der Phase 1 des Unternehmens für AM103 bekannt, dem von Amira entdeckten, oral verabreichten Arzneimittelkandidaten für die Behandlung entzündlicher Erkrankungen im Zusammenhang mit dem Leukotrien-Signalweg. Amira gab ausserdem den Start einer Phase-1-Studie für AM803 bekannt, einem zweiten oralen Arzneimittelkandidaten, der auf die gleiche Entzündungsreaktion abzielt.
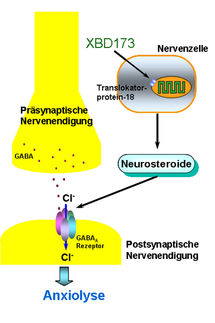
Bei AM103 und AM803 handelt es sich um neuartige Inhibitoren des 5-Lipoxygenase-aktivierenden Proteins (FLAP), die dank der Unterdrückung der Synthese von Leukotrienen - biologischen Verbindungen, die zur Entzündung führen - das Potenzial für die Behandlung von Asthma und kardiovaskulärer Erkrankungen demonstriert haben. Die kürzlich abgeschlossene AM103-Studie wurde aufgelegt, um die Sicherheit und Verträglichkeit einer steigenden Einzeldosierung und steigender Mehrfachdosierungen des Präparats bei gesunden Freiwilligen zu untersuchen, denen bis zu 11 Tage lang AM103 oder ein Placebo verabreicht wurde. In der Studie wurden ausserdem die pharmakodynamischen Eigenschaften von AM103, insbesondere ihre Fähigkeit, die Leukotrienproduktion zu hemmen, ausgewertet.
Die Ergebnisse der Phase-1-Studie zeigen, dass AM103 bei Dosen bis zu 1.000 mg pro Tag ohne Anzeichen von signifikanten Nebenwirkungen sicher und gut verträglich ist. Die systemische Exposition von AM103 wurde linear von 50 mg auf 1.000 mg erhöht.
Die pharmakodynamischen Daten demonstrierten eine stabile und statistisch signifikante Reduktion von LTB4 und LTE4 auf dosisabhängige Weise. "Die Ergebnisse dieser Studie haben unsere Erwartungen hinsichtlich der Sicherheit erfüllt und sogar übertroffen und liefern pharmakodynamische Beweise, die mit diesem Wirkungsmechanismus konsistent sind", sagte Peppi Prasit, Chief Scientific Officer von Amira. "Die Halbwertszeit von bis zu 10 Stunden bietet uns ausserdem die Möglichkeit, die einmal tägliche Dosis in einer Phase-2-Studie zu untersuchen, deren Beginn wir für das Jahr 2008 erwarten."
Meistgelesene News
Themen
Organisationen
Weitere News aus dem Ressort Forschung & Entwicklung

Holen Sie sich die Life-Science-Branche in Ihren Posteingang
Ab sofort nichts mehr verpassen: Unser Newsletter für Biotechnologie, Pharma und Life Sciences bringt Sie jeden Dienstag und Donnerstag auf den neuesten Stand. Aktuelle Branchen-News, Produkt-Highlights und Innovationen - kompakt und verständlich in Ihrem Posteingang. Von uns recherchiert, damit Sie es nicht tun müssen.