Exakten dreidimensionalen Aufbau des «Kuschelhormon»-Rezeptors bestimmt
Bauplan des Oxytocin-Rezeptors fördert Entwicklung neuer Autismus-Medikamente
Anzeigen
Das «Kuschelhormon» Oxytocin ist an diversen Störungen der psychischen Gesundheit und der Fortpflanzung beteiligt. Forscher der Universität Zürich haben nun den exakten dreidimensionalen Aufbau des Oxytocin-Rezeptors bestimmt, an den das Hormon bindet. Diese Kenntnis hilft, neue Medikamente zur Behandlung einer Reihe von Krankheiten zu entwickeln.

Oxytocin stärkt die Mutter-Kind-Beziehung und steuert soziale Bindungen, ist aber auch an diversen psychischen Störungen beteiligt (Symbolbild).
Photo by Guillaume de Germain on Unsplash
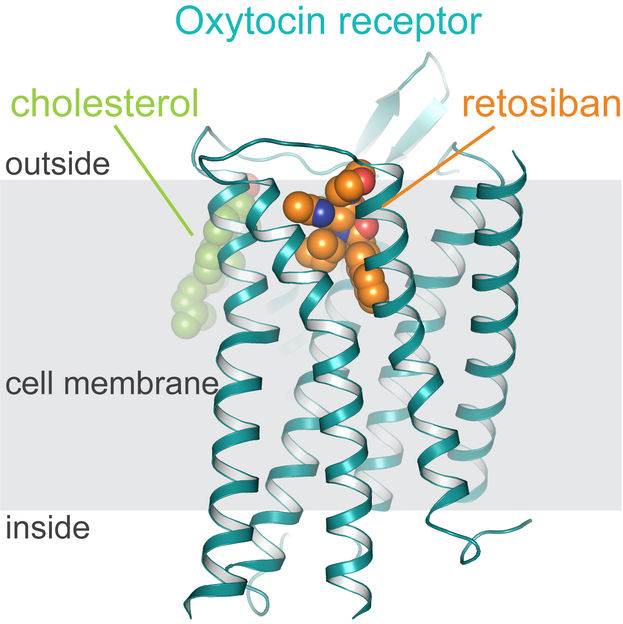
Struktur des Oxytocin-Rezeptors in der Zellmembran (grau), an das Retosiban (orange) und Cholesterol (grün) gebunden sind.
UZH

Das sogenannte «Kuschel- oder Liebeshormon» Oxytocin stärkt nicht nur die Mutter-Kind-Beziehung und beeinflusst soziale Bedingungen. Es spielt auch eine wichtige Rolle bei verschiedenen psychischen Erkrankungen wie Autismus, Asperger-Syndrom, sozialen Ängsten oder Suchtanfälligkeit. Darüber hinaus löst Oxytocin die Wehen aus, startet den Geburtsvorgang und ist an vielen Aspekten der Fortpflanzung – sowie entsprechenden Störungen – beteiligt. Seine vielfältigen Wirkungen löst das Hormon aus, indem es an den Oxytocin-Rezeptor bindet. Substanzen, die spezifisch auf den Oxytocin-Rezeptor zielen, haben daher ein grosses medizinisches Potenzial.
Schwierige Entwicklung neuer Medikamente
Seit seiner Entdeckung vor fast 30 Jahren versuchen Forschende, Medikamente zu entwickeln, die gezielt an den Oxytocin-Rezeptor binden. Die Experimente erwiesen sich jedoch als sehr schwierig. Mit Ausnahme des Hormons selbst ist kaum ein Medikament für den klinischen Einsatz zugelassen, das die Rezeptorfunktion beeinflusst. Ein Team unter der Leitung von Andreas Plückthun, Professor am Biochemischen Institut der Universität Zürich (UZH), hat nun den detaillierten dreidimensionalen Bauplan des Oxytocin-Rezeptors bestimmt. Konkret untersuchten sie, wie der Rezeptor aussieht, wenn Retosiban daran gebunden ist – ein Wirkstoff, der zur Unterdrückung vorzeitiger Wehen entwickelt wurde.
«Die Struktur des Oxytocin-Rezeptors zu ermitteln, war ein äusserst anspruchsvolles Unterfangen. Gelungen ist es nur dank der Kombination der Methoden der gerichteten Evolution und des Protein-Engineering, die von uns entwickelt wurden», sagt Plückthun. «Zu verstehen, wie Retosiban im atomaren Detail mit dem Rezeptor interagiert, dient als Blaupause für die Entwicklung neuer Therapeutika, die dessen Wirkung regulieren», ergänzt der Biochemiker.
Besseres Verständnis der Wirkungsweise
Die Wissenschaftler machten noch eine weitere Entdeckung. «Damit das von Oxytocin ausgelöste Signal effizient übermittelt werden kann, muss der Oxytocin-Rezeptor mit zwei weiteren Substanzen interagieren: Cholesterin und Magnesium», sagt Doktorand Yann Waltenspühl. Diese beiden Rezeptor-Regionen waren bisher nicht bekannt. «Ihre Identifizierung verbessert das Verständnis, wie der Rezeptor funktioniert, grundlegend», so der Erstautor der Studie.
Raschere Entwicklung neuer Therapeutika für diverse Krankheiten
Die neuen Erkenntnisse könnten auch direkt auf die sehr eng verwandten Vasopressin-Rezeptoren anwendet werden. Das Hormon Vasopressin steuert den Wassergehalt von Körperflüssigkeiten sowie den Blutdruck. Seine Rezeptoren sind daher Angriffspunkte für Arzneimittel zur Behandlung diverser Krankheiten – von Nierenerkrankungen bis hin zu Herzinsuffizienz. Wie der Oxytocin-Rezeptor sind auch die Vasopressin-Rezeptoren an Störungen des Autismus-Spektrums beteiligt. «Unsere Arbeit dürfte daher die Medikamentenentwicklung für ein breites Spektrum an weit verbreiteten und schweren menschlichen Erkrankungen fördern», schliesst Andreas Plückthun.




























































