La microfluidique rend la microscopie à super-résolution reproductible et conviviale
Une équipe de recherche internationale dirigée par l'université de Göttingen conçoit un système d'imagerie polyvalent
Annonces
Comprendre comment les cellules sont organisées et comment leurs composants moléculaires interagissent de manière coordonnée et coopérative est un objectif central des sciences de la vie modernes. Pour répondre à ces questions, les chercheurs doivent observer simultanément de nombreuses structures à l'intérieur d'une même cellule et cartographier la façon dont elles sont organisées et interagissent. Pour ce faire, il faut recourir à la "microscopie à super-résolution multiplexée", une méthode d'imagerie avancée qui révèle les détails cellulaires bien au-delà des limites des microscopes à lumière conventionnels. Cependant, les méthodes existantes sont souvent exigeantes sur le plan technique, difficiles à reproduire et mal adaptées aux échantillons biologiques fragiles. Une équipe de recherche internationale dirigée par l'université de Göttingen et le centre médical universitaire de Göttingen (UMG), dans le cadre du pôle d'excellence de Göttingen "Bioimagerie multi-échelle : Des machines moléculaires aux réseaux de cellules excitables" (MBExC), a entrepris de surmonter ces limitations. L'équipe a mis au point un système microfluidique spécialisé qui facilite la microscopie à super-résolution multiplexée, la rend plus reproductible et la rend accessible à une plus large communauté. Ces travaux ont été publiés dans la revue ACS Nano.

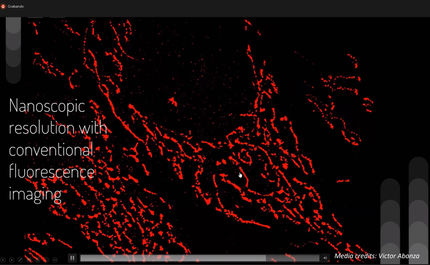
Image de super-résolution multiplexée de cibles à l'intérieur de la même cellule U2OS, prise à l'aide du système microfluidique nouvellement développé. Les molécules cibles de l'échantillon sont marquées avec de l'ADN présentant des séquences différentes mais de même couleur. Différentes protéines cibles peuvent être localisées avec une précision de l'ordre du nanomètre et superposées pour créer une image finale.
Adapted from the original publication in ACS Nano (2026). DoI: 10.1021/acsnano.5c18697
Pour vraiment comprendre le fonctionnement d'une cellule, les scientifiques doivent visualiser non pas un seul composant à la fois, mais de nombreuses protéines et structures spécialisées simultanément et voir comment elles interagissent à l'intérieur de la cellule. En outre, ces expériences deviennent de plus en plus complexes et sensibles à de petites variations, ce qui peut limiter la reproductibilité. Le nouveau système microfluidique injecte et retire avec précision les solutions de la chambre d'échantillon, remplaçant le pipetage manuel par une manipulation contrôlée et reproductible des fluides. "Le système que nous avons mis au point nous permet de maintenir une qualité d'image élevée pendant de longs cycles d'imagerie", explique le Dr Samrat Basak, premier auteur et chercheur postdoctoral actuellement en poste à l'université LMU de Munich. "En maintenant des conditions cohérentes entre les différentes étapes de marquage et de lavage, la plateforme microfluidique permet de cartographier directement les informations provenant de différentes cibles, ce qui rend possible l'imagerie des protéines, des structures spécialisées et des interactions complexes à l'intérieur de la cellule". Les chercheurs ont démontré cette technique sur des cellules cancéreuses humaines, révélant l'organisation des filaments de protéines à l'intérieur de la cellule. L'équipe a également appliqué la méthode à des cellules musculaires spécialisées isolées dans les ventricules d'un cœur de souris. "Les cellules musculaires spécialisées et fragiles du cœur sont particulièrement difficiles à imager", explique le premier auteur Kim-Chi Vu, UMG et MBExC. "Le système microfluidique était essentiel pour réaliser l'imagerie sans déformer les cellules ou les détacher de la surface.
La nouvelle machine peut être utilisée en mode manuel ou automatisé et est compatible avec une large gamme de systèmes d'imagerie. "L'idée de base était de développer un système rentable, adaptable et pouvant être modifié en fonction des besoins d'imagerie spécifiques de systèmes biologiques complexes", explique le Dr Roman Tsukanov, chercheur postdoctoral principal à l'université de Göttingen. "En automatisant l'échange de fluides, nous avons éliminé une source majeure de variabilité et rendu les protocoles d'imagerie complexes beaucoup plus conviviaux.
"Cette approche contribuera à normaliser l'imagerie de super-résolution multiplexée et à la rendre largement accessible, ce qui profitera à la fois à la recherche et aux applications médicales", ajoute le professeur Jörg Enderlein de la faculté de physique de l'université de Göttingen.
Note: Cet article a été traduit à l'aide d'un système informatique sans intervention humaine. LUMITOS propose ces traductions automatiques pour présenter un plus large éventail d'actualités. Comme cet article a été traduit avec traduction automatique, il est possible qu'il contienne des erreurs de vocabulaire, de syntaxe ou de grammaire. L'article original dans Anglais peut être trouvé ici.