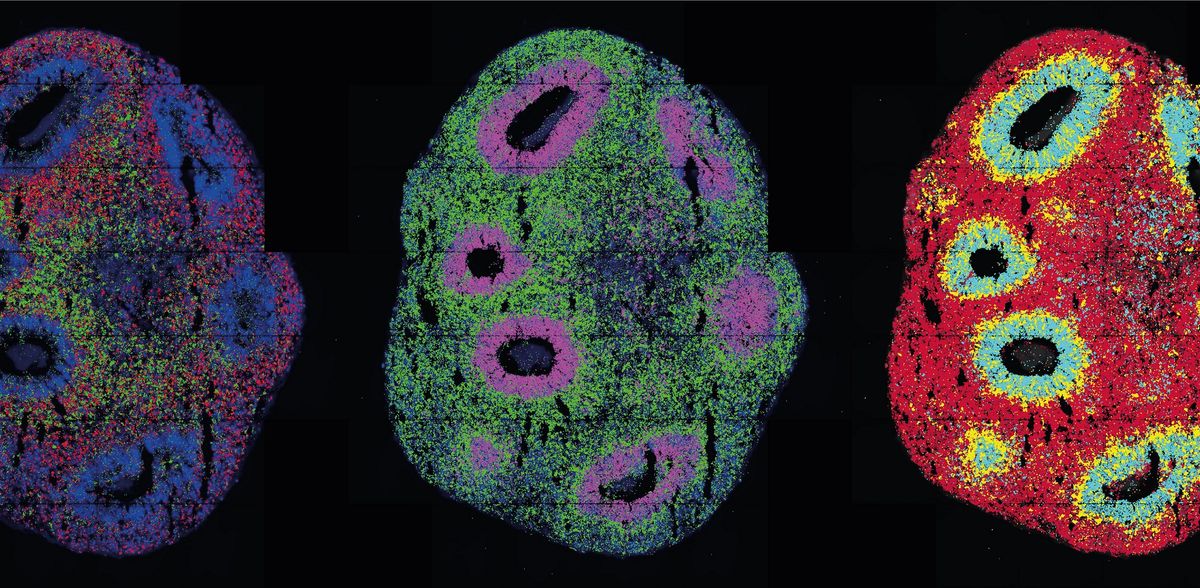
Concevoir des organoïdes avec de la lumière
Les organoïdes aident les chercheurs à comprendre les processus biologiques de la santé et de la maladie
Annonces
Ils ressemblent à des nuages d'orage au format d'une tête d'épingle : les organoïdes. Les cultures cellulaires tridimensionnelles jouent un rôle important dans la recherche médicale et clinique, car elles reproduisent les structures tissulaires et les fonctions organiques dans la boîte de Pétri. Elles permettent aux scientifiques de comprendre comment les maladies apparaissent, comment les organes se développent ou comment les médicaments agissent. Grâce à la technologie des cellules uniques, ils peuvent atteindre le niveau moléculaire des cellules. Grâce à la transcriptomique spatiale, ils peuvent même observer en 3D quels gènes sont actifs à quel endroit de l'organoïde au fil du temps.
Les "organes miniatures" sont généralement développés à partir de cellules souches. Ce sont des cellules qui ne sont pas encore ou à peine différenciées. Elles peuvent se développer en n'importe quel type de cellule, par exemple en cellules cardiaques ou rénales, en cellules musculaires ou en neurones. Pour ce faire, les scientifiques les "nourrissent" de facteurs de croissance et les placent dans une solution nutritive. Là, elles s'agglomèrent en de minuscules amas de cellules, dans lesquels elles finissent par fonctionner et interagir comme si elles se trouvaient dans un véritable tissu. Jusqu'à présent, il n'était guère possible de contrôler ce processus. Des chercheurs autour du professeur Nikolaus Rajewsky, directeur de l'Institut de biologie des systèmes médicaux du Max Delbrück Center (MDC-BIMSB) à Berlin, décrivent désormais dans la revue spécialisée "Nature Methods" une technologie qui leur permet de le déclencher, de le contrôler et de l'observer avec une résolution spatiale et temporelle. "Pour cela, nous avons combiné la transcriptomique spatiale avec l'optogénétique", explique le premier auteur, le Dr Ivano Legnini. "Ainsi, nous sommes non seulement en mesure de contrôler l'expression des gènes dans les cellules vivantes, mais aussi d'observer son évolution".
Des capteurs de lumière activent ou bloquent des gènes
En optogénétique, des "capteurs de lumière" naturels ou fabriqués artificiellement sont insérés dans des cellules. Lorsque la lumière tombe sur ces capteurs, ils activent ou bloquent les gènes dans les cellules - selon la manière dont ils sont programmés. Legnini a intégré de tels capteurs de lumière dans des cellules précurseurs de neurones développées à partir de cellules souches, qui devaient s'assembler en organoïdes neuraux. Pour ce faire, il a collaboré avec l'équipe de la plateforme technologique Organoïdes, dirigée par le Dr Agnieszka Rybak-Wolf, et le groupe "Biologie systémique de la différenciation des cellules et tissus neuronaux" du Dr Robert Patrick Zinzen. Les chercheurs ont voulu comprendre comment le système nerveux se développe dans l'embryon humain. Les morphogènes jouent un rôle clé dans ce processus - des molécules qui signalent aux cellules précurseurs neuronales si elles doivent devenir des neurones dans la partie antérieure du cerveau ou dans la partie postérieure de la moelle épinière, par exemple. La combinaison de ces molécules produit des modèles typiques d'expression génétique au cours du développement.
À l'aide de la lumière, les chercheurs ont activé l'un de ces morphogènes, à savoir Sonic-Hedgehog (SHH). Les analyses de cellules individuelles à résolution spatiale qui ont suivi ont montré que les cellules se sont ensuite organisées en organoïdes aux motifs typiques. Les chercheurs ont généré l'impulsion lumineuse de deux manières : soit à l'aide d'un microscope à laser, soit à l'aide d'un microscope numérique à micro-miroirs, que le groupe de Rajewsky a développé en collaboration avec le Dr Andrew Woehler. Andrew Woehler dirigeait à l'époque la plateforme de microscopie optique du Max Delbrück Center ; depuis novembre 2022, il est à la tête du département de technologie expérimentale du Howard Hughes Medical Institute à Ashburn, aux États-Unis. Une puce contenant plusieurs centaines de milliers de minuscules miroirs est insérée dans ce microscope spécial. Ceux-ci peuvent être programmés de manière à ce que le microscope puisse créer des motifs d'éclairage complexes sur un échantillon, contrairement à un laser qui ne touche qu'un seul point à la fois.
Précis - avec un potentiel d'amélioration
"Notre méthode nous permet de reproduire très précisément dans la boîte de Pétri des processus liés à l'expression des gènes dans les tissus", explique Ivano Legnini. Depuis mars de cette année, il met en place son propre groupe de travail à la Human Technopole de Milan. Il veut notamment y améliorer la résolution spatiale et temporelle de la technologie et la rendre applicable à d'autres organoïdes.
Nikolaus Rajewsky veut lui aussi continuer à peaufiner la méthode : "Je me réjouis beaucoup de collaborer avec des experts en optogénétique afin d'améliorer encore la technologie et de l'appliquer à des modèles d'organoïdes humains cliniquement pertinents".
Note: Cet article a été traduit à l'aide d'un système informatique sans intervention humaine. LUMITOS propose ces traductions automatiques pour présenter un plus large éventail d'actualités. Comme cet article a été traduit avec traduction automatique, il est possible qu'il contienne des erreurs de vocabulaire, de syntaxe ou de grammaire. L'article original dans Allemand peut être trouvé ici.