El ordenador cuántico resuelve el enigma de las proteínas
Entrevista con el Dr. Sandipan Mohanty, del Centro de Supercomputación de Jülich
El Dr. Sandipan Mohanty, físico y especialista en códigos, lleva 20 años trabajando en simulaciones de biología molecular para los superordenadores más rápidos del mundo. Estas simulaciones ayudan a desentrañar los componentes básicos de la vida y aportan nuevos conocimientos sobre la maquinaria celular. Ahora, junto con investigadores de la Universidad sueca de Lund, ha dado un paso más y ha llevado el problema del plegamiento de proteínas a un ordenador cuántico. El recocido cuántico JUPSI de D-Wave de la instalación de usuarios de ordenadores cuánticos JUNIQ del Forschungszentrum Jülich tiene más de 5.000 qubits y es el primer dispositivo de este tamaño fuera de Norteamérica. En una entrevista, Sandipan Mohanty nos habla de su trabajo pionero.

El recocido cuántico de onda D JUPSI de la infraestructura de computación cuántica JUNIQ del Forschungszentrum Jülich.
Forschungszentrum Jülich / Sascha Kreklau
¿Cuál era la tarea que se había propuesto, Dr. Sandipan Mohanty?
Yo diría que lo que realmente hemos conseguido es demostrar la viabilidad de los ordenadores cuánticos para cuestiones de investigación no triviales en nuestro campo. Los ordenadores cuánticos son una tecnología bastante nueva y aún no está claro cómo programarlos cuando se intenta resolver tareas científicas reales con estas nuevas máquinas. Por ejemplo, es bastante diferente de resolver el problema con la informática clásica de alto rendimiento.
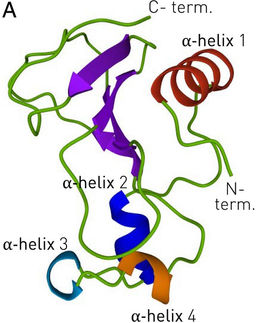
Más concretamente, hemos estudiado con éxito el plegamiento de proteínas utilizando un modelo muy sencillo. Las proteínas son importantes componentes básicos de la vida. Cumplen una gran variedad de tareas. Entre ellas están, por ejemplo, el transporte de sustancias y la estructura celular. Y sólo pueden cumplir todas estas funciones si tienen una forma muy específica, que consiguen mediante un proceso llamado plegamiento de proteínas. Una de las muchas razones por las que existe un gran interés en este proceso es la conexión entre enfermedades neurodegenerativas como el Alzheimer o el Parkinson con el mal plegamiento de las proteínas. Nuestra esperanza es que los ordenadores cuánticos ofrezcan importantes ventajas que hagan avanzar nuestra comprensión de tales fenómenos.
¿Por qué el plegamiento de proteínas es tan intensivo desde el punto de vista computacional?
Las proteínas son largas cadenas flexibles de aminoácidos. Una propiedad fascinante de estas moléculas es que una gran fracción de todas las proteínas se agrupan espontáneamente en formas tridimensionales muy específicas cuando las ponemos en una solución, pensemos en el agua. En principio, basta con conocer la secuencia de aminoácidos que componen una cadena proteica. La cadena sabe automáticamente qué forma tiene que adoptar.
Al modelizar este proceso de plegado en un ordenador, hay mucho que probar. Es como intentar calcular todas las formas posibles de colocar un collar para encontrar la "mejor". Además, examinar cada disposición es también muy costoso computacionalmente debido al gran número de partículas implicadas. Por lo general, hay que calcular millones de interacciones para cada disposición examinada.
¿Cómo funciona el ordenador cuántico en comparación con un ordenador digital clásico?
La tarea que resolvimos está a años de distancia en complejidad de los problemas que normalmente resolvemos con superordenadores clásicos, donde son habituales las simulaciones atómicamente detalladas a gran escala. En la máquina D-Wave utilizamos un modelo HP muy reducido. Esto simplifica enormemente el problema, conservando sólo las características físicas esenciales mínimas del proceso de plegado. Ignoramos el medio circundante, dividimos los aminoácidos en sólo dos tipos, aproximamos cada aminoácido por una única bola que sólo puede ocupar posiciones en una red.
Las simulaciones correspondientes también pueden realizarse de forma clásica. Para ello basta con un cuaderno de notas. El tiempo de cálculo no difiere mucho, en ambos casos se tarda de uno a dos minutos. Sin embargo, este valor en realidad no tiene sentido. Mucho más importante es la calidad de los resultados. Y aquí, el recocido cuántico rinde claramente mejor. Fue bastante fácil alcanzar el 100% de éxito en la búsqueda de las estructuras de menor energía en JUPSI. En cambio, con los ordenadores clásicos, las simulaciones comparables sólo alcanzan el 80 por ciento para una cadena de 30 aminoácidos. En el caso de las proteínas más complejas, formadas por bloques de 48 o 64 aminoácidos, lo hacen mucho peor, mientras que el recocido cuántico también produce siempre el resultado correcto en este caso.
¿Por qué el ordenador cuántico es más preciso que un ordenador clásico?
Porque se beneficia de aspectos específicos del problema de investigación. El esfuerzo computacional que requieren los ordenadores clásicos para tener en cuenta todas las conformaciones relevantes de las proteínas es astronómicamente alto. Crece exponencialmente con la longitud de la cadena de proteínas. Con una cadena de dos partículas, hay quizá diez posibilidades. Con tres partículas, ya hay cien. Pero con 100 partículas -que siguen siendo pocas para una proteína- habría que calcular miles de millones de veces más variaciones que átomos hay en el universo.
Para hacer cualquier cálculo significativo, hay que recurrir a muchos trucos. Tanto nuestro grupo en el JSC como mis colaboradores en Suecia están especializados en las llamadas simulaciones Monte Carlo. Se trata de un procedimiento basado en la física estadística y el muestreo estocástico. Aunque se garantiza que las simulaciones infinitamente largas producen resultados correctos, las cortas pueden tener grandes errores. En la práctica, se intenta realizar simulaciones "suficientemente largas", de modo que los errores estimados sean aceptablemente pequeños. Aquí reside la ventaja del recocido cuántico. Esta máquina puede, si se programa correctamente, realizar esta aproximación de forma muy directa a través de sus acoplamientos mecánicos cuánticos. Básicamente, es una especie de experimento de física intrincada que resuelve automáticamente la ecuación. En nuestro problema, parece tener el efecto de que se requieren tiempos de ejecución comparativamente menores para obtener respuestas muy buenas. Sin embargo, el hecho de que funcione tan bien en la práctica nos sorprendió un poco.
¿Qué perspectivas de aplicación abre esto a los ordenadores cuánticos?
Nuestro trabajo es sólo un primer paso. La mayoría de los ordenadores cuánticos actuales sólo tienen unos pocos qubits. El sistema D-Wave tiene 5000, que es mucho. Pero para la mayoría de los problemas de investigación, las aplicaciones fructíferas de los ordenadores cuánticos necesitarían aún más qubits. Todavía estamos muy lejos de simulaciones como las que se utilizan en la investigación de fármacos realizadas en superordenadores. Supongo que tendremos que esperar dos o tres generaciones más de dispositivos para poder resolver esos problemas en un ordenador cuántico.
Pero tengo esperanzas. A diferencia de las investigaciones existentes de las que hemos aprendido, nuestra formulación conserva su simplicidad al aumentar el tamaño del sistema. Esto abre un posible camino más suave hacia el estudio de problemas considerablemente más complejos en ordenadores cuánticos.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.