La luz impulsa la inyección
Acoplando un sistema de inyección bacteriano con un interruptor molecular controlado por luz, los científicos pueden inyectar proteínas en las células eucarísticas
Anuncios
Cuando bacterias como la Salmonella o la Yersinia provocan fiebre, diarrea o dolor abdominal, actúan pequeñas "agujas de inyección": su sistema de secreción de tipo 3, o T3SS para abreviar, dispara proteínas de virulencia bacteriana directamente a las células eucarióticas huéspedes. Los investigadores han pensado en utilizar dispositivos de inyección bacteriana para introducir proteínas en las células eucarióticas. Un equipo de investigación de Max Planck ha conseguido ahora controlar el sistema de inyección de forma optogenética, es decir, con luz. En el futuro esto permitirá utilizar el sistema en aplicaciones biotecnológicas o médicas.
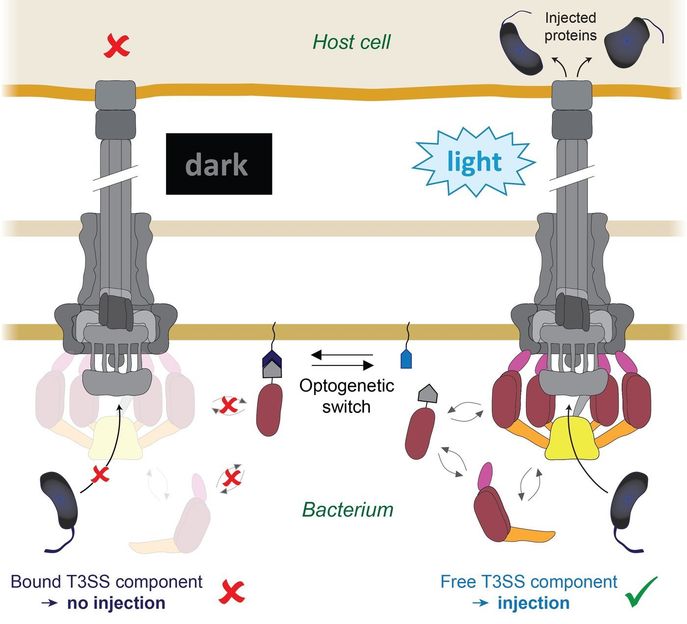
Principio molecular del sistema LITESEC. En la oscuridad (izquierda), un componente T3SS, que es necesario para la inyección (rojo), está anclado a la membrana bacteriana. Tan pronto como la bacteria se ilumina (derecha), el componente se libera. Así, la T3SS se activa y se pueden inyectar proteínas en la célula huésped (arriba).
© Max Planck Institute for terrestrial Microbiology/Diepold
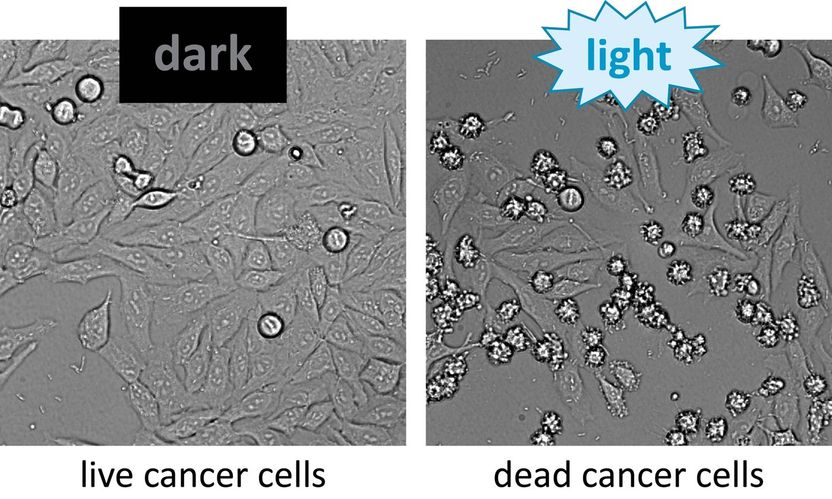
Izquierda: Células cancerígenas incubadas con la bacteria LITESEC, que inyectan una proteína pro-apoptótica y por lo tanto pueden llevar a la muerte celular. A la derecha: Bajo la iluminación, muchas células muertas en forma de estrella se ven después de una hora.
© Max Planck Institute for terrestrial Microbiology/Diepold
La T3SS es esencial para la virulencia de muchos patógenos humanos importantes, como Salmonella, Shigella y Escherichia coli, que causan varios millones de muertes al año. También es importante en las infecciones hospitalarias, por ejemplo por Pseudomonas aeruginosa, en las que la presencia de una SSTT funcional se asocia con una mayor mortalidad en modelos animales y una mayor resistencia a los antibióticos, una enfermedad grave y un mal pronóstico en los seres humanos infectados.
Por consiguiente, la T3SS se considera un objetivo central para posibles terapias que podrían perjudicar su función y prevenir infecciones. Por otra parte, el secuestro de este sistema bacteriano ofrecería la posibilidad de una entrega controlada de proteínas a las células huéspedes a través de la T3SS, como en un caballo de Troya. La inyección de proteínas a través de la T3SS es rápida y eficiente: un solo inyector puede transferir varios miles de proteínas efectoras en pocos segundos.
Sin embargo, tan poderoso como es el sistema de inyección de T3SS, está lejos de ser preciso, para gran decepción de los investigadores. "Tan pronto como un T3SS contacta con cualquier célula anfitriona, dispara su carga inmediatamente. Esto es desfavorable para las aplicaciones en biotecnología o medicina, donde queremos apuntar a tipos de células específicas, por ejemplo en la terapia de tumores", dice Andreas Diepold, jefe del grupo de investigación del Instituto Max-Planck de Microbiología Terrestre en Marburgo.
Inyección de proteínas a través de un interruptor de encendido/apagado
Pero ahora Andreas Diepold y su equipo han dado un gran paso hacia este objetivo: han conseguido controlar el inyector T3SS usando un interruptor de luz molecular. Esto permitirá a los científicos inyectar proteínas en las células eucarióticas en un momento y lugar precisos. "Durante mi beca postdoctoral en Oxford, descubrí que algunas partes de la T3SS son dinámicas", recuerda Andreas Diepold. "Se intercambian constantemente entre este aparato y el interior de la célula." El científico aplicó sus hallazgos al joven campo de investigación de la optogenética. El principio de esta técnica es que las interacciones de las proteínas pueden ser controladas con una velocidad de milisegundos cambiando su conformación cuando son estimuladas con luz de longitudes de onda específicas, permitiendo así un control rápido y específico de procesos moleculares definidos en los sistemas biológicos.
El doctor Florian Lindner acopló el componente dinámico T3SS con una parte de este interruptor de interacción optogénica, mientras que su otra parte estaba anclada a la membrana bacteriana. Exponiendo las bacterias y las células anfitrionas a la luz azul, la disponibilidad de los componentes T3SS y por consiguiente la función de la T3SS podía ser activada y desactivada.
Aplicando la LITESEC a la investigación de tumores
Como el sistema es flexible en cuanto a qué tipo de proteínas se inyectan, puede utilizarse de muchas maneras. En colaboración con Thorsten Stiewe de la Universidad Philipps de Marburgo, el grupo de investigación utilizó el nuevo sistema para atacar y matar las células tumorales cultivadas. El grupo ahora planea utilizar esta técnica para futuras investigaciones básicas y para el desarrollo de nuevas aplicaciones.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.








































