Una variante más precisa de Cas9
Las tijeras genéticas más específicas CRISPR-Cas9 hacen que la edición del genoma sea aún más precisa
Anuncios
CRISPR-Cas9 ha revolucionado el campo de la genética por su capacidad de cortar el ADN en sitios objetivos definidos. Los investigadores están utilizando la enzima Cas9 para apagar específicamente los genes, o insertar nuevos fragmentos de ADN en el genoma. Pero no importa cuán específica sea la enzima Cas9, a veces corta donde no debería. Los científicos de la Unidad Max Planck para la Ciencia de los Patógenos en Berlín y la Facultad de Medicina de la Universidad Martín Lutero de Halle-Wittenberg ahora reportan una variante de Cas9 que aumenta la especificidad de la edición del genoma.
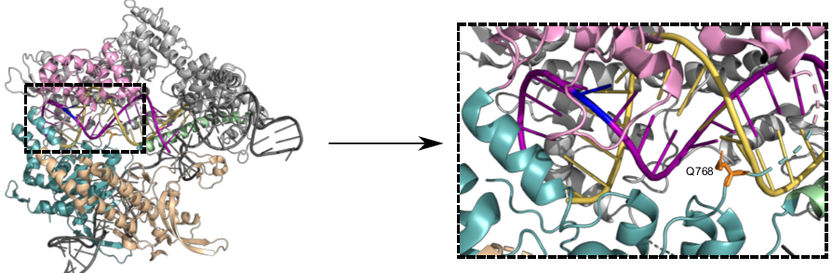
Estructura de Cas9 unida a un solo ARN guía (marco en gris oscuro, espaciador en amarillo) y a una hebra objetivo de ADN (púrpura). La modificación del residuo de aminoácido Q768 (naranja, cuadro discontinuo) da como resultado una variante más específica de Cas9.
© Bratovic et al., 2020
Para que el Cas9 corte una diana de ADN, necesita ser dirigido al sitio objetivo por lo que se llama ARN guía. El ARN guía contiene la secuencia complementaria al sitio objetivo del ADN, funcionando como un código postal para guiar a Cas9 hacia su objetivo. "A veces, sin embargo, Cas9 también puede cortar secuencias de ADN que son muy similares a la diana real, conocidas como "off-targets", explica Emmanuelle Charpentier, directora de la Unidad Max Planck para la Ciencia de los Patógenos.
Esta actividad indeseada de CRISPR-Cas9 puede llevar a inexactitudes en la edición del genoma. "Un corte no deseado en el lugar equivocado del genoma humano puede tener profundas consecuencias. Por eso necesitamos un sistema más específico", dice Michael Böttcher, profesor adjunto de la Facultad de Medicina de la Universidad Martin Luther.
Por lo tanto, los científicos están tratando de optimizar la especificidad de Cas9 utilizando diferentes enfoques. En el presente estudio, el equipo de investigadores de Berlín y Halle se centró en un dominio de Cas9 conservado evolutivamente, conocido como hélice de puente.
Los aminoácidos forman un bucle estable
Los investigadores descubrieron que la hélice de puente desempeña un papel fundamental en el mecanismo por el cual Cas9 interactúa con su ARN guía y el sitio objetivo del ADN. Identificaron un grupo de residuos de aminoácidos que entran en contacto con la columna vertebral de fosfato del ARN guía, facilitando así la formación de un bucle estable, que es esencial para la actividad de Cas9. En ese bucle, el ARN guía unido a Cas9 se empareja con la hebra complementaria de la secuencia diana de ADN mientras desplaza la segunda hebra de ADN, lo que permite a Cas9 cortar ambas hebras de ADN.
Los investigadores generaron nuevas variantes de Cas9 cambiando estos residuos de aminoácidos y encontraron que varias variantes cortan con mucha menos frecuencia en sitios fuera del objetivo que la enzima Cas9 original. Además, muestran que una de las variantes identificadas, llamada R63A/Q768A, aumentó la especificidad de la edición del gen de la Cas9 también en las células humanas. "Nuestros resultados proporcionan una nueva base para una mayor optimización de CRISPR-Cas9. Demuestran la necesidad de obtener más conocimientos sobre la bioquímica de los sistemas CRISPR-Cas para mejorarlos aún más", dice Charpentier.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.
Publicación original
Bratovic M, Fonfara I et al.; "Bridge Helix Arginines Play a Critical Role in Cas9 Sensitivity to Mismatches"; Nat. Chem. Biol.; 2 March, 2020