Gekoppelte Proteine
Wie menschliche Zellen auf externe Signale reagieren und diese weiterverarbeiten
Anzeigen
Mit neuen biotechnologischen Methoden haben Wissenschaftler der Universität Heidelberg und der Sendai-Universität in Japan untersucht, wie menschliche Zellen auf externe Signale reagieren und diese weiterverarbeiten. Im Mittelpunkt standen dabei die Wechselwirkungen zwischen sogenannten G-Proteinen – den „Vermittlern“ der Signalweiterleitung – und den Rezeptoren mit der Bezeichnung GPCRs, die Signalprozesse auslösen. Die Forscher haben nicht nur ein besseres Verständnis der GPCR-G-Protein-Interaktionen gewonnen; sie sind nun auch in der Lage, ihre Funktionen besser als zuvor vorherzusagen.
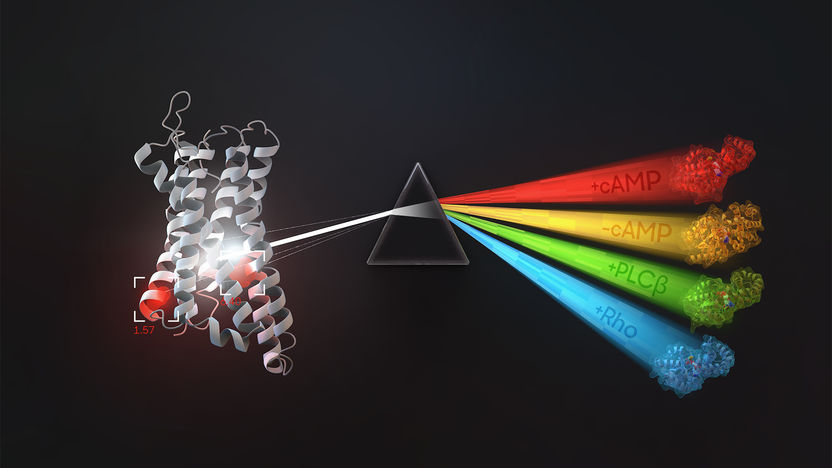
Die Grafik zeigt, welche G-Proteine an bestimmte G-Protein-gekoppelte Rezeptoren (GPCRs) binden und wie diese wiederum mit Signalereignissen zusammenhängen
© Thomas Splettstoesser (www.sci-style.com)
Alle lebenden Systeme reagieren auf Signale aus der Umwelt. Wahrgenommen und verarbeitet werden diese Signale bei Menschen und Tieren vor allem mithilfe von biologischen Rezeptoren in der Zellmembran, die mit dem G-Protein gekoppelt sind. Diese Proteine besetzen eine Schlüsselposition in der Signalweiterleitung. Die daran ankoppelnden GPCRs – der Name steht für G-Protein coupled receptors – stellen die größte Familie der Transmembranrezeptoren dar, die auf eine große Vielzahl an extrazellulären physikochemischen Signalen außerhalb der Zelle reagieren können und daraufhin spezifische Prozesse in der Zelle auslösen. Dies geschieht, indem sie beispielsweise an ein oder mehrere G-Proteine koppeln. Diese Kopplungen hat jetzt das Team von Prof. Dr. Robert Russell vom Biochemie-Zentrum der Universität Heidelberg gemeinsam mit den japanischen Kollegen untersucht.
Menschen besitzen insgesamt 16 G-Proteine, die an beinahe 1.000 verschiedene GPCRs gekoppelt werden. Mithilfe von biotechnologischen Werkzeugen und maschinellem Lernen haben die Wissenschaftler 148 repräsentative Rezeptoren sowie elf Proteine näher untersucht, um daran die gesamte Bandbreite an GPCR-G-Protein-Interaktionen besser verstehen zu können. Sie entschlüsselten dabei mehrere hundert Kopplungs-Events, die Aufschluss geben über die Rezeptoren und ihre Funktionsweise. „Dank der neuen Daten können wir nun besser als jemals zuvor GPCRs-G-Protein-Interaktionen vorhersagen. Dies erlaubt uns außerdem, künstliche GPCRs zu designen, die jeweils besondere Signalweg-Eigenschaften besitzen und somit effizient in biomedizinischen Studien eingesetzt werden können“, erläutert der Erstautor der Studie, Dr. Francesco Raimondi. Er ist Mitarbeiter im Team von Prof. Russell, dessen Forschungsgruppe auch am BioQuant-Zentrum der Universität Heidelberg angesiedelt ist. Die Wissenschaftler gehen davon aus, dass ein besseres Verständnis der Wechselwirkungen zwischen GPCRs und G-Proteinen auch für die Entwicklung neuer Medikamente von Bedeutung sein könnte.