Eiweiß-Origami reguliert Krebsenzym
Eiweißmoleküle - oder Proteine - in der Zelle liegen in einer dreidimensionalen Struktur vor, die darüber entscheidet, ob sie chemisch aktiv sind oder nicht. Wissenschaftler am Leibniz-Institut für Altersforschung – Fritz Lipmann-Institut e.V. (FLI) in Jena haben einen Zellmechanismus aufgeklärt, der ein Proteinmolekül wie ein Papier-Origami entfaltet und damit aktiviert. Das geöffnete Molekül spielt eine wichtige Rolle bei der Regulation eines Krebsenzyms. Die Wissenschaftler um Helen Morrison haben somit einen weiteren Baustein entdeckt, der zum Verständnis von Krebs beiträgt.
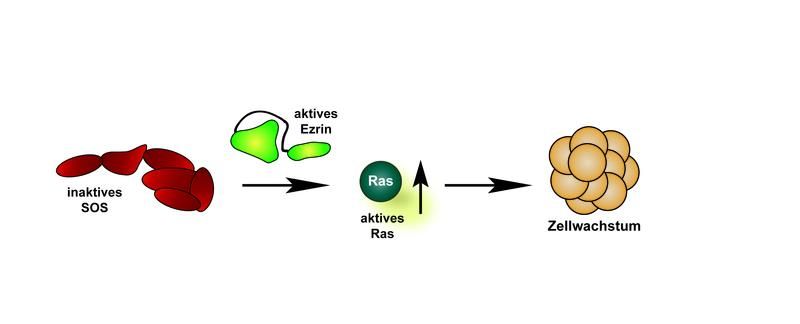
Die Aktivierung von Ras über SOS und Ezrin.
Katja Geißler, FLI.
Das entscheidende Gen heißt Ras. Es wurde 1981 als erstes Onkogen von dem amerikanischen Forscher Robert Allan Weinberg beschrieben. Ihm gelang damit der Nachweis, dass Mutationen im genetischen Code dieses Gens zu starkem Zellwachstum führen und damit zur Krebsentstehung beitragen. Das Ras-Enzym befindet sich an der Zellmembran. Es ist ein zentrales Glied in der Regulation verschiedener Wachstums- und Differenzierungsprozesse. „Bei 20-30 % aller menschlichen Tumoren ist zu viel Ras in der Zelle aktiv“, erklärt Katja Geißler, Erstautorin der Studie und Postdoktorantin am FLI. Dies kann zum einen darin begründet sein, dass durch eine Genveränderung zu viel Ras produziert wird, oder aber dass es Fehler in den Regulationsmechanismen der Ras-Aktivität gibt. Einen dieser Mechanismen haben die Forscher in Jena untersucht.
Krebsgen wird streng reguliert
Da Ras in der Zelle großen Schaden anrichten kann, wenn es in zu großer Menge oder in zu starker Aktivität vorhanden ist, wird das Enzym über verschiedene Mechanismen streng reguliert. Ein wichtiger Baustein dabei ist das Protein SOS (Son of sevenless). SOS ist ein großes, sehr komplexes Molekül, das zunächst eng zusammengefaltet in der Zelle vorliegt. Arbeiten kann es so nicht. Da Ras aber auf SOS angewiesen ist, um aktiv werden zu können, liegt in SOS ein Schlüssel zur Regulation. Erst wenn SOS entfaltet wird, kann es seinen Dienst tun.
Regulator wird aufgefaltet wie ein Papier-Origami
Wie aber kann SOS entfaltet werden? Dafür ist ein weiteres Protein notwendig, Ezrin. Dieses bindet direkt an SOS und bewirkt damit zwei Dinge: Zum einen öffnet es die komplexe Struktur von SOS, zum anderen stabilisiert es die Bindung zwischen SOS, Ras und der Zellmembran. Erst jetzt kann Ras aktiv arbeiten. „Ezrin ist gewissermaßen der Zündschlüssel der Maschinerie“, sagt Lars B. Riecken, der im Fritz-Lipmann-Institut seine Doktorarbeit anfertigt und an der Studie beteiligt war. „Funktioniert die Kontrolle von SOS z.B. durch Ezrin aber nicht perfekt, so kann Ras überaktiv werden. In der Folge wachsen Krebszellen.“
Maus, Ratte oder Mensch – der Mechanismus bleibt
Die Forscher in der Gruppe von Helen Morrison am FLI haben für ihre Untersuchungen mit verschiedenen Modellen gearbeitet. Zum einen natürlich mit den in der Grundlagenforschung üblichen Mäuse- und Rattenzellen. Zum anderen aber auch mit hoch gereinigten menschlichen Proteinen im Reagenzglas. Der Mechanismus der Aktivierung von Ras über Ezrin und SOS funktioniert immer gleich. Wenn man jetzt noch in Betracht zieht, dass im Januar 2012 in den USA ein Inhibitor für Ezrin gefunden wurde, so öffnet sich vielleicht ein weiteres Türchen auf dem Weg zu einer effektiven Krebstherapie. Der Inhibitor beeinträchtigt die Funktion von Ezrin. Er ist inzwischen für Laborzwecke käuflich zu erwerben.
Tumortherapie ist vielfältig
„Bis zu einem neuen Krebsmedikament ist es aber noch ein langer Weg“, sagen Katja Geißler und Lars B. Riecken. „In der Grundlagenforschung erarbeiten wir Puzzlestücke, die dann von der pharmazeutischen Forschung zusammengesetzt werden, um neue Wirkstoffe zu testen.“
Dies gilt umso mehr wenn man bedenkt, wie viele verschiedene Ansatzpunkte es inzwischen in der Krebstherapie gibt. Neben Strahlentherapie, Entfernen des Tumors durch Operation, Immuntherapie und Gentherapie ist die medikamentöse Chemotherapie die wichtigste Säule bei der Behandlung von Krebs. Der in Jena aufgeklärte Mechanismus bietet in Zukunft vielleicht die Möglichkeit, einen neuen Signaltransduktionshemmer zu entwickeln. Diese Medikamentengruppe wirkt direkt in der Tumorzelle und gilt damit als besonders verträglich für den Patienten.
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft
Meistgelesene News
Weitere News von unseren anderen Portalen
Verwandte Inhalte finden Sie in den Themenwelten
Themenwelt Gentherapie
Genetische Erkrankungen, die einst als unbehandelbar galten, stehen nun im Zentrum innovativer therapeutischer Ansätze. Die Forschung und Entwicklung von Gentherapien in Biotech und Pharma zielen darauf ab, defekte oder fehlende Gene direkt zu korrigieren oder zu ersetzen, um Krankheiten auf molekularer Ebene zu bekämpfen. Dieser revolutionäre Ansatz verspricht nicht nur die Behandlung von Symptomen, sondern die Beseitigung der Krankheitsursache selbst.

Themenwelt Gentherapie
Genetische Erkrankungen, die einst als unbehandelbar galten, stehen nun im Zentrum innovativer therapeutischer Ansätze. Die Forschung und Entwicklung von Gentherapien in Biotech und Pharma zielen darauf ab, defekte oder fehlende Gene direkt zu korrigieren oder zu ersetzen, um Krankheiten auf molekularer Ebene zu bekämpfen. Dieser revolutionäre Ansatz verspricht nicht nur die Behandlung von Symptomen, sondern die Beseitigung der Krankheitsursache selbst.