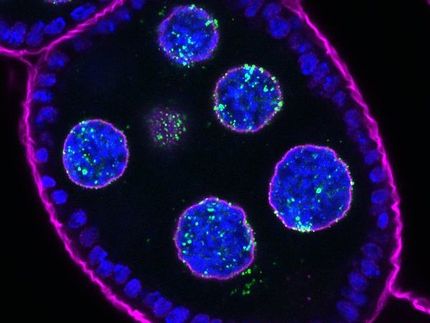
Forscher erzielen Durchbruch ins Zellinnere
Große Moleküle in lebende Zellen transportiert
Anzeigen
Es ist eine der großen pharmakologischen Fragen: Wie bringt man große funktionale Biomoleküle wie Proteine oder Antikörper in eine Körperzelle? Die Verknüpfung mit zellpenetrierenden Peptiden ist ein vielversprechender Weg – hat bislang jedoch noch nicht durchweg zu den erhofften Ergebnissen geführt. Jetzt präsentieren Forscher vom Leibniz-Forschungsinstitut für Molekulare Pharmakologie (FMP) in Berlin und der TU Darmstadt eine neue Lösung: Befestigt man diese Peptide zusätzlich an der Zelloberfläche, klappt es mit dem Transport ins Zellinnere um vieles besser. Die bahnbrechenden Ergebnisse sind soeben im Fachmagazin „Nature Chemistry“ erschienen.
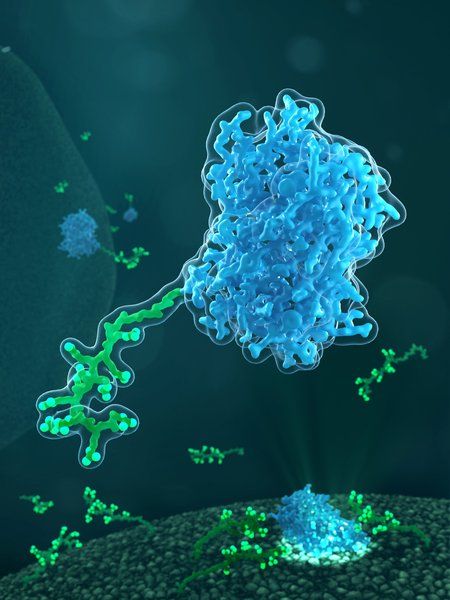
Zellpenetrierende Peptide (grün) auf der Zelloberfläche wirken als Türöffner für den Transport eines Proteins (blau) in lebende Zellen.
Barth van Rossum
Unser Zellinneres ist aus gutem Grund durch eine Zellmembran vor unerwünschten Besuchern geschützt. Aus pharmakologischer Sicht ist dieser Schutz jedoch ein lästiges Hindernis, da große Proteine oder Antikörper nur schwer bis gar nicht ins sogenannte Zytoplasma gelangen. Die meisten Medikamente umgehen diese Barriere, indem sie an der Zelloberfläche ansetzen. Wirkstoffe zellgängig zu machen, bleibt indes eine der drängenden Fragen für die biomedizinische Forschung und die Pharmaindustrie.
Schon seit mehr als zwei Jahrzehnten wird an zellpenetrierenden Peptiden geforscht. Dabei wird etwa ein Protein oder ein Antikörper mit einem chemischen oder biochemischen „Tag“ verknüpft, der das Eindringen in die Zelle erleichtern soll. Doch trotz weltweiter Bemühungen scheitern viele dieser Ansätze, wenn es um den Transport von solch großen Biomolekülen geht.
Auch die Arbeitsgruppe von Christian Hackenberger vom Leibniz-Forschungsinstitut für Molekulare Pharmakologie (FMP) in Berlin hat es sich zum Ziel gesetzt, zellgängige Proteine herzustellen und kooperiert dabei eng mit Dr. M. Cristina Cardoso von der TU Darmstadt, einer weltweit führenden Expertin auf dem Gebiet der zellpenetrierenden Peptide.
Doppelte Manipulation verbessert den Transport erheblich
Nun ist dem Forscherteam aus Berlin und Darmstadt ein entscheidender Schritt gelungen, sogar große Moleküle ins Zellinnere zu bringen. Der Trick: Die Forscher verknüpfen nicht nur diese Moleküle mit den zellpenetrierenden Peptiden, sondern auch die Zelloberfläche. Wie Experimente an lebenden Zellen zeigten, wird dadurch die intrazelluläre Aufnahme von funktionalen Proteinen und Antikörpern erheblich verbessert.
„Auch wenn wir von ersten medizinischen Anwendungen noch weit entfernt sind, stellt die Arbeit einen echten Paradigmenwechsel für den zellulären Transport von funktionalen Molekülen dar“, freut sich der Arbeitsgruppenleiter Christian Hackenberger. „Denn wir haben an lebenden Zellen zeigen können, dass Proteine und Antikörper nicht nur scheinbar mühelos die Zellmembran passieren können, sondern auch in der Zelle aktiv sind, ohne dabei eine Toxizität auszulösen.“
Die Fracht wird einfacher zellgängig
Ganz entscheidend für diesen Erfolg ist, dass mit dem neuen Verfahren nur rund ein Zehntel der bisher verwendeten Substanz-Konzentrationen benötigt wird. Das vereinfacht die Methode deutlich und macht sie robuster und vielseitiger. „Wir können die Konzentrationen jetzt so weit reduzieren, dass die Fracht wirklich verlässlich in das Innere der Zelle gelangen kann“, sagt der frisch promovierte Erstautor Anselm Schneider. „Das gab es vorher so noch nicht.“
Anselm Schneider hatte im Rahmen seiner Doktorarbeit die zündende Idee, die Zelloberfläche mit den gleichen zellpenetrierenden Peptiden auszustatten wie die Fracht, die in die Zelle hinein soll. Gemeinsam mit dem Leiter der Mikroskopie-Facility am FMP Martin Lehmann beobachtete er, wie die Zellmembran scheinbar mühelos durchbrochen wurde. „Es ist diese Synergie, die es nun ermöglicht, eine ganze Bandbreite an Molekülen ins Zellinnere zu transportieren, was im wahrsten Sinne des Wortes ein Durchbruch ist“, so Anselm Schneider.
Tür zu neuen pharmakologischen Interventionen aufgestoßen
Die Anwendungsmöglichkeiten des zellulären Molekültransports sind breit. Mit aktiven zellpermeablen Proteinen oder Antikörpern können etwa Signalwege in einer Krebszelle gezielt beeinflusst oder krebstreibende Gen-Mutationen ausgeschaltet werden. Denkbar ist auch der Ersatz eines fehlenden Enzyms zum Beispiel bei einer Erbkrankheit – bis hin zum Gene-Editing, also der genetischen Manipulation von Zellen durch bereits fertige Proteine, die man zudem mit weiteren Eigenschaften ausstatten kann. Es gibt also viel zu tun für das Forscherteam!
Originalveröffentlichung
Anzeigen
Weitere News aus dem Ressort Wissenschaft
Meistgelesene News
Weitere News von unseren anderen Portalen
Verwandte Inhalte finden Sie in den Themenwelten
Themenwelt Antikörper
Antikörper sind spezialisierte Moleküle unseres Immunsystems, die gezielt Krankheitserreger oder körperfremde Substanzen erkennen und neutralisieren können. Die Antikörperforschung in Biotech und Pharma hat dieses natürliche Abwehrpotenzial erkannt und arbeitet intensiv daran, es therapeutisch nutzbar zu machen. Von monoklonalen Antikörpern, die gegen Krebs oder Autoimmunerkrankungen eingesetzt werden, bis hin zu Antikörper-Drug-Konjugaten, die Medikamente gezielt zu Krankheitszellen transportieren – die Möglichkeiten sind enorm.
Themenwelt Antikörper
Antikörper sind spezialisierte Moleküle unseres Immunsystems, die gezielt Krankheitserreger oder körperfremde Substanzen erkennen und neutralisieren können. Die Antikörperforschung in Biotech und Pharma hat dieses natürliche Abwehrpotenzial erkannt und arbeitet intensiv daran, es therapeutisch nutzbar zu machen. Von monoklonalen Antikörpern, die gegen Krebs oder Autoimmunerkrankungen eingesetzt werden, bis hin zu Antikörper-Drug-Konjugaten, die Medikamente gezielt zu Krankheitszellen transportieren – die Möglichkeiten sind enorm.