TGN1412 – wichtiger Kofaktor identifiziert – Potenziale und Risiken superagonistischer Antikörper
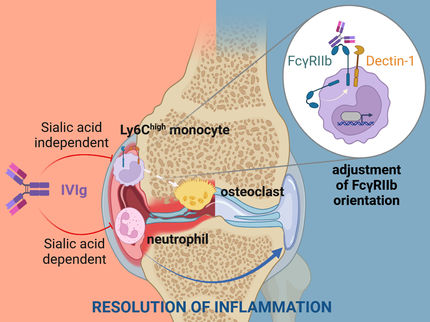
Vor sechs Jahren kam es bei einer klinischen Studie mit dem monoklonalen Antikörper TGN1412 bei den Studienteilnehmern zu einer Entgleisung des Immunsystems mit Multiorganversagen. Forscher des Paul-Ehrlich-Instituts haben jetzt die Interaktion des induzierbaren Kostimulators "ICOS" auf der T Zelle mit seinem Liganden "LICOS" auf der Endothelzelle als wichtigen Auslöser der Immunreaktion durch TGN1412 identifiziert. Dass über zwei kostimulatorische Signale eine polyklonale T Zellaktivierung induziert werden kann, zeigt zum einen die Möglichkeiten, zum anderen aber auch die Risiken solcher Antikörper.
Im März 2006 sorgte eine klinische Prüfung im Vereinigten Königreich für große Aufregung: In einer "First-in-Man"-Studie erhielten sechs gesunde Probanden den humanisierten monoklonalen Antikörper TGN1412. Der CD28-Superagonist befand sich in der klinischen Entwicklung u.a. zur Behandlung der rheumatoiden Arthritis. Bei allen Probanden kam es bereits kurz nach der Gabe von TGN1412 zu einer akuten massiven Freisetzung von immunologischen Botenstoffen (Zytokinsturm). Diese schwere lebensbedrohliche Entgleisung des Immunsystems machte eine intensivmedizinische Betreuung der Studienteilnehmer erforderlich und führte zu Gesundheitsschäden.
Wissenschaftler weltweit beschäftigen sich mit den immunologischen Prozessen in Verbindung mit dem "Superagonisten" TGN1412. Anders als bei einer normalen Aktivierung der T-Zelle über die spezifische Antigenbindung an seinen Rezeptor plus weiterer Gefahrensignale erfolgt die Aktivierung der T-Zelle durch einen solchen Superagonisten unabhängig vom T-Zell-Rezeptor. Allerdings konnte gezeigt werden, dass sich in vitro die periphere T-Zelle allein durch Zugabe von löslichem TGN1412 nicht aktivieren lässt. Es wurde seitdem postuliert, dass erst die Kreuzvernetzung beziehungsweise die Immobilisierung des monoklonalen Antikörpers über seinen konstanten Fc-Teil an den Fc-gamma-Rezeptor bestimmter Zellen die Aktivierung ermöglicht.
Die schnelle Immunreaktion der Studienteilnehmer nach TGN1412-Gabe ließ Immunologen des Paul-Ehrlich-Instituts (PEI) um die Nachwuchsgruppenleiterin PD Dr. Zoe Waibler vermuten, dass entweder Blut- oder Endothelzellen an den beobachteten Effekten beteiligt sind. Mit ihnen kommt der Antikörper bei intravenöser Gabe zuerst in Kontakt. Die Forscher konzentrierten sich auf humane Nabelschnurendothelzellen (HUVEC, human umbilical vein endothelial cells), das am besten etablierte Modell für humane Endothelzellen. Sie konnten tatsächlich zeigen, dass sich periphere T-Zellen durch TGN1412 allein nicht stimulieren lassen, in Anwesenheit der Endothelzellen dagegen schon. Völlig überraschend war jedoch der Befund, dass die Fc-gamma-Rezeptoren entgegen den bisherigen Annahmen für die Wirksamkeit der Endothelzellen bei der TGN1412-vermittelten T-Zellaktivierung keine Rolle spielten.
Welcher Bestandteil der Endothelzellen war nun aber für den beobachteten Effekt verantwortlich? Die PEI-Forscher untersuchten eine ganze Reihe kostimulatorischer Moleküle und machten schließlich die Interaktion zwischen dem induzierbaren Kostimulator "ICOS" auf der T Zelle des Immunsystems und seinem Liganden "LICOS" auf der Endothelzelle als Signal aus. Erst durch dieses zweite Signal kam es zur Aktivierung der T-Zelle. "Wir konnten zeigen, dass TGN1412 in Verbindung mit einem weiteren kostimulatorischen Signal eine antigenunabhängige T-Zellaktivierung herbeiführt", erläutert Waibler die Befunde, und ergänzt: "Dass die Fc:Fc-Rezeptor-Interaktion in diesem In-vitro-System keine Rolle spielt, war für alle völlig unerwartet."
Die antigenunabhängige Antwort bedeutet, dass – anders als bei der physiologischen Antwort – durch diesen Agonisten nicht ein T-Zell-Klon mit einem jeweils spezifischem T-Zell-Rezeptor aktiviert wird, sondern viele verschiedene. "Die Fähigkeit dieses Superagonisten, eine antigenunabhängige polyklonale T-Zellaktivierung herbeizuführen, zeigt das enorme therapeutische Potenzial, gleichzeitig aber auch die Risiken solcher immunaktivierenden Antikörper auf", betont Prof. Klaus Cichutek, Präsident des Paul-Ehrlich-Instituts. "Befunde wie diese tragen zu einem besseren Verständnis der immunologischen Prozesse bei. Dieses ist notwendig, um noch besser als bisher im Vorfeld klinischer Prüfungen die immunologische Reaktion solcher Superagonisten abschätzen zu können."
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft
Meistgelesene News
Weitere News von unseren anderen Portalen
Verwandte Inhalte finden Sie in den Themenwelten
Themenwelt Antikörper
Antikörper sind spezialisierte Moleküle unseres Immunsystems, die gezielt Krankheitserreger oder körperfremde Substanzen erkennen und neutralisieren können. Die Antikörperforschung in Biotech und Pharma hat dieses natürliche Abwehrpotenzial erkannt und arbeitet intensiv daran, es therapeutisch nutzbar zu machen. Von monoklonalen Antikörpern, die gegen Krebs oder Autoimmunerkrankungen eingesetzt werden, bis hin zu Antikörper-Drug-Konjugaten, die Medikamente gezielt zu Krankheitszellen transportieren – die Möglichkeiten sind enorm.
Themenwelt Antikörper
Antikörper sind spezialisierte Moleküle unseres Immunsystems, die gezielt Krankheitserreger oder körperfremde Substanzen erkennen und neutralisieren können. Die Antikörperforschung in Biotech und Pharma hat dieses natürliche Abwehrpotenzial erkannt und arbeitet intensiv daran, es therapeutisch nutzbar zu machen. Von monoklonalen Antikörpern, die gegen Krebs oder Autoimmunerkrankungen eingesetzt werden, bis hin zu Antikörper-Drug-Konjugaten, die Medikamente gezielt zu Krankheitszellen transportieren – die Möglichkeiten sind enorm.