Les dommages causés par les radiations à l'ADN paternel sont transmis à la progéniture.
Les dommages subis par le génome paternel ne peuvent être réparés et sont transmis à la progéniture, tandis que l'ovule femelle répare ou limite les dommages.
La question de savoir si l'exposition des pères aux rayonnements peut avoir des conséquences sur leurs enfants est l'une des questions les plus anciennes de la biologie des rayonnements. En utilisant le nématode Caenorhabditis elegans comme modèle, le professeur Dr Björn Schumacher et son équipe ont découvert que les dommages causés par les rayonnements aux spermatozoïdes matures ne peuvent pas être réparés mais sont au contraire transmis à la progéniture. En revanche, les ovules femelles réparent correctement les dommages ou, si les dommages sont trop graves, sont éliminés et aucun dommage n'est transmis. Cependant, lorsque l'ovule est fécondé par un spermatozoïde qui a été endommagé par des radiations, les protéines de réparation maternelles fournies par l'ovule tentent de réparer l'ADN paternel. À cette fin, un mécanisme de réparation très sujet aux erreurs est utilisé et fusionne les morceaux d'ADN cassés de manière aléatoire. Ces fusions aléatoires des cassures entraînent alors des modifications structurelles des chromosomes paternels. La progéniture qui en résulte est désormais porteuse des dommages chromosomiques et présente à son tour de graves défauts de développement. Les travaux réalisés sur C. elegans jettent les bases d'une meilleure compréhension des mécanismes des effets héréditaires de l'exposition paternelle aux rayonnements.
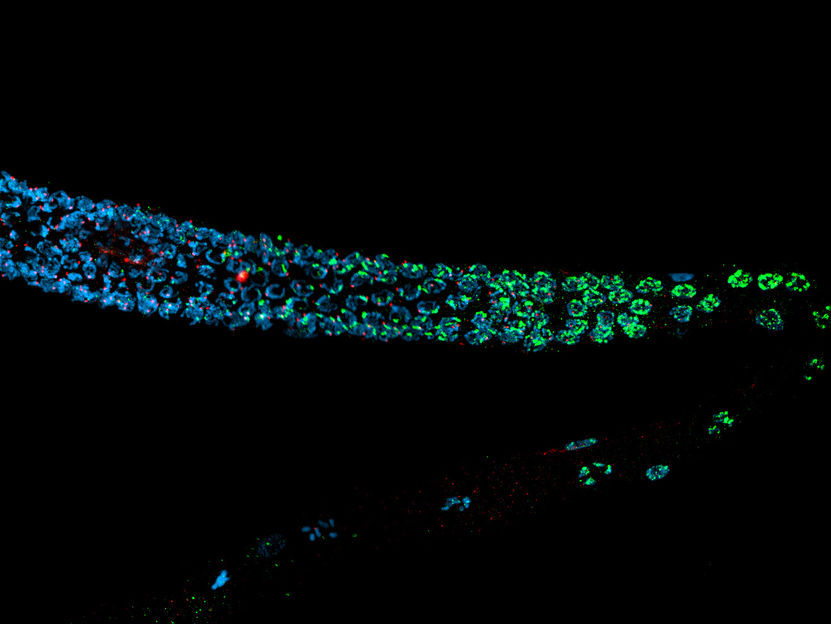
Image au microscope de C. elegans. ADN densément emballé dans les vers femelles. L'ADN est bleu, le marqueur d'histone H3K9me2 est vert, et le marqueur de chromosone X HIM-8 est rouge.
Siyao Wang, Universität zu Köln
Ces travaux ont été publiés dans la revue Nature sous le titre "Inheritance of paternal DNA damage by histone-mediated repair restriction" .
La progéniture issue d'animaux mâles exposés aux rayonnements et de femelles saines est porteuse de ce que l'on appelle des variations structurelles - des connexions aléatoires de parties de chromosomes. Dans la progéniture, ces aberrations entraînent des cassures récurrentes mais ces dommages ne peuvent plus être réparés. Au lieu de cela, les chromosomes endommagés sont protégés d'une réparation précise par des protéines, appelées histones, qui tassent densément les longs brins d'ADN. Dans cet ADN très dense, les cassures ne peuvent plus être atteintes par les protéines de réparation. Les structures compactes de l'ADN sont étroitement maintenues par des protéines histones spécifiques, HIS-24 et HPL-1. Lorsque ces protéines histones sont supprimées, les dommages hérités du père sont complètement éliminés et une progéniture viable peut être produite. La découverte que les protéines histones régissent l'accessibilité de l'ADN pour les réparations pourrait fournir des cibles thérapeutiques efficaces pour traiter les dommages causés par les rayonnements.
Cela concerne-t-il également les dommages causés par les rayonnements chez l'homme ? En plus des travaux sur les nématodes, l'équipe a détecté les mêmes variantes structurelles, ou chromosomes assemblés de manière aléatoire, chez l'homme. Ici aussi, les aberrations chromosomiques étaient spécifiquement transmises par les pères, mais pas par les mères. Pour cela, les scientifiques ont analysé différents ensembles de données provenant du projet 1000 Genome, qui contient les données génétiques de plus d'un millier de personnes, et du projet Islandic deCODE, qui contient les données génétiques des mères, pères et enfants respectifs.
"On pense que les aberrations du génome, en particulier les variations structurelles des chromosomes, qui se développent dans la lignée germinale paternelle, augmentent le risque de troubles tels que l'autisme et la schizophrénie", a déclaré Schumacher. Cela signifie que, chez l'homme également, le sperme mature doit être particulièrement protégé des dommages causés par les rayonnements et que les spermatozoïdes matures endommagés ne doivent pas être utilisés pour la conception. Il a ajouté : "De tels dommages peuvent potentiellement être infligés lors d'une radiothérapie ou d'une chimiothérapie et constituent donc un risque pendant les deux mois nécessaires à la génération de nouveaux spermatozoïdes pour remplacer celui qui est endommagé." En effet, contrairement aux spermatozoïdes matures, les spermatozoïdes nouvellement générés ont la capacité de réparer précisément les dommages.
Fait intéressant, les scientifiques ont trouvé ces variations structurelles dans les chromosomes également chez les nématodes à l'état sauvage et dans la population humaine. Ces résultats suggèrent que les dommages subis par les spermatozoïdes matures et la réparation imprécise de l'ADN paternel dans le zygote pourraient être des facteurs importants de la diversité génétique au cours de l'évolution et pourraient être responsables de maladies génétiques chez l'homme.
Note: Cet article a été traduit à l'aide d'un système informatique sans intervention humaine. LUMITOS propose ces traductions automatiques pour présenter un plus large éventail d'actualités. Comme cet article a été traduit avec traduction automatique, il est possible qu'il contienne des erreurs de vocabulaire, de syntaxe ou de grammaire. L'article original dans Anglais peut être trouvé ici.