Wie sich Nervenzellen auf das "Dauerfeuern" vorbereiten
Max-Planck-Forschern beobachten erstmals, wie Nervenzellen die Ausschüttung von Vesikeln über einströmendes Kalzium steuern / Einblicke in Schlüsselschritte der biologischen Signalübertragung
Wenn Nervenzellen elektrische Impulse feuern, führt eine erneute Stimulation in kurzem zeitlichen Abstand häufig zu einer erhöhten Ausschüttung von Botenstoffen und damit zu einer verstärkten elektrischen Antwort der nachgeschalteten postsynaptischen Zelle. Wenn wir zum Beispiel erschrecken, setzen neuroendokrine Zellen des Nebennierenmarks große Mengen von Adrenalin in die Blutbahn frei. Unsere Aufmerksamkeit und Reaktionsfähigkeit wird dadurch erhöht. Interessanterweise beruhen diese Vorgänge auf einem sehr ähnlichen Prozess - der kontrollierten Ausschüttung von Botenstoffen durch Freisetzung von Vesikeln.
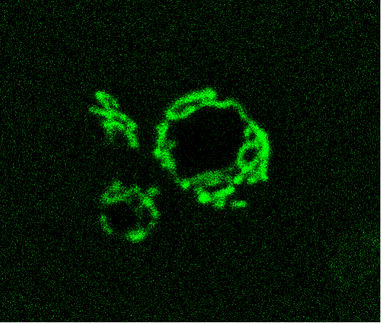
Neuroendokrine Zellen und Nervenzellen "verpacken" chemische Botenstoffe und Neurotransmitter in winzige, membranumhüllte Speicherbläschen, die Vesikel. Diese Container der Signalübertragung werden im Zellinneren gefüllt und an den Zellrand transportiert, wo sie erst nach einer Stimulation mit der äußeren Zellmembran verschmelzen. Dabei wird ihr Inhalt ausgeschüttet. Während bei der Hormonausschüttung typischerweise Hunderte von Vesikeln freigesetzt werden, bewirkt ein elektrischer Nervenimpuls häufig nur die Freisetzung eines einzelnen Bläschens. Die Fusion dieses Vesikels mit der Zellmembran löst eine kurzzeitige Erhöhung der Kalziumionen-Konzentration im Zellinneren aus. Dieser Anstieg erfolgt über spannungsabhängige Ionenkanäle in der Zellmembran: Durch eine elektrische Stimulation der Zelle öffnen sich diese Kanäle und Kalziumionen strömen ins Zellinnere. Kalzium-Sensormoleküle auf den Vesikeln detektieren diese erhöhte Kalziumkonzentrationen und leiten die Verschmelzung der Vesikel mit der Zellmembran ein.
Doch die Freisetzung der Vesikel erfolgt nicht automatisch: Nicht jede elektrische Erregung setzt ein Vesikel frei, und manche Ausschüttung geschieht spontan, ohne vorherigen Nervenimpuls. Bislang war bekannt, dass ein Vesikel erst dann freigesetzt wird, wenn die Kalziumkonzentration in der Zelle extrem steigt. Die beobachtete "Unzuverlässigkeit" der Datenübertragung ließe sich also dadurch erklären, dass die Kalziumkonzentration in der Nähe einzelner Vesikel unterschiedlich stark ansteigt. Das Kalzium wiederum gelangt durch spannungsabhängige Ionenkanäle, die durch einen elektrischen Nervenimpuls geöffnet werden, in das Zellinnere. Modellrechnungen sagen nun voraus, dass Vesikel vor allem dann freigesetzt werden, wenn sie sich in der Nähe von offenen Kalziumionenkanälen befinden.
Biophysikalische Experimente haben andererseits ergeben, dass sich Zellen vor zu hohen Kalziumkonzentrationen schützen, indem starke Kalziumpuffer den Großteil des einströmenden Kalziums wieder binden. Auf diese Weise begrenzen sie den Anstieg der intrazellulären Kalziumkonzentration räumlich und zeitlich. In Nervenzellen vergeht zwischen einer elektrischen Stimulation und der Freisetzung eines Vesikels weniger als eine tausendstel Sekunde. Diese Tatsache, zusammen mit der starken Abhängigkeit der Vesikelausschüttung von der Kalziumkonzentration, legen die Vermutung nahe, dass Kalziumionenkanäle und Vesikel dicht nebeneinander liegen sollten. Dann führt ein Kalziumeinstrom durch offene Ionenkanäle zu einem sprunghaften Anstieg der Kalziumkonzentration in der unmittelbarer Umgebung des an der Zellmembran verankerten Vesikels. Umgekehrt erklärt dieses Modell der "Kalzium-Mikrodomänen", warum die synaptische Übertragung manchmal auch nicht funktioniert: In diesem Fall sind Vesikel und Ionenkanal zu weit voreinander entfernt, so dass der Kalziumsensor des Vesikels diese Ionen nicht messen kann und die Verschmelzung mit der Zellmembran unterbleibt.
Meistgelesene News
Organisationen
Weitere News aus dem Ressort Wissenschaft

Holen Sie sich die Life-Science-Branche in Ihren Posteingang
Ab sofort nichts mehr verpassen: Unser Newsletter für Biotechnologie, Pharma und Life Sciences bringt Sie jeden Dienstag und Donnerstag auf den neuesten Stand. Aktuelle Branchen-News, Produkt-Highlights und Innovationen - kompakt und verständlich in Ihrem Posteingang. Von uns recherchiert, damit Sie es nicht tun müssen.