El "mecanismo de relojería" interno establece el tiempo para la división celular en las bacterias
Anuncios
Investigadores del Biozentrum de la Universidad de Basilea han descubierto un mecanismo de "relojería" que controla la división celular en las bacterias. En dos publicaciones, en "Nature Communications" y "PNAS", informan de cómo una pequeña molécula de señalización pone en marcha el "reloj", que informa a la célula sobre el momento adecuado para reproducirse.
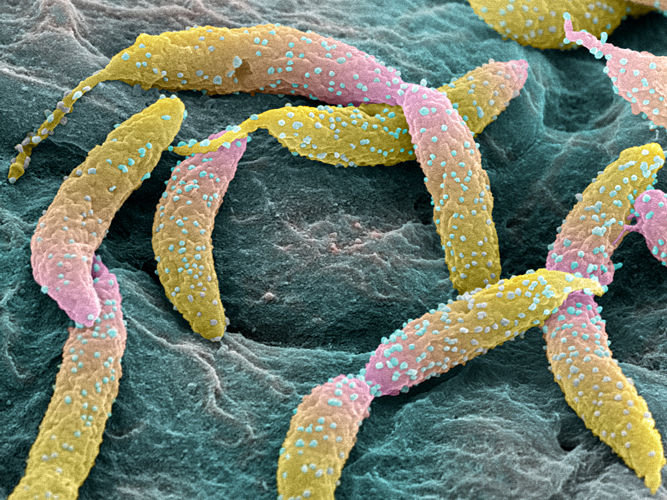
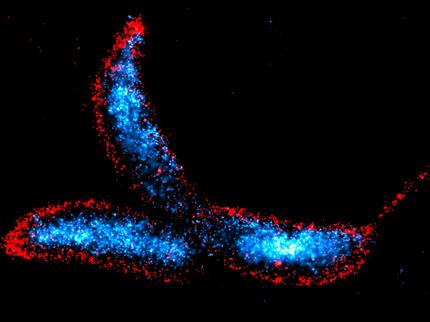
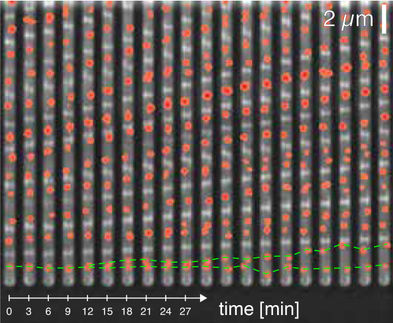
La molécula de señalización c-di-GMP controla la división celular en Caulobacter crescentus.
University of Basel, Swiss Nanoscience Institute/Biozentrum
La capacidad de los patógenos para multiplicarse en el huésped es crucial para la propagación de las infecciones. La velocidad de la división bacteriana depende en gran medida de las condiciones ambientales. En condiciones desfavorables, como la deficiencia de nutrientes, las bacterias tienden a detenerse después de la división y se reproducen más lentamente. ¿Pero cómo saben las bacterias cuándo es el momento de entrar en la siguiente ronda de división celular?
Un equipo del Biozentrum de la Universidad de Basilea, dirigido por el Prof. Urs Jenal, ha identificado ahora un interruptor central para la reproducción en la bacteria modelo Caulobacter crescentus: la molécula de señalización c-di-GMP. En su actual estudio, publicado en la revista Nature Communications, informan que esta molécula inicia un mecanismo "similar a un reloj", que determina si las bacterias individuales se reproducen.
Una molécula de señalización regula el "mecanismo de relojería" en las bacterias
Aún no se sabe cuánto tiempo se detiene una célula después de la división y cómo decide entonces participar en la siguiente ronda de división. La molécula de señalización c-di-GMP juega un papel clave en este proceso. "El aumento del nivel de c-di-GMP pone en acción las ruedas dentadas individuales del reloj de la célula, una tras otra", explica Jenal. "Estas ruedas dentadas son enzimas llamadas quinasas. Preparan la transición de la célula de la fase de reposo a la de división".
Las enzimas responden a los niveles de c-di-GMP
Bajo condiciones de vida favorables, las bacterias recién nacidas empiezan a producir la molécula de señalización - esto hace que el reloj comience a correr. El nivel inicialmente bajo de c-di-GMP activa una primera cinasa. Esto activa la expresión de más de 100 genes, que impulsan a la célula hacia la división y potencian la producción de c-di-GMP.
Los niveles máximos resultantes de c-di-GMP finalmente estimulan la última rueda de la maquinaria, también una cinasa. "Con este paso, la célula decide finalmente replicar su ADN y desencadenar la división celular", explica Jenal. "Simultáneamente los más de 100 genes se apagan de nuevo, ya que sólo son importantes para la fase de transición pero obstruyen las etapas posteriores de la proliferación".
Conocimiento de la activación de la enzima mediada por c-di-GMP
En un estudio paralelo, recientemente publicado en el PNAS, un equipo dirigido por el profesor Tilman Schirmer, también en el Biozentrum de la Universidad de Basilea, describe cómo el c-di-GMP activa la primera rueda dentada del recién descubierto reloj a nivel atómico.
Los investigadores han revelado que los dominios móviles de la quinasa están inicialmente bloqueados en una posición fija. La unión de c-di-GMP libera los dominios, activando así la cinasa para la expresión de los genes. "En nuestro estudio, hemos descubierto un nuevo modo de activación mediada por c-di-GMP", dice Schirmer. "Una vez más, estamos fascinados por la diversidad ʻstrategiesʼ de esta pequeña molécula para regular los procesos bioquímicos."
El principio universal en la reproducción de las bacterias
El c-di-GMP reguló el tiempo del ciclo celular bacteriano por esta molécula de señalización parece ser un mecanismo universal. Los investigadores asumen que este mecanismo permite a las bacterias coordinar con precisión el crecimiento y el desarrollo. El esclarecimiento de este novedoso mecanismo también contribuye a una mejor comprensión del crecimiento de los patógenos bacterianos.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.
Publicación original
Andreas Kaczmarczyk, Antje M. Hempel, Christoph von Arx, Raphael Böhm, Badri N. Dubey, Jutta Nesper, Tilman Schirmer, Sebastian Hiller and Urs Jenal; "Precise timing of transcription by c-di-GMP coordinates cell cycle and morphogenesis in Caulobacter"; Nature Communications; 2020.
Badri N. Dubey, Elia Agustoni, Raphael Böhm, Andreas Kaczmarczyk, Francesca Mangia, Christoph von Arx, Urs Jenal, Sebastian Hiller, Iván Plaza-Menacho, and Tilman Schirmer; "Hybrid histidine kinase activation by cyclic di-GMP–mediated domain liberation"; PNAS; 2020.