Une nouvelle méthode permet de charger l'ARNm dans les exosomes en 10 minutes : il suffit de mélanger et c'est parti !
Une équipe du KIST met au point une méthode basée sur les cubosomes pour charger des produits thérapeutiques volumineux sans endommager les exosomes
Annonces
Les exosomes, vésicules d'origine naturelle responsables de la communication intercellulaire, apparaissent comme des systèmes d'administration de médicaments de nouvelle génération capables de transporter des produits thérapeutiques vers des cellules spécifiques. Cependant, leurs membranes très serrées et riches en cholestérol rendent extrêmement difficile l'encapsulation de grosses molécules telles que l'ARNm ou les protéines. Les approches conventionnelles reposent sur des techniques telles que l'électroporation ou le traitement chimique, qui endommagent souvent les médicaments et les exosomes, réduisent l'efficacité de l'administration et nécessitent des étapes de purification complexes, ce qui constitue un obstacle important à la commercialisation.
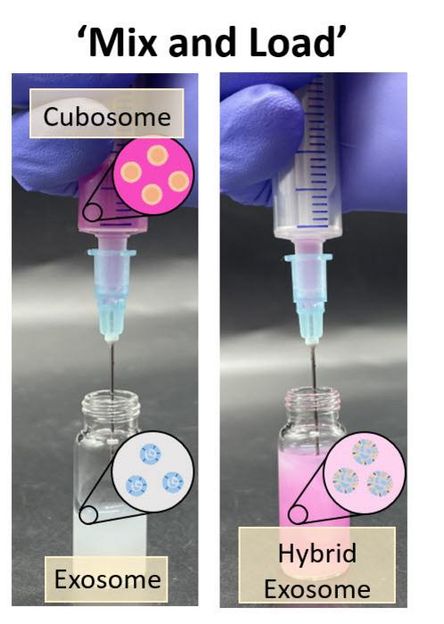
Représentation visuelle du processus de formation d'exosomes hybrides chargés d'une cargaison thérapeutique, obtenue simplement en mélangeant des cubosomes et des exosomes. La figure illustre la méthode de préparation actuelle, en soulignant la simplicité et la facilité de mise en œuvre, rendant le processus accessible sans équipement spécialisé.
Korea Institute of Science and Technology(KIST)
Une équipe de recherche conjointe dirigée par le Dr Hojun Kim du Center for Advanced Biomolecular Recognition et le Dr Hong Nam Kim du Center for Brain Convergence Research du Korea Institute of Science and Technology (KIST, Président Sang-Rok Oh) a mis au point une nouvelle technique de chargement des médicaments qui permet d'incorporer efficacement de grandes biomolécules dans les exosomes simplement en les mélangeant. Cette avancée permet une encapsulation stable des médicaments en moins de 10 minutes, sans qu'il soit nécessaire de recourir à un équipement spécialisé ou à un traitement complexe.
L'équipe a utilisé une nanoparticule à base de lipides appelée "cubosome", qui imite la structure de fusion des membranes cellulaires et fusionne naturellement avec les exosomes. En mélangeant des cubosomes porteurs d'ARNm avec des exosomes à température ambiante pendant seulement 10 minutes, les chercheurs ont obtenu une fusion efficace et ont confirmé que l'ARNm avait été chargé avec succès dans les exosomes. L'analyse a montré que plus de 98 % de l'ARNm était encapsulé, tandis que l'intégrité structurelle et la fonction biologique des exosomes étaient préservées.
En outre, les exosomes modifiés ont démontré leur capacité à traverser la barrière hémato-encéphalique, l'un des obstacles les plus difficiles à franchir en matière d'administration de médicaments. L'équipe a notamment observé un effet de "homing", c'est-à-dire que les exosomes retournent vers le type de cellule dont ils sont issus, ce qui permet de cibler l'administration de médicaments dans les tissus malades. Cette technologie permet de charger efficacement de grandes biomolécules sans altérer les exosomes eux-mêmes, ce qui ouvre la voie à des applications pratiques des thérapies à base d'exosomes dans la médecine de précision.
La technique est très adaptable aux environnements cliniques, car elle ne nécessite pas d'équipement spécialisé ni de traitement complexe. Elle préserve la fonction des exosomes tout en permettant l'administration de charges utiles importantes, ce qui offre un large potentiel pour le traitement de maladies incurables, notamment les troubles neurologiques, le cancer et les affections auto-immunes. L'équipe prévoit d'effectuer d'autres évaluations de sécurité en vue d'une application clinique et d'établir un système de production de masse pour les cubosomes.
Le Dr Hojun Kim, du KIST, a déclaré : "Cette technologie permet aux professionnels de la santé de combiner facilement les exosomes et les molécules thérapeutiques sur le site clinique, ce qui constitue une étape importante vers la réalisation d'une médecine personnalisée." Le Dr Hong Nam Kim a ajouté : "Parce qu'elle permet l'administration précise de médicaments, même dans des tissus complexes tels que le cerveau, elle présente un grand potentiel pour le traitement d'un large éventail de maladies."
Note: Cet article a été traduit à l'aide d'un système informatique sans intervention humaine. LUMITOS propose ces traductions automatiques pour présenter un plus large éventail d'actualités. Comme cet article a été traduit avec traduction automatique, il est possible qu'il contienne des erreurs de vocabulaire, de syntaxe ou de grammaire. L'article original dans Anglais peut être trouvé ici.










































