Schicksalhafter Faktor für Immunzellen
FOXP3 kontrolliert rund 90 Gene und verleiht regulatorischen T-Zellen ihre besonderen Fähigkeiten zur Vermeidung von Autoimmunkrankheiten
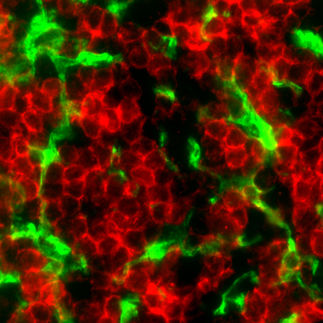
Dass unser Immunsystem nicht so leicht aus dem Gleichgewicht kommt, dafür sorgen bestimmte Immunzellen, die regulatorischen T-Zellen. Sie enthalten das Protein FOXP3 – einen so genannten „Transkriptionsfaktor“, der beeinflusst, welche Gene abgelesen werden. Wissenschaftler um Prof. Dunja Bruder vom Helmholtz-Zentrum für Infektionsforschung (HZI) und der Otto-von-Guericke Universität Magdeburg haben nun herausgefunden, dass FOXP3 rund 90 Gene direkt reguliert, unter anderem das Gen für den Botenstoff Interleukin-22.
Unser Immunsystem schützt uns vor vielen Krankheiten, es kann aber auch - wie im Falle von Autoimmunerkrankungen - „versehentlich“ den eigenen Körper angreifen. Damit das nicht so leicht passiert, gibt es verschiedene Arten von Immunzellen, die die Selbstangreifer stoppen. Dazu zählen auch die regulatorischen T-Zellen. Sie helfen, das Immunsystem im Gleichgewicht zu halten. Wissenschaftler und Ärzte interessiert, wie diese Zellen genau funktionieren, um dies für die Therapie von Autoimmunerkrankungen, Allergien oder auch zur Vermeidung von Transplantat-Abstoßungen gezielt auszunutzen.
Dass diese Zellen den Transkriptionsfaktor FOXP3 enthalten, war bereits seit längerem bekannt. Er bestimmt, welche von den Tausenden unserer Gene in einer regulatorischen T-Zelle an- oder abgeschaltet sein müssen, damit regulatorische T-Zellen funktionieren. „Menschen mit einer Mutation im FOXP3-Gen bilden keine funktionierenden regulatorischen T-Zellen. Dadurch gerät ihr immunologisches Gleichgewicht aus den Fugen und sie leiden unter schwersten Autoimmunerkrankungen, die viele Organe betreffen“, beschreibt Dunja Bruder die Wichtigkeit dieses Proteins. Die Professorin für Infektionsimmunologie am Universitätsklinikum Magdeburg und Leiterin der Arbeitsgruppe „Immunregulation“ am HZI erforscht mit ihrem Team, wie das Immunsystem im Gleichgewicht bleibt. Weil FOXP3 ein so entscheidendes Molekül für diese Zellen ist, haben die Wissenschaftler untersucht, welche Gene es direkt beeinflusst.
Um den regulatorischen T-Zellen dieses Geheimnis zu entlocken, haben sie eine neuartige Methode verwendet: "Durch die sogenannte ChIP-on-chip Analyse konnten wir sichtbar machen, an welchen Stellen unseres Erbmaterials das Protein bindet – ein Signal, dass ein Gen, das sich in unmittelbarer Nähe einer solchen Bindungsstelle befindet, jetzt an- oder ausgeschaltet werden soll“, erklärt der Immunologe und Erstautor der Studie Dr. Andreas Jeron. Für die ChIP-on-chip Analyse werden Zellen chemisch behandelt, so dass FOXP3 an der DNA-Sequenz, an die es gebunden hat, fixiert wird. Dann schneiden die Wissenschaftler das Erbmaterial in kleine Stücke und „angeln“ mit Antikörpern nach FOXP3. Weil FOXP3 fest mit der DNA verbunden wurde, fischen sie so auch die entsprechenden DNA-Abschnitte. Diese können sie farbig markieren und mittels eines DNA-Microarrays analysieren, der die DNA-Abschnitte rund 25.000 bereits bekannten sogenannten Promotorregionen des menschlichen Genoms zuordnen kann. Promotorregionen werden von Transkriptionsfaktoren wie FOXP3 häufig zum An- und Abschalten von Genen benutzt. Auf diese Weise identifizierten die Forscher 90 Gene, an deren Promotorregion FOXP3 bindet und diese somit direkt reguliert. Viele dieser Gene sind wichtig für die Aktivierung oder Co-Stimulation der regulatorischen T-Zellen.
Eines der Gene, das durch FOXP3 abgeschaltet wird, enthält den Bauplan für Interleukin-22 (IL-22). Dieses Molekül wird bekanntermaßen nicht von regulatorischen T-Zellen produziert, aber unter anderem von den nah verwandten Th17-Zellen. Anders als regulatorische T-Zellen, die überschießende Immunantworten gegen körpereigenes Gewebe verhindern, gelten Th17-Zellen als Mitverursacher von Autoimmunerkrankungen wie z.B. der rheumatoiden Arthritis. Zwar ist bekannt, dass es sich bei regulatorischen und Th17-Zellen um Untergruppen mit unterschiedlichen immunologischen Funktionen handelt. Unklar ist bislang jedoch, wie verhindert wird, dass sich schützende regulatorische T-Zellen in krankheitsverursachende Th17-Zellen umwandeln können. Die Ergebnisse der HZI-Forscher legen nahe, dass FOXP3 durch das Ausschalten von Genen wie IL-22 zu dieser Abgrenzung der Zelltypen, die auf verschiedene Aufgaben spezialisiert sind, beiträgt — Es macht die regulatorischen T-Zellen dauerhaft zu dem, was sie sind.“
„Diese Erkenntnis verdanken wir auch den modernen Screening-Methoden, mit denen wir im großen Maßstab die Gene einer Zelle untersuchen können“, so Dr. Robert Geffers, der am HZI die Abteilung „Genomanalytik“ leitet, in der die Erbsubstanz von Krankheitserregern und Immunzellen untersucht wird. „Das Ergebnis unserer Studie unterstreicht die wichtige Funktion von FOXP3. Es dient als molekularer Schalter für die direkte Regulation einer Vielzahl immunologisch bedeutender Gene in regulatorischen T-Zellen“ fasst Prof. Bruder zusammen. „Wir verstehen jetzt besser, welche Merkmale der Zellen auf diesen einen Transkriptionsfaktor zurückzuführen sind. Genau dieses verbesserte Verständnis der molekularen Funktion von FOXP3 ist im Hinblick auf eine sichere Anwendung regulatorischer T-Zellen in der Klinik absolut essentiell.“
Originalveröffentlichung
Andreas Jeron, Wiebke Hansen, Franziska Ewert, Jan Buer, Robert Geffers, Dunja Bruder ChIP-on-chip analysis identifies IL-22 as direct target gene of ectopically expressed FOXP3 transcription factor in human T cells BMC Genomics, 2012