Un nuevo algoritmo descubre los secretos de las fábricas de células
Sólo hay que probar las enzimas más prometedoras
Las moléculas de los medicamentos y los biocombustibles pueden fabricarse a medida en fábricas de células vivas, donde las enzimas biológicas hacen el trabajo. Ahora, investigadores de la Universidad Tecnológica de Chalmers han desarrollado un modelo informático capaz de predecir la velocidad de funcionamiento de las enzimas, lo que permite encontrar las fábricas vivas más eficaces, así como estudiar enfermedades difíciles.
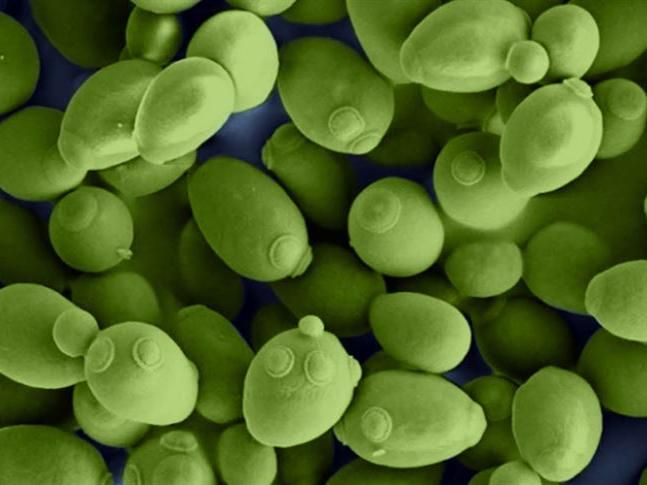
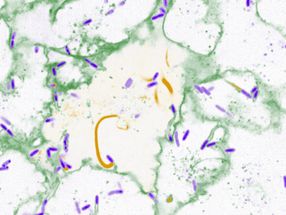
Los investigadores probaron su modelo simulando el metabolismo en más de 300 tipos de levaduras. Cuando se comparó con los conocimientos medidos y preexistentes, los investigadores concluyeron que los modelos con valores de kcat predichos podían simular con precisión el metabolismo. La imagen muestra la levadura de panadería común, Saccharomyces cerevisiae
Chalmers University of Technology
Las enzimas son proteínas que se encuentran en todas las células vivas. Su trabajo consiste en actuar como catalizadores que aumentan la velocidad de determinadas reacciones químicas que tienen lugar en las células. Así, las enzimas desempeñan un papel crucial en el funcionamiento de la vida en la Tierra y pueden compararse con las pequeñas fábricas de la naturaleza. También se utilizan en los detergentes y para fabricar, entre otras cosas, edulcorantes, tintes y medicamentos. Los usos potenciales son casi infinitos, pero se ven obstaculizados por el hecho de que el estudio de las enzimas es caro y requiere mucho tiempo.
"Estudiar cada enzima natural con experimentos en un laboratorio sería imposible, simplemente son demasiadas. Pero con nuestro algoritmo podemos predecir qué enzimas son las más prometedoras con sólo mirar la secuencia de aminoácidos que las componen", dice Eduard Kerkhoven, investigador en biología de sistemas de la Universidad Tecnológica de Chalmers y autor principal del estudio.
Sólo hay que probar las enzimas más prometedoras
El número de recambio de la enzima, o valor kcat, describe la rapidez y la eficacia de una enzima y es esencial para entender el metabolismo de una célula. En el nuevo estudio, los investigadores de Chalmers han desarrollado un modelo informático que puede calcular rápidamente el valor kcat. La única información necesaria es el orden de los aminoácidos que componen la enzima, algo que suele estar ampliamente disponible en bases de datos abiertas. Una vez que el modelo hace una primera selección, sólo hay que probar en el laboratorio las enzimas más prometedoras.
Dado el número de enzimas que existen en la naturaleza, los investigadores creen que el nuevo modelo de cálculo puede ser de gran importancia.
"Vemos muchas posibles aplicaciones biotecnológicas. Por ejemplo, se pueden producir biocombustibles cuando las enzimas descomponen la biomasa en un proceso de fabricación sostenible. El algoritmo también puede utilizarse para estudiar enfermedades del metabolismo, donde las mutaciones pueden provocar defectos en el funcionamiento de las enzimas del cuerpo humano", afirma Eduard Kerkhoven.
Más conocimientos sobre la producción de enzimas
Otras posibles aplicaciones son la producción más eficiente de productos elaborados a partir de organismos naturales, frente a los procesos industriales. La penicilina extraída de un moho es un ejemplo de ello, así como el medicamento contra el cáncer taxol del tejo y el edulcorante stevia. Los organismos naturales suelen producirlos en pequeñas cantidades.
"El desarrollo y la fabricación de nuevos productos naturales pueden verse muy favorecidos por el conocimiento de las enzimas que pueden utilizarse", afirma Eduard Kerkhoven.
El modelo de cálculo también puede señalar los cambios en el valor kcat que se producen si las enzimas mutan, e identificar los aminoácidos no deseados que pueden tener un impacto importante en la eficiencia de una enzima. El modelo también puede predecir si las enzimas producen más de un "producto".
"Podemos revelar si las enzimas tienen alguna actividad "pluriempleo" y producen metabolitos que no son deseables. Es útil en industrias en las que a menudo se quiere fabricar un único producto puro".
Los investigadores probaron su modelo utilizando 3 millones de valores de kcat para simular el metabolismo en más de 300 tipos de levaduras. Crearon modelos informáticos de la rapidez con la que las levaduras podían crecer o producir determinados productos, como el etanol. Cuando se compararon con los conocimientos medidos y preexistentes, los investigadores llegaron a la conclusión de que los modelos con valores de kcat predichos podían simular con precisión el metabolismo.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.