Descubierto el mecanismo de invasión del ADN de las vacunas adenovirales Covid-19
La liberación prematura de ADN activa los sistemas de alarma antivirales
Los adenovirus poseen una proteína linchpin que estabiliza su ADN hasta que llega al núcleo de la célula infectada. A continuación, la proteína se desprende del genoma viral y el virus se desprende. Sólo entonces se liberan los genes en el núcleo, lo que es necesario para la producción de nuevos virus. Este proceso, descubierto por investigadores de la Universidad de Zúrich, es clave para el funcionamiento eficaz de diversas vacunas Covid-19.
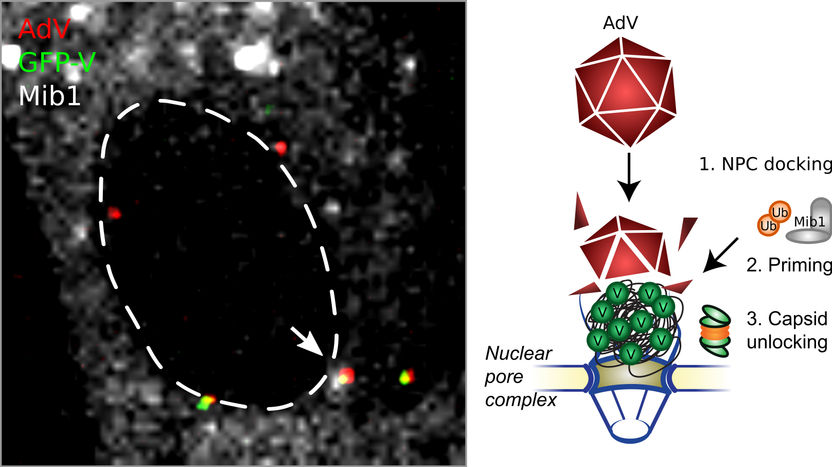
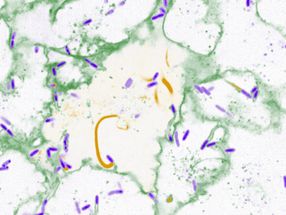
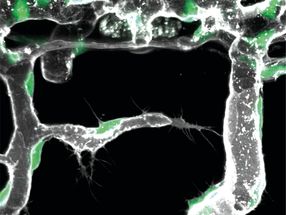
Las partículas entrantes de adenovirus (AdV) se acoplan a los complejos de poros nucleares del núcleo de una célula humana (NPC, línea discontinua). La enzima celular Mind bomb1 (Mib1, estructuras gris-blancas) las prepara para el desbloqueo y elimina la proteína V (GFP-V, puntos verdes). A continuación, el genoma de ADN viral sin recubrimiento se importa al núcleo. La flecha resalta una partícula de virus que contiene tanto la proteína V como la Mib1, el amarillo denota las partículas que contienen la proteína V, y el rojo muestra las partículas que carecen de V y Mib1.
Michael Bauer/Alfonso Gomez-Gonzalez, UZH
Los adenovirus causan enfermedades respiratorias en los seres humanos y se han utilizado como vectores en la vacunación durante muchos años, por ejemplo contra el MERS y el virus del Ébola. Varias vacunas Covid-19 se basan en adenovirus de replicación defectuosa, como los productos de AstraZeneca, Johnson & Johnson, CanSino Biologics y Sputnik V. Las células vacunadas producen la proteína de espiga del SARS-CoV-2 en su superficie y, por tanto, desencadenan una respuesta inmunitaria protectora en el cuerpo humano.
La proteína viral aumenta la estabilidad de la partícula del virus
Los investigadores están aprovechando una característica clave de los adenovirus, a saber, su capacidad para infectar células humanas y transferir ADN extraño al núcleo de estas células. Un nuevo estudio dirigido por Urs Greber, profesor del Departamento de Ciencias de la Vida Molecular de la Universidad de Zúrich (UZH), demuestra ahora que este proceso evolucionó mediante un sofisticado mecanismo. "La proteína viral V desempeña un papel clave. Conecta el ADN con la cubierta proteica que rodea el genoma. La proteína V aumenta la estabilidad de la partícula del virus fuera de la célula, y también en el citoplasma de las células infectadas", explica Greber.
La cubierta proteica impide que la célula reconozca el ADN extraño invasor y active los sistemas de alarma. Una vez que la partícula del virus alcanza el complejo de poros nucleares -la puerta de entrada al núcleo-, el ADN viral se libera en el núcleo, donde la maquinaria de la célula lee la información genética y produce las proteínas correspondientes. En las vacunas Covid-19, las células producen la proteína de la espiga en la superficie del coronavirus. La presentación de la proteína viral en el exterior de la célula desencadena entonces la respuesta inmunitaria en el cuerpo humano.
La liberación prematura de ADN activa los sistemas de alarma antivirales
Los científicos de la UZH han demostrado que un adenovirus al que le falta la proteína V no sólo es menos estable que los adenovirus normales, sino que además libera su ADN de forma prematura, antes de alcanzar el complejo de poros nucleares. "Esto reduce la infección y desencadena reacciones que activan el sistema inmunitario", dice Greber. Demasiadas de estas reacciones desencadenan la inflamación. En particular, tanto las vacunas basadas en vectores como las de ARNm contra el coronavirus requieren la cantidad justa de estas reacciones para inducir una fuerte respuesta inmunitaria.
En las vacunas basadas en vectores, la capa de proteína protectora que rodea al ADN permite que la partícula llegue al complejo de poros nucleares, donde se libera el ADN viral. Este "desencubrimiento" es absolutamente esencial para la importación nuclear, y el éxito en la vacunación basada en vectores, ya que el complejo de poros nucleares impide que las grandes partículas de virus invadan el núcleo. "Hemos podido demostrar que la proteína V aprovecha la activación por parte de una enzima celular llamada Mind bomb 1, que cambia sus características y conduce a la ruptura de la capa proteica. La enzima inicia así la importación nuclear del genoma del ADN viral", dice Greber.
Detener la infección viral y mejorar la terapia génica
Para demostrar esta función clave de Mind bomb1, los investigadores utilizaron adenovirus normales para infectar células humanas que carecían de Mind bomb 1, así como un virus mutante que contenía la proteína V, que no puede ser modificada por esta enzima. En ambos casos, la importación nuclear del ADN viral era defectuosa y las partículas del virus se agrupaban en los complejos de poros nucleares. En otras palabras, la infección viral se detuvo.
"Nuestros resultados inspiran el desarrollo de estrategias antivirales y mejoran los procedimientos para transferir genes a las células enfermas para la terapia clínica", afirma Urs Greber. En particular, los adenovirus se emplean de diversas maneras, como portadores de ADN para la edición de genes en enfermedades genéticas y metabólicas, así como en el cáncer.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.